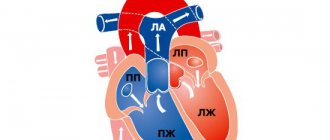
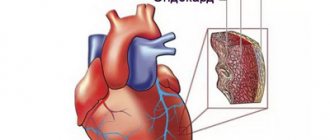
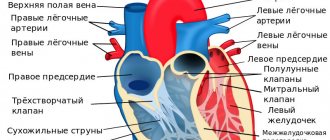
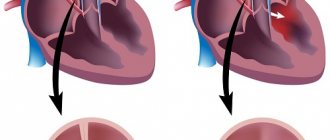
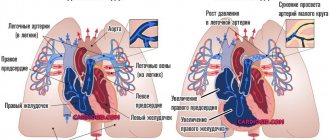
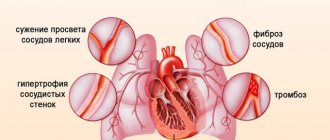
Наш организм устроен таким образом, что повредив один орган, страдает целая система, в итоге это влечет за собой общую истощаемость организма. Основным органом в жизнедеятельности человека является сердце, которое состоит из трех основных прослоек. Одной из самых важных и восприимчивой к повреждениям считается миокард. Данный слой — это мышечная ткань, которая состоит из поперечных волокон. Именно эта особенность позволяет сердцу работать в разы быстрее и эффективнее. Одной из основных функций является сократительная способность миокарда, которая может со временем понижаться. Именно причины и последствия данной физиологии и следует тщательно рассмотреть.
Сократительная способность сердечной мышцы снижается при ишемии сердца или инфаркте миокарда
Необходимо сказать, что наш сердечный орган имеет достаточно высокий потенциал в том плане, что может увеличивать при надобности кровообращение. Таким образом, это может происходить при обычных занятиях спортом, либо же при тяжелом физическом труде. Кстати, если говорить о потенциальных возможностях сердца, то объем кровообращения может увеличиться до 6-ти раз. Но, бывает такое, что сократимость миокарда падает по различным причинам, это уже говорит о его пониженных возможностях, которые следует вовремя диагностировать и принять необходимые меры.
Причины снижения
Для тех, кто не знает, следует сказать, что функции миокарда сердца представляют целый алгоритм работы, который не нарушается ни в коем случае. Благодаря возбуждаемости клеток, сократимости сердечных стенок и проводимости кровотока , наши кровеносные сосуды получают порцию полезных веществ, которая необходима для полноценной работоспособности. Сократительная способность миокарда считается удовлетворительной тогда, когда его активность повышается с увеличением физических нагрузок. Именно тогда можно говорить о полноценном здоровье, если же этого не происходит, следует разобраться сначала в причинах данного процесса.
Важно знать, что сниженная сократимость мышечной ткани может быть из-за следующих проблем со здоровьем:
- авитаминоз;
- миокардит;
- кардиосклероз;
- гипертиреоз;
- повышение обмена веществ;
- атеросклероз и др.
Итак, причин для снижения сократимости мышечной ткани может быть масса, но главной является одна. При длительной физической нагрузке, наш организм может не дополучать не только необходимую порцию кислорода, но и то количество полезных веществ, которое необходимо для жизнедеятельности организма, и из которых вырабатывается энергия. В таких случаях, в первую очередь используются внутренние запасы, которые всегда имеются в организме. Стоит сказать, что данных запасов надолго не хватает, и когда они исчерпываются, в организме происходит необратимый процесс, вследствие чего повреждаются кардиомиоциты (это клетки, из которых состоит миокард), а сама мышечная ткань теряет свою сократительную способность.
Помимо факта повышенных физических нагрузок, сниженная сократимость миокарда левого желудочка может возникнуть как следствие следующих осложнений:
- серьезное поражение головного мозга;
- следствие неудачного оперативного вмешательства;
- болезни, связанные с сердцем, например, ишемия;
- после инфаркта миокарда;
- следствие токсического воздействия на мышечную ткань.
Необходимо сказать, что данное осложнение может очень сильно испортить качество жизни человека. Помимо общего ухудшения здоровья человека, оно может спровоцировать сердечную недостаточность, что не является хорошим признаком. Необходимо уточнить, что сократительная способность миокарда должна быть сохранена при любых обстоятельствах. Для этого следует ограничить себя в переутомлении при длительных физических нагрузках.
Одними из самых приметных являются следующие признаки сниженной сократимости:
- быстрая утомляемость;
- общая слабость организма;
- быстрый набор веса;
- учащенное дыхание;
- отеки;
- приступы ночного удушья.
Диагностирование снижения сократительной способности
При первых же вышеуказанных признаках следует обратиться к специалисту, ни в коем случае нельзя заниматься самолечением, либо игнорировать данную проблему, так как последствия могут быть плачевными. Зачастую, чтобы определить сократимость миокарда левого желудочка которая может быть удовлетворительной, либо же сниженной, проводится обычное ЭКГ, плюс эхокардиография.
ЭхоКГ миокарда позволяет измерить объем левого желудочка сердца в систолу и диастолу
Бывает, что после проведения ЭКГ нет возможности поставить точный диагноз, тогда пациенту назначают Холтеровский мониторинг. Данный метод позволяет сделать более точное заключение, с помощью постоянного наблюдения электрокардиографа.
Помимо вышеуказанных методов, применяются следующие:
- ультразвуковое исследование (УЗИ);
- биохимический анализ крови;
- контроль артериального давления.
Способы лечения
Для того чтобы понять, каким образом проводить лечение, для начала следует провести квалифицированную диагностику, которая определит степень и форму недуга. Например, глобальная сократимость миокарда левого желудочка должна устраняться с помощью классических методов лечения. В подобных случаях специалисты рекомендуют пропить медикаменты, которые способствуют улучшению микроциркуляции крови. Плюс к данному курсу прописывают препараты, с помощью которых есть возможность улучшить обмен веществ в сердечном органе.
Назначаются лекарственные вещества регулирующие обмен веществ в сердце и улучшающие микроциркуляцию крови
Конечно же, для того чтобы терапия имело должный результат, следует избавиться от основного заболевания, которым был вызван недуг. Кроме того, если дело касается спортсменов, либо людей с повышенной физической загруженностью, то здесь для начала можно обойтись специальным режимом, который ограничивает физические нагрузки и рекомендации проведения дневного отдыха. В более тяжелых формах в течение 2-3 дней назначается постельный режим . Стоит сказать, что данное нарушение легко поддается коррекции, если вовремя провести диагностические мероприятия.
Сократимость миокарда является способностью сердечной мышцы обеспечить ритмические сокращения сердца в автоматическом режиме с целью продвижения крови по сердечно-сосудистой системе. Сама сердечная мышца имеет специфическое строение, отличающееся от остальных мышц организма.
Особенности миокарда
Миокард обладает рядом физических и физиологических свойств, позволяющих ему обеспечивать полноценное функционирование сердечно-сосудистой системы. Эти особенности сердечной мышцы, позволяют не только поддерживать кровообращение, обеспечивая непрерывное поступление крови из желудочков в просвет аорты и легочного ствола, но также и осуществлять компенсаторно-приспособительные реакции, обеспечивая адаптацию организма к повышенным нагрузкам.
Физиологические свойства миокарда обуславливаются его растяжимостью и эластичностью. Растяжимость сердечной мышцы обеспечивает ее способность к значительному увеличению собственной длины без повреждения и нарушения своей структуры.
Эластические свойства миокарда обеспечивают его способность возвращаться в исходную форму и положение после того, как заканчивается воздействие деформирующих сил (сокращение, расслабление).
Также, важную роль в поддержании адекватной сердечной деятельности играет способность сердечной мышцы к развитию силы в процессе сокращения миокарда и совершению работы во время систолы.
Что такое сократительная способность миокарда
Сократимость сердца – это одно из физиологических свойств сердечной мышцы, реализующее насосную функцию сердца за счет способности миокарда сокращаться во время систолы (приводя к изгнанию крови из желудочков в аорту и легочной ствол (ЛС)) и расслабляться в период диастолы.
Вначале осуществляется сокращение предсердных мышц, а затем сосочковых мышц и субэндокардиального слоя желудочковых мышц. Далее, сокращение распространяется на весь внутренний слой желудочковых мышц. Это обеспечивает полноценную систолу и позволяет поддерживать непрерывный выброс крови из желудочков в аорту и ЛС.
Сократительная способность миокарда поддерживается также его:
- возбудимостью, способностью генерировать потенциал действия (возбуждаться) в ответ на действие раздражителей;
- проводимостью, то есть способностью проводить сгенерированный потенциал действия.
Сократимость сердца зависит также и от автоматизма сердечной мышцы, проявляющейся самостоятельной генерацией потенциалов действия (возбуждений). Благодаря этой особенности миокарда, даже денервированное сердце некоторое время способно сокращаться.
От чего зависит сократимость сердечной мышцы
Физиологические особенности сердечной мышцы регулируются блуждающими и симпатическими нервами, которые способны влиять на миокард:
- хронотропно;
- инотропно;
- батмотропно;
- дромотропно;
- тонотропно.
Особенности сердечной мышцы
Возбудимость сердечной мышцы неодинакова во всех участках сердца. Наиболее возбудимым синусоатриальным узел. Возбудимость пучка Гиса значительно меньше. Хотя во время сокращения мышца сердца возбудима. Но в этот период, который почти совпадает с систолой, самые сильные искусственные раздражения сердца не вызывают нового сокращения вследствие «конфликта двух сильных возбуждений, слишком близко поставленных одно к другому во времени в одном и том же субстрате» (А. А. Ухтомский). Это состояние полное потери возбудимости во время сокращения сердца обозначается как абсолютная рефрактерность. После этого во время расслабления мышцы сердца при раздражении сердца ударом индукционного электрического тока, вследствие изменения интервала времени между двумя возбуждениями и изменения функционального состояния сердца, может быть получено вне очереди, но более слабое сокращение.
Этот второй период неполной возбудимости во время расслабления сердца обозначается как относительная рефрактерность. Непосредственно после периода относительной рефрактерности наблюдается кратковременное повышение возбудимости — экзальтационная фаза. Продолжительность абсолютной и относительной рефрактерности зависит от длительности- сердечного цикла. Период абсолютной рефрактерности синусоатриального узла у человека доходит до 0,3 с., предсердий — от 0,06 до 0,12 с., а желудочков — от 0,3 до 0,4 с.
Благодаря продолжительной рефрактерности сердце отвечает на продолжительное раздражение ритмическими сокращениями и в обычных условиях на может прийти в состояние тетануса.
Если на желудочек сердца холоднокровного животного нанести раздражение до прихода очередного автоматического импульса, т. е. в периоде относительной рефрактерности, то возникает преждевременное сокращение сердца — экстрасистола, за которым следует компенсаторная пауза, по продолжительности превышающая обычную.
Экстрасистолы возникают при изменениях в проводящей системе или в мышце сердца. Влияние на изменение возбудимости обозначается как батмотропное.
Сокращение сердечной мышцы не усиливается с увеличением раздражения. Если непосредственно наносить раздражение на сердечную мышцу, наращивая каждый раз величину раздражения, то обнаруживается следующий факт. Вначале при слабых раздражениях мышца па них не реагирует сокращением, затем при некотором повышении величины раздражения она сокращается. Это сокращение максимальное. Дальнейшее увеличение силы раздражения уже не увеличивает сокращения сердечной мышцы (Г. Боудич, 1871).
Однако это только частный случай, а не правило, так как высота сокращения мышцы сердца («все») изменяется и зависит, от ее возбудимости и лабильности, т. е. от ее функционального состояния. «Ничего» также не существует, так как при подпороговых раздражениях возникает возбуждение, которое суммируется при определенной частоте раздражений.
Величина наибольшего сокращения сердечной мышцы зависит от уровня обмена веществ в ней. Влияние на силу сердечных сокращений обозначается как инотропное.
В процессе филогенеза выработалась способность сердечной мышцы увеличивать силу своих сокращений в зависимости от увеличения количества притекающей к сердцу крови и повышения давления крови в артериальной системе.
Увеличение притока крови к сердцу и повышение кровяного давления в физиологических условиях вызываются мышечной работой и некоторыми эмоциями.
Как увеличивает сердце силу своих сокращений при повышенных нагрузках?
Сила сокращений сердца увеличивается благодаря увеличению начальной длины мышечных волокон (Старлинг, 1916).
Мышечные волокна имеют определенную длину при диастоле сердца во время покоя организма, перед началом сокращения сердца (начальная длина). При увеличении притока крови к сердцу и при затруднениях оттока, вызванных повышением кровяного давления, сердце в диастоле от переполнения полости кровью растягивается сильнее, следовательно, начальная длина мышечных волокон сердца увеличивается. Чем больше приток крови к сердцу или чем больше кровяное давление, затрудняющее отток крови, тем больше начальное растяжение мышечных волокон.
На изолированных мышцах установлено, что энергия сокращении скелетной и сердечной мышц прямо пропорциональна начальниц длине мышечных волокон. Чем больше начальная длина волокон, тем сильнее сокращение. Поэтому при увеличении начальной длины волокон сердца оно сильнее сокращается во время систолы и благодаря этому увеличивается количество выбрасываемой крови.
Большое значение имеет кровоснабжение и питание сердечной мышцы. Чем лучше питание мышцы, тем меньше она предварительно растягивается.
В естественных условиях при отсутствии дополнительного растяжения сердца увеличение силы сокращений — результат усиления обмена веществ в сердечном мускуле под влиянием нервной системы (трофическое влияние).
Когда сердечная мышца утомляется, то давление в сердце падает и оно растягивается. Способность сердца производить прежнюю работу при утомлении зависит от степени растяжения его мышечных волокон.
Степень растяжения сердца определяется толщиной и состоянием сердечной мышцы. Максимально сердце может расшириться до перикарда, который, таким образом, обусловливает предельное расширение сердца.
Возможно, вас заинтересует:
Нервно-мышечный препарат
Строение сердца
Сила мышц
Опорно-двигательная система человека
Кровоснабжение сердца
Как регулируется сократимость миокарда
Воздействие блуждающих нервов вызывает снижение:
- сократимости миокарда,
- ЧСС,
- генерации потенциала действия и его распространения,
- метаболических процессов в миокарде.
То есть, оказывает исключительно отрицательные инотропные, тонотропные и т.д. эффекты.
Влияние симпатических нервов проявляется повышением сократимости миокарда, увеличением ЧСС, ускорением метаболических процессов, а также повышением возбудимости и проводимости сердечной мышцы (положительные эффекты).
При сниженном АД происходит стимуляция симпатического воздействия на сердечную мышцу, усиление сократимости миокарда и увеличение ЧСС, за счет чего осуществляется компенсаторная нормализация артериального давления.
При повышении давления происходит рефлекторное снижение сократимости миокарда и ЧСС, позволяющие понизить артериальное давление до адекватного уровня.
На сократимость миокарда также оказывает влияние значительная стимуляция:
- зрительных,
- слуховых,
- тактильных,
- температурных и т.д. рецепторов.
Это обуславливает изменение частоты и силы сердечных сокращений во время физической или эмоциональной нагрузки, нахождении в жарком или холодном помещении, а также при воздействии любых значимых раздражителей.
Из гормонов, наибольшее влияние на сократимость миокарда оказывают адреналин, тироксин и альдостерон.
Роль ионов кальция и калия
Также, изменять сократимость сердца могут ионы калия и кальция. При гиперкалиемии (избытке ионов калия) происходит снижение сократимости миокарда и частоты сердечных сокращений, а также торможение образования и проведения потенциала действия (возбуждения).
Ионы кальция наоборот способствуют увеличению сократимости миокарда, частоты его сокращений, а также увеличивают возбудимость и проводимость сердечной мышцы.
Препараты, оказывающие влияние на сократимость миокарда
Значительным влиянием на сократительную способность миокарда обладают препараты сердечных гликозидов . Данная группа препаратов способна оказывать отрицательный хронотропный и положительный инотропный эффект (основной препарат группы – дигоксин в терапевтических дозах повышает сократимость миокарда). Благодаря этим свойствам, сердечные гликозиды являются одной из основных групп препаратов, используемых в лечении сердечной недостаточности.
Также, на СМ способны оказывать воздействие препараты бета-блокаторов (снижают сократимость миокарда, оказывают отрицательный хронтропный и дромотропный эффекты), блокаторы Са каналов (оказывают отрицательный инотропный эффект), ингибиторы АПФ (улучшают диастолическую функцию сердца, способствуя увеличению сердечного выброса в систолу) и т.д.
Повышение сократимости миокарда и сердечного выброса
С целью повышения сократительной способности миокарда целесообразно в первую очередь применение сердечных гликозидов. Практически эти препараты необходимо назначать всем больным с нарушением кровообращения и застойными явлениями как в малом, так и в большом круге, включая тех больных, у которых имеются нарушения ритма и проводимости и даже при повышенном сердечном выбросе. При этом эффективность гликозидов различна при разных заболеваниях и даже у отдельных больных с одним и тем же страданием. Сердечные гликозиды более результативны при пороках сердца без признаков ревматической активности, а также при атеросклеротическом поражении сердца. Обычно менее выражен эффект при миокардитах и поражениях миокарда при таких заболеваниях, как тиреотоксикоз, анемия, миокардиопатия при амилоидозе, гемохроматоз, уремия и т. д. Абсолютным противопоказанием к применению гликозидов является состояние, связанное с интоксикацией ими. При этом нередко эти симптомы могут быть неярко выражены, близкими к проявлениям самой сердечной недостаточности, и требуется внимательное наблюдение для их своевременной диагностики. Небольшое замедление атриовентрикулярной проводимости не является противопоказанием к назначению гликозидов. Однако при блокаде с проведением импульсов 2:1 и наличии периодов Венкебаха эти средства нужно использовать с осторожностью. При полной поперечной блокаде эти препараты можно вводить, если есть уверенность в том, что нарастание нарушения проводимости и возникновение блокады не были связаны с приемом гликозидов.
Показания к назначению гликозидов определяются всегда клинически при выявлении признаков недостаточности сердца даже в начальной стадии. Обычно проводят комплексное лечение, которое включает покой, мочегонные средства, диету с ограничением соли. Поэтому полноту «дигитализации» оценить бывает трудно. Величина максимальной дозы, продолжительность ее введения определяются в каждом конкретном случае индивидуально с учетом динамики клинических данных.
Эффективность гликозидов у больных с сердечной недостаточностью в течение многих лет привлекают к ним большое внимание фармакологов. Проведена большая работа по изучению механизма действия этих препаратов на сердце, а также по внедрению в практику новых эффективных веществ этого ряда и выделению в химически чистом виде активнодействующих средств. Сердечные гликозиды обнаружены в большом количестве растений. Чаще всего используются препараты, полученные из наперстянки пурпуровой (дигитоксин), наперстянки шерстистой (дигоксин, лантозид, целанид, или изоланид), горицвета (адонис, строфантин и т. д.). С химической точки зрения активные гликозиды состоят из двух главных частей: генина — структуры, близкой стероидным гормонам (в основе которой лежит циклопентанпергидрофенантрен), и присоединенного к генину пяти- или шестичленного лактонного кольца и молекулы углевода. Фармакологическое действие связано прежде всего с генином. Молекула углевода определяет в значительной степени такие свойства препарата, как способность всасываться, накапливаться в организме и проходить через биологические мембраны. Полный синтез сердечных гликозидов не производился, однако синтетические производные их были получены при соединении различных группировок со стероидным ядром (например/ ацетил-строфантин, который содержит ацетатную группу в третьей позиции).
Положительное инотропное действие с усилением сократимости миокардиальных волокон в результате непосредственного действия на них сердечных гликозидов было убедительно продемонстрировано в опытах на изолированных папиллярных мышцах кошки. При добавлении дигитоксина в раствор, в котором находились эти мышцы, их предварительно истощенная способность сокращаться под влиянием электрических импульсов быстро восстанавливалась. Это непосредственное действие гликозидов на миокард показано также на сердце человека в условиях хирургического вмешательства с применением искусственного кровообращения, когда сократимость сердца оценивалась с помощью электрокимографии или по скорости изменения давления в левом желудочке. Сердечные гликозиды ухудшают проводимость в миокарде и увеличивают время рефрактерного периода атриовентрикулярного узла. Однако индивидуальная чувствительность сердца разных людей в этом отношении сильно колеблется, вплоть до возможности замедления атриовентрикулярной проводимости при лечении терапевтическими дозами препарата. Увеличение рефрактерного периода атриовентрикулярного узла связано как с непосредственным влиянием гликозидов, так и с их ваготропным эффектом. Рефрактерный период миокарда предсердий и желудочков под влиянием сердечных гликозидов уменьшается.
Токсические дозы наперстянки вызывают аритмии и нарушения проводимости, что связано с различными эффектами, включая повышение автоматизма и снижение возбудимости и проводимости по волокнам Пуркинье. Увеличивается склонность желудочков к фибрилляции. В зависимости от преобладания того или иного токсического действия наперстянка в летальной дозе может обусловить фибрилляцию желудочков или остановку сердца.
Точный механизм действия гликозидов на сократительный миокард до настоящего времени не выяснен. С помощью современной техники показано, что сердечные гликозиды обеспечивают параллельное и пропорциональное увеличение силы сокращения мышечных волокон и поглощение ими кислорода. При этом они усиливают процесс окисления глюкозы и свободных жирных кислот в сердце.
Токсические дозы гликозидов уменьшают содержание калия в сердечной мышце. Уменьшение концентрации внутриклеточного калия обусловлено ингибицией притока калия при неизменном его оттоке. Предполагают, что уменьшение содержания внутриклеточного калия есть наиболее существенный результат действия этих препаратов, ответственный в конечном счете за их инотропный эффект. Однако не все исследователи с этим согласны. Весьма вероятной считается связь действия гликозидов с их влиянием на перемещения иона кальция в клетках миокарда, поскольку именно этот ион также оказывает положительное инотропное действие путем участия в сопряжении процессов возбуждения и сокращения. С помощью современной техники пока не удалось надежно установить характер перемещений иона кальция в мио-кардиальных клетках и изменения его содержания в саркоплазматическом ретикулуме и митохондриях под влиянием наперстянки. Изучалось влияние наперстянки на аденозинтрифосфатазу. Некоторые авторы отметили, что гликозиды снижают активность аденозинтрифосфатазы, зависимой от калия и натрия. Так как ионный насос требует энергии аденозинтрифосфата, ингибиция аденозинтрифосфатазы может изменить внутриклеточное содержание ионов. Следует отметить, что этот эффект гликозидов был показан на многих типах клеток, причем обычно гликозиды добавлялись в токсической концентрации. В других исследованиях установлено, что нетоксические концентрации гликозидов приводят к стимуляции аденозинтрифосфатазы. Это позволяет предполагать, что именно указанный фермент является «рецептором» гликозидов, через который они осуществляют свое инотропное действие.
Некоторые метаболические эффекты гликозидов близки к действию катехоламинов. В связи с этим обсуждается предположение о том, что гликозиды повышают сократимость миокарда в результате высвобождения катехоламинов, но оно не было убедительно подтверждено. Не имеется также определенных доказательств, что гликозиды прямо влияют на белки миокарда. Таким образом, механизм инотропного действия гликозидов требует дальнейшего изучения.
Сердечные гликозиды оказывают и экстракардиальное действие. Они обусловливают, в частности, брадикардию, которая связана с их ваготропным эффектом. Этим же частично объясняется склонность к нарушениям атриовентрикулярной проводимости.
Прямое введение сердечных гликозидов в перфузируемую артерию приводит к ее спазму, правда, относительно кратковременному по сравнению с более длительным инотропным эффектом. В эксперименте на собаках отмечалась склонность к спазму коронарных артерий под влиянием гликозидов. Однако клиническое значение этих наблюдений сомнительно. Учащения приступов стенокардии под влиянием гликозидов не наблюдают. У здоровых лиц отмечают веноконстрикцию, а при сердечной недостаточности — парадоксальную дилатацию вен. Под влиянием непосредственного раздражающего действия гликозидов на слизистую оболочку желудочно-кишечного тракта, а также на центральную нервную систему часто отмечают анорексию, тошноту, рвоту, диарею. При введении строфантина в почечную артерию собаки выделение натрия и воды увеличивается, что указывает на непосредственное влияние препарата на канальцы. Его связывают с ингибицией аденозинтрифосфатазы, но считается маловероятным аналогичное объяснение диуретического эффекта гликозидов у больных с сердечной недостаточностью, так как у здоровых при введении строфантина мочегонный эффект отсутствует.
Влияние гликозидов на сердце и кровообращение у здоровых лиц и у больных с сердечной недостаточностью несколько отличается. У больных наблюдается увеличение сердечного выброса с улучшением опорожнения сердца и уменьшением давления в предсердиях, венах и легочной артерии. При этом улучшается почечный кровоток, повышается клубочковая фильтрация и, видимо, снижается секреция альдостерона. Все это ведет к усиленному натрийурезу с уменьшением объема циркулирующей крови и вслед за этим размеров сердца. У лиц со здоровым сердцем при введении гликозидов сердечный выброс не изменяется или даже уменьшается. Однако в данном случае этот показатель отражает не только сократимость миокарда, но и ряд других изменений в кровообращении. Показано, что сократимость миокарда при этом возрастает, хотя одновременно возникает резкое снижение давления в левом предсердии вследствие уменьшения венозного притока. Эти эффекты практически нивелируются у больных, у которых решающим фактором является улучшение функции сердца. Влияние гликозидов на размеры сердца как у здоровых, так и у больных лиц также обычно зависит от непосредственного их влияния не только на миокард, но и на вегетативную нервную систему и сосуды. Имея в виду воздействие (в том числе опосредованное) на электрическую активность сердца, следует указать на возможность возникновения практически любых нарушений проводимости и эктопических аритмий под влиянием гликозидов.
Препараты гликозидов отличаются друг от друга по всасываемости, быстроте наступления эффекта и его продолжительности. Всасывание при приеме препарата внутрь колеблется от 10—20% у лантозида до 60—70% у дигоксина и до 100% у дигитоксина. Скорость наступления эффекта варьирует от 5—10 мин при внутривенном введении строфантина до 1 ч при приеме дигитоксина. Метаболизм и экскреция гликозидов изучались с помощью препаратов, меченных радиоактивными изотопами. Период полувыведения дигоксина составляет 1,5 сут, при этом он выделяется неизмененным с мочой, и поэтому поддерживающая доза должна быть снижена при хронической почечной недостаточности (при резком снижении функции почек до Уз средней дозы для больных с нормальной функцией почек).
Показания к назначению, величина поддерживающей дозы и необходимость отмены сердечных гликозидов в связи с интоксикацией определяются, как правило, с учётом комплексной оценки клинических проявлений и предшествующего лечения (прием препаратов, способствующих выведению калия). На ЭКГ в связи с дигитализацией обычно появляются изменения, прежде всего со стороны конечной части желудочкового комплекса ST — T, но они чаще не коррелируют ни с достигаемым оптимальным эффектом, ни с токсическими явлениями, которые позже могут возникнуть в виде нарушений предсердно-желудочковой проводимости.
Лечение гликозидами сердечной недостаточности чаще всего проводится длительно с применением поддерживающих доз. Однако как раз при многих заболеваниях миокарда дигитализация может быть ограничена периодом обострения основного заболевания, которое иногда купируется сочетанным применением ряда средств устраняющих основную причину сердечной недостаточности (как, например, при тиреотоксикозе, ревмокардите ит. д.).
- Препараты сердечных гликозидов
- Интоксикация сердечными гликозидами
Чем опасно нарушение сократимости
Сниженная сократимость миокарда сопровождается уменьшением сердечного выброса и нарушением кровоснабжения органов и тканей. Вследствие этого, развивается ишемия, возникают метаболические нарушения в тканях, нарушается гемодинамика и увеличивается риск тромбообразования, развивается сердечная недостаточность.
Когда может нарушаться СМ
Снижение СМ может отмечаться на фоне:
- гипоксии миокарда ;
- ишемической болезни сердца ;
- выраженного атеросклероза коронарных сосудов;
- инфаркта миокарда и постинфарктного кардиосклероза;
- аневризмы сердца (наблюдается резкое снижение сократимости миокарда левого желудочка);
- острых миокардитов, перикардитов и эндокардитов;
- кардиомиопатий (максимальное нарушение СМ наблюдается при истощении адаптационных возможностей сердца и декомпенсации кардиомиопатии);
- травм голоного мозга;
- аутоиммунных заболеваний;
- инсультов;
- интоксикаций и отравлений;
- шоков (при токсическом, инфекционном, болевом, кардиогенном и т.д.);
- авитаминозов;
- нарушения баланса электролитов;
- кровопотери;
- тяжелых инфекций;
- интоксикаций при активном росте злокачественных новообразований;
- анемий различного генеза;
- эндокринных заболеваний.
Нарушение сократимости миокарда – диагностика
Наиболее информативными методами исследования СМ являются:
- стандартная электрокардиограмма;
- ЭКГ с нагрузочными пробами;
- холтеровское мониторирование;
- ЭХО-К.
Также, для выявления причины снижения СМ выполняется общий и биохимический анализ крови, коагулограмма, липидограмма, оценивается гормональный профиль, проводится УЗИ почек, надпочечников, щитовидной железы и т.д.
СМ на ЭХО-КГ
Наиболее важным и информативным исследованием является ультразвуковое исследование сердца (оценивание объема желудочков во время систолы и диастолы, толщины миокарда, вычисления минутного объема крови и эффективного сердечного выброса, оценка амплитуды межжелудочковой перегородки и т.д.).
Лечение нарушений СМ
Все лечение должно подбираться врачом кардиологом, в соответствии с причиной нарушения СМ.
Для улучшения метаболических процессов в миокарде могут применяться препараты:
- рибоксина,
- милдроната,
- L-карнитина,
- фосфокреатина,
- витамины группы В,
- витамины А и Е.
Также могут использоваться препараты калия и магния (Аспаркам, Панангин).
Пациентам с анемиями показаны препараты железа, фолиевой кислоты, витамина В12 (в зависимости от типа анемии).
При выявлении нарушений липидного баланса может назначаться гиполипидемическая терапия. Для профилактики тромбообразования, по показаниям назначаются антиагреганты и антикоагулянты.
Также, могут использоваться препараты, улучшающие реологические свойства крови (пентоксифиллин).
Больным с сердечной недостаточностью могут быть назначены сердечные гликозиды, бета-блокаторы, ингибиторы АПФ, мочегонные средства, препараты нитратов и т.д.
Поперечная блокада сердца
Поперечная блокада сердца представляет собой нарушение распространения волны возбуждения, идущей от синоаурикулярной области, на уровне атриовентрикулярного узла.
Поперечная блокада может возникать в результате ишемического поражения области локализации атриовентрикулярного узла, при инфекциях, интоксикации, миокардите, ревматическом поражении, тиреотоксикозе, применении некоторых лекарственных препаратов (сердечных гликозидов, бета-блокаторов и др.),
В зависимости от глубины нарушения проводимости атриовентрикулярного узла различают четыре степени поперечной блокады сердца.
Блокада I степени (простое удлинение интервала PQ)
Это самая легкая степень нарушения проводимости, которая характеризуется лишь некоторым замедлением проведения импульса через атриовентрикулярную область. При этом к желудочкам проводится каждый импульс, генерируемый синусным узлом. Ритм остается правильным. На ЭКГ поперечная блокада I степени проявляется в виде удлинения интервала PQ более 0,21 с.
Блокада II степени (периодическое выпадение желудочкового комплекса)
Данный вид поперечной блокады заключается в прогрессирующем (в течение нескольких сердечных циклов) снижении проводимости атриовентрикулярного узла, которое в конечном итоге заканчивается временной полной потерей его способности к проведению импульса. В результате происходит выпадение одного желудочкового сокращения.
Далее наблюдается восстановление свойств атриовентрикулярного узла, и подобный цикл повторяется вновь и вновь. На ЭКГ поперечная блокада II степени может проявляться в двух видах: Мобитц-I и Мобитц-И. Мобитц-I характеризуется прогрессирующим увеличением интервала PQ, которое по достижении определенного критического предела заканчивается выпадением желудочкового комплекса (периоды Венкебаха—-Самойлова).
Мобитц-II отличается периодическим выпадением желудочкового комплекса без предшествующего нарастания длительности интервала PQ.
Блокада III степени (неполная поперечная блокада сердца)
В данном случае через атриовентрикулярный узел проводятся не все импульсы, приходящие от синусного узла, а лишь каждый второй или каждый третий и т.д. Соответственно, при этом соотношение сокращений предсердий и желудочков составляет 2:1,3:1 и т. д.
Когда проведение импульса блокируется над атриовентрикулярной областью, функцию водителя ритма может взять на себя верхняя часть атриовентрикулярного узла. При этом частота сокращений желудочков становится не намного меньшей, чем в норме, и сердечная гемодинамика нарушается не очень глубоко. Субъективно это выражается в неприятных ощущениях перебоев в работе сердца.
Блокада IV степени (полная поперечная блокада сердца)
Данный вид нарушения атриовентрикулярной проводимости является самым тяжелым и характеризуется тем, что от предсердий к желудочкам не проходит ни один импульс. При этом сам атриовентрикулярный узел, как правило, импульсы не генерирует (по этой причине эту форму патологии мы также рассматривали в подразделе, посвященном патологии автоматизма сердца).
В такой ситуации нарушается согласованная работа предсердий и желудочков: предсердия сокращаются в синусном ритме, а желудочки — в идиовентрикулярном, поскольку водителем ритма для них становится пучок Гиса. Причем частота сокращений желудочков снижается до 30-40 в минуту. Стойкая полная поперечная блокада сердца требует имплантации искусственного водителя ритма.
Нередко поперечная блокада сердца осложняется развитием очень серьезного патологического состояния — синдрома Морганьи—Эдемса— Стокса, возникающего при переходе неполной поперечной блокады в полную и наоборот.
В этот момент наступает так называемая преавтоматическая пауза, характеризующаяся полной остановкой сердца, которая может продолжаться от нескольких секунд до нескольких минут и проявляется в зависимости от длительности от обморока до клинической смерти. Данный синдром может возникать до нескольких раз в сутки.
Прогноз
При своевременном выявлении нарушения СМ и дальнейшем лечении, прогноз благоприятный. В случае развития сердечной недостаточности, прогноз зависит от ее тяжести и наличия сопутствующих заболеваний, утяжеляющих состояние больного (постинфарктный кардиосклероз, аневризма сердца, тяжелые сердечные блокады, сахарный диабет и т.д.).
Все материалы публикуются под авторством, либо редакцией профессиональных медиков ( об авторах ), но не являются предписанием к лечению. Обращайтесь к специалистам!
При использовании материалов ссылка или указание названия источника обязательны.
Автор: Сазыкина Оксана Юрьевна, кардиолог
Сердечная мышца является самой выносливой в человеческом организме. Высокая работоспособность миокарда обусловлена рядом свойств клеток миокарда – кардиомиоцитов. К таким свойствам относятся автоматизм (способность самостоятельно генерировать электричество), проводимость (способность передавать электрические импульсы близлежащим мышечным волокнам в сердце) и сократимость – способность синхронно сокращаться в ответ на электрическое возбуждение.
В более глобальном понятии сократимостью называют способность сердечной мышцы в целом сокращаться с целью проталкивания крови в крупные магистральные артерии – в аорту и в легочной ствол. Обычно говорят о сократимости миокарда левого желудочка, так как именно он осуществляется самую большую работу по выталкиванию крови, и эта работа оценивается по фракции выброса и ударному объему, то есть по тому количеству крови, который выбрасывается в аорту с каждым сердечным циклом.
Сердечный цикл
Общая характеристика строения и работы сердца
Анимированное изображение сердечного цикла
Сердечный цикл кратко
Сердце сокращается ритмично и циклично. Один цикл длится 0,8-0,85 секунды, это составляет примерно 72-75 сокращений (ударов) в минуту.
Основные фазы:
- Систола – сокращение мышечного слоя (миокарда) и выброс крови из сердечных полостей. Сначала сокращаются ушки сердца, затем предсердия и после них желудочки. Сокращение пробегает по сердцу волной от ушек к желудочкам. Сокращение сердечной мышцы запускается её возбуждением, а возбуждение начинается от синоатриального узла в верхней части предсердий.
- Диастола – расслабление сердечной мышцы (миокарда). При этом происходит усиление собственного кровоснабжения миокарда и обменных процессов в нём. Во время диастолы происходит наполнение полостей сердца кровью: одновременно как предсердий, так и желудочков. Важно отметить, что кровь заполняет одновременно и предсердия, и желудочки, т.к. клапаны между предсердиями и желудочками (атриовентрикулярные) в диастолу открыты.
Полный сердечный цикл
С точки зрения движения возбуждения по сердечной мышце цикл следует начинать с возбуждения и сокращения предсердий, т.к. именно на них идёт возбуждение от главного водителя ритма сердца — сино-атриального узла.
Водитель ритма
Водитель сердечного ритма — это особый участок сердечной мышцы, который самостоятельно порождает электрохимические импульсы, возбуждающие сердечную мышцу и приводящие к её сокращению.
У человека ведущим водителем ритма является синусно-предсердный (сино-атриальный) узел. Это участок сердечной ткани, содержащий «пейсмейкерные» клетки, т.е. клетки, способные к самопроизвольному возбуждению. Он находится на своде правого предсердия у места впадения в него верхней полой вены. Узел состоит из небольшого числа сердечных мышечных волокон, иннервированных окончаниями нейронов из вегетативной нервной системы. Важно понять, что вегетативная иннервация не создаёт самостоятельного ритма импульсации сердца, а лишь регулирует (изменяет) ритм, который задают сами пейсмейкерные сердечные клетки. В сино-атриальном узле зарождается каждая волна возбуждения сердца, которая приводит к сокращению сердечной мышцы и служит стимулом для возникновения следующей волны.
Фазы сердечного цикла
Итак, спровоцированная волной возбуждения волна сокращения сердца начинается с предсердий.
1. Систола (сокращение) предсердий (вместе с ушками) – 0,1 с. Предсердия сокращаются и проталкивают уже находящуюся в них кровь в желудочки. В желудочках тоже уже имеется кровь, которая залилась в них из вен во время диастолы, пройдя через предсердия и открытые атриовентрикулярные клапаны. За счет своего сокращения предсердия доливают в желудочки дополнительные порции крови.
2. Диастола (расслабление) предсердий – это расслабление предсердий после сокращения, оно длится 0,7 секунды. Таким образом, время отдыха у предсердий намного превышает время их работы, и это важно знать. Из желудочков кровь не может вернуться обратно в предсердия благодаря особым атриовентрикулярным клапанам между предсердиями и желудочками (трёхстворчатый справа и двухстворчатый, или митральный, слева). Таким образом, в диастолу у предсердий стенки расслаблены, но кровь в них из желудочков не идёт. В этом период сердце имеет 2 пустые и 2 наполненные камеры. В предсердия начинает поступать кровь из вен. Сначала кровь медленное наполняет расслабленные предсердия. Затем, после сокращения желудочков и наступившего у них расслаблением она своим давление открывает клапаны и поступает в желудочки. Диастола предсердий при этом ещё не закончилась.
И вот, наконец, в сино-атриальном узле рождается новая волна возбуждения и под её влиянием предсердия переходят к систоле и проталкивают скопившуюся в них кровь в желудочки.
3. Систола желудочков – 0,3 с. Волна возбуждения идёт от предсердий, а также по межжелудочковой перегородке, и достигает миокарда желудочков. Желудочки сокращаются. Кровь под давлением выбрасывается из желудочков в артерии. Из левого — в аорту, чтобы бежать по большому кругу кровообращения, а из правого — в легочный ствол, чтобы бежать по малому кругу кровообращения. Максимальное усилие и максимальное давление крови обеспечивает левый желудочек. Он обладает наиболее мощным миокардом из всех камер сердца.
4. Диастола желудочков — 0,5 с. Обратите внимание, что опять отдых длится дольше, чем работа (0,5 с против 0,3). Желудочки расслабились, закрыты полулунные клапаны на их границе в артериями, они не дают крови вернуться в желудочки. Атриовентрикулярные (предсердно-желудочковые) клапаны в это время открыты. Начинается заполнение кровью желудочков, которая поступает в них из предсердий, но пока без сокращения предсердий. Все 4 камеры сердца, т.е. желудочки и предсердия, расслаблены.
5. Общая диастола сердца – 0,4 с . Стенки предсердий и желудочков расслаблены. Желудочки наполняются кровью, притекающей в них через предсердия из полых вен , на 2/3, а предсердия — полностью.
6. Новый цикл. Начинается следующий цикл – систола предсердий.
Видео: Перекачка крови в сердце
Для закрепления этих сведений посмотрите на анимированную схему сердечного цикла:
Анимированная схема сердечного цикла — очень советую кликнуть и рассмотреть подробности!
Подробности работы желудочков сердца
1. Систола.
2. Изгнание.
3. Диастола
Систола желудочков
1. Период систолы, т.е. сокращения, состоит из двух фаз:
1) Фаза асинхронного сокращения – 0,04 с. Происходит неравномерное сокращение стенки желудочков. Одновременно с этим происходит сокращение межжелудочковой перегородки. За счёт этого в желудочках нарастает давление, и в результате закрывается атриовентрикулярный клапан. В результате желудочки изолируются от предсердий.
2) Фаза изометрического сокращения . Это означает, что длина мышц не меняется, хотя их напряжение возрастает. Объем желудочков тоже не меняется. Все клапаны закрыты, стенки желудочков сокращаются и стремятся сжаться. В итоге стенки желудочков напрягаются, но кровь не движется. Но при этом возрастает давление крови внутри желудочков, оно открывает полулунные клапаны артерий и для крови появляется выход.
2. Период изгнание крови – 0.25 с.
1) Фаза быстрого изгнания – 0,12 с.
2) Фаза медленного изгнания – 0,13 с.
Изгнание (выброс) крови из сердца
Кровь под давлением выдавливается из левого желудочка в аорту. Давление в аорте резко возрастает, и она расширяется, принимая большую порцию крови. Однако за счет упругости своей стенки аорта тут же опять сжимается и прогоняет кровь по артериям. Расширение и сжатие аорты порождает поперечную волну, которая распространяется с определенной скоростью по сосудам. Это волна расширения и сжатия стенки сосудов – пульсовая волна. Её скорость не совпадает со скоростью движения крови.
Пульс — это поперечная волна расширения и сжания стенки артерии, порождённая расширением и сжатием аорты при выбросе в неё крови из левого желудочка сердца.
Диастола желудочков
Протодиастолический период – 0,04 с. От окончания систолы желудочков до закрытия полулунных клапанов. В этот период часть крови возвращается обратно в желудочек из артерий под давление крови в кругах кровообращения.
Фаза изометрического расслабления – 0,25 с. Все клапаны закрыты, мышечные волокна сокращены, они еще не растянулись. Но напряжение их уменьшается. Давление в предсердиях становится выше, чем в желудочках, и это давление крови открывает атриовентрикулярные клапаны для пропускания крови из предсердий в желудочки.
Фаза наполнения. Идёт общая диастола сердца, в которую происходит наполнение кровью всех его камер, причём сначала быстро, а потом медленно. Кровь проходит транзитом через предсердия и заполняет желудочки. Желудочки заполняются кровью на 2/3 объема. В этот момент сердце функционально 2-х камерное, т.к. разделены только его левая и правая половины. Анатомически же все 4 камеры сохранены.
Пресистола . Желудочки кончательно заполняются кровью в результате систолы предсердий. Желудочки всё ещё расслаблены, в то время как предсердия уже сокращены.
Биоэлектрические основы сократимости миокарда
цикл сокращения сердца
Сократительная способность всего миокарда зависит от биохимических особенностей в каждом отдельном мышечном волокне. Кардиомиоцит, как и любая клетка, имеет мембрану и внутренние структуры, в основном состоящие из сократительных белков. Эти белки (актин и миозин) могут сокращаться, но только в том случае, если через мембрану в клетку поступают ионы кальция. Далее следует каскад биохимических реакций, и в результате белковые молекулы в клетке сокращаются, словно пружинки, вызывая сокращение и самого кардиомиоцита. В свою очередь, поступление кальция в клетку через специальные ионные каналы возможно только в случае процессов реполяризации и деполяризации, то есть ионных токов натрия и калия через мембрану.
При каждом поступившем электрическом импульсе мембрана кардиомиоцита возбуждается, и активизируется ток ионов в клетку и из нее. Такие биоэлектрические процессы в миокарде возникают не одномоментно во всех отделах сердца, а поочередно – сначала возбуждаются и сокращаются предсердия, затем сами желудочки и межжелудочковая перегородка. Итогом всех процессов является синхронное, регулярное сокращение сердца с выбрасыванием определенного объема крови в аорту и далее по всему организму. Таким образом, миокард выполняет свою сократительную функцию.
Видео: подробнее о биохимии сократимости миокарда
Как сокращается сердце?
Сократимость — одно из свойств миокарда, заключающееся в создании ритмических движений предсердий и желудочков, позволяющих прокачивать кровь в сосуды. Камеры сердца постоянно проходят через 2 фазы:
- Систола — вызывается соединением актина и миозина под воздействием энергии АТФ и выхода ионов калия из клеток, при этом тонкие волокна скользят по толстым и пучки уменьшаются в длине. Доказана возможность волнообразных движений.
- Диастола — происходит расслабление и разъединение актина и миозина, восстановление затраченной энергии за счет синтеза из полученных по «мостикам» ферментов, гормонов, витаминов.
Установлено, что силу сокращений обеспечивает входящий внутрь миоцитов кальций.
Весь цикл сокращения сердца, включая систолу, диастолу и общую паузу за ними, при нормальном ритме укладывается в 0,8 сек. Начинается с систолы предсердий, происходит наполнение кровью желудочков. Затем предсердия «отдыхают», переходя в фазу диастолы, а желудочки сокращаются (систола). Подсчет времени «работы» и «отдыха» сердечной мышцы показал, что за сутки на состояние сокращения приходится 9 час 24 мин, а на расслабление — 14 час 36 мин.
Последовательность сокращений, обеспечение физиологических особенностей и потребностей организма при нагрузке, волнениях зависит от связи миокарда с нервной и эндокринной системами, способности принимать и «расшифровывать» сигналы, активно приспосабливаться к жизненным условиям человека.
Распространение возбуждения от синусового узла можно проследить по интервалам и зубцам ЭКГ
Зачем нужно знать о сократимости миокарда?
Сердечная сократимость – это важнейшая способность, которая свидетельствует о здоровье самого сердца и всего организма в целом. В том случае, когда у человека сократимость миокарда в пределах нормы, беспокоиться ему не о чем, так как при полном отсутствии кардиологических жалоб можно с уверенностью заявить о том, что на данный момент с его сердечно-сосудистой системой все в порядке.
Если же врач заподозрил и с помощью обследования подтвердил, что у пациента нарушена или снижена сократимость миокарда, ему необходимо как можно скорее дообследоваться и начать лечение, если у него выявлено серьезное заболевание миокарда. О том, какие заболевания могут стать причиной нарушения сократимости миокарда, будет изложено ниже.
Что такое нормокинез сократимости миокарда
Допамин увеличивает сократимость миокарда и уменьшает общее легочное и общее периферическое сосудистое сопротивление. Инотропные препараты увеличивают потребление кислорода миокардом, что в свою очередь требует увеличения коронарного кровотока.
Цель исследования — изучение сократительной функции миокарда левого и правого желудочков радиовентрикулографическими методами.
ФВ ЛЖ у пациентов, стоящих в листе ожидания на трансплантацию сердца, значительно снижена (Ј 40% у 78% и Ј 20% у 18% больных). 13. Капелько В.И. Значение оценки диастолы желудочков в диагностике заболеваний сердца.
Сократимость миокарда по ЭКГ
Сократительная способность сердечной мышцы может быть оценена уже при проведении электрокардиограммы (ЭКГ), так как этот метод исследования позволяет зарегистрировать электрическую активность миокарда. При нормальной сократимости сердечный ритм на кардиограмме является синусовым и регулярным, а комплексы, отражающие сокращения предсердий и желудочков (PQRST), имеют правильный вид, без изменений отдельных зубцов. Также оценивается характер комплексов PQRST в разных отведениях (стандартных или грудных), и при изменениях в разных отведениях можно судить о нарушении сократимости соответствующих отделов левого желудочка (нижняя стенка, высоко-боковые отделы, передняя, перегородочная, верхушечно-боковая стенки ЛЖ). В связи с высокой информативностью и простотой в проведении ЭКГ является рутинным методом исследования, позволяющим своевременно определить те или иные нарушения в сократимости сердечной мышцы.
Продольная блокада сердца
Под продольной блокадой сердца понимается нарушение проведения импульса на уровне левой или правой ножки пучка Гиса. Чаще всего причиной развития данного вида патологии служит очаговая ишемия соответствующей области миокарда межжелудочковой перегородки.
В зависимости от глубины повреждения проводящей системы сердца продольная блокада может сопровождаться различными расстройствами сердечной деятельности вплоть до выраженной диссоциации в деятельности желудочков, заключающейся в их асинхронном сокращении.
При полной блокаде правой ножки пучка Гиса возбуждение на правый желудочек распространяется с левого. На ЭКГ в правых грудных отведениях отмечается высокий и широкий зубец R.
При полной блокаде левой ножки пучка Гиса возбуждение левого желудочка возникает при его распространении с правого. В этом случае на ЭКГ в правых грудных отведениях зубец R будет иметь маленькую амплитуду, зубец S широкий и глубокий; в левых грудных отведениях зубец R широкий и зазубренный (имеет М-образную форму).
Сократимость сердца в норме и нарушения сократимости миокарда
О том, сохранена ли у пациента сократимость сердечной мышцы или нет, можно достоверно судить только после проведения УЗИ сердца. Так, на основании расчета суммарного индекса подвижности стенок, а также определения толщины стенки ЛЖ во время систолы, можно выявить нормальный тип сократимости или отклонения от нормы. Нормой считается утолщение исследуемых сегментов миокарда более 40%. Увеличение толщины миокарда на 10-30% свидетельствует о гипокинезии, а утолщение менее, чем на 10% от исходной толщины – о тяжелой гипокинезии.
Исходя из этого, можно выделить следующие понятия:
- Нормальный тип сократимости – все сегменты ЛЖ сокращаются в полную силу, регулярно и синхронно, сократительная способность миокарда сохранена,
- Гипокинезия – снижение локальной сократимости ЛЖ,
- Акинезия – полное отсутствие сокращения данного сегмента ЛЖ,
- Дискинезия – сокращение миокарда в исследуемом сегменте неправильное,
- Аневризма – “выпячивание” стенки ЛЖ, состоит из рубцовой ткани, полностью отсутствует способность к сокращениям.
Кроме данной классификации, выделяют нарушения глобальной или локальной сократимости. В первом случае миокард всех отделов сердца не в состоянии сократиться с такой силой, чтобы осуществить полноценный сердечный выброс. Во случае нарушения локальной сократимости миокарда снижается активность тех сегментов, которые непосредственно подвержены патологическим процессам и в которых визуализируются признаки дис-, гипо- или акинезии.
При каких заболеваниях встречаются нарушения сократимости миокарда?
графики изменения сократительной способности миокарда в различных ситуациях
Нарушения глобальной или локальной сократимости миокарда могут быть обусловлены заболеваниями, для которых характерно наличие воспалительных или некротических процессов в сердечной мышце, а также формирование рубцовой ткани вместо нормальных мышечных волокон. К категории патологических процессов, которые провоцируют нарушение локальной сократимости миокарда, относятся следующие:
- Гипоксия миокарда при ишемической болезни сердца,
- Некроз (гибель) кардиомиоцитов при остром инфаркте миокарда,
- Формирование рубца при постинфарктном кардиосклерозе и аневризме ЛЖ,
- Острый миокардит – воспаление сердечной мышцы, вызванное инфекционными агентами (бактерии, вирусы, грибки) или аутоиммунными процессами (системная красная волчанка, ревматоидный артрит и др),
- Постмиокардитический кардиосклероз,
- Дилатационный, гипертрофический и рестриктивный типы кардиомиопатии.
Кроме патологии непосредственно сердечной мышцы, к нарушению глобальной сократимости миокарда могут привести патологические процессы в полости перикарда (в наружной сердечной оболочке, или в сердечной сумке), которые мешают миокарду полноценно сокращаться и расслабляться – перикардит, тампонада сердца.
При остром инсульте, при травмах головного мозга также возможно кратковременное снижение сократительной способности кардиомиоцитов.
Из более безобидных причин снижения сократительной способности миокарда можно отметить авитаминоз, миокардиодистрофию (при общем истощении организма, при дистрофии, анемии), а также острые инфекционные заболевания.
Возможны ли клинические проявления нарушенной сократимости?
Изменения в сократимости миокарда не бывают изолированными, и, как правило, сопровождаются той или иной патологией миокарда. Поэтому из клинических симптомов у пациента отмечаются те, которые характерны для конкретной патологии. Так, при остром инфаркте миокарда отмечаются интенсивные боли в области сердца, при миокардите и кардиосклерозе – одышка, а при нарастающей систолической дисфункции ЛЖ – отеки. Часто встречаются нарушения сердечного ритма (чаще мерцательная аритмия и желудочковая экстрасистолия), а также синкопальные (обморочные) состояния, обусловленные низким сердечным выбросом, и, как следствие, малым притоком крови к головному мозгу.
Как относиться к гипертрофии?
Обычно длительная повышенная нагрузка вызывает гипертрофию. Толщина стенки левого желудочка увеличивается более чем на 15 мм. В механизме образования важным моментом является отставание прорастания капилляров вглубь мышцы. В здоровом сердце количество капилляров на мм2 сердечной мышечной ткани составляет около 4000, а при гипертрофии показатель снижается до 2400.
Поэтому состояние до определенного момента считается компенсаторным, но при значительном утолщении стенки ведет к патологии. Обычно развивается в том отделе сердца, который должен усиленно работать, чтобы протолкнуть кровь сквозь суженное отверстие либо преодолеть препятствие сосудов.
Гипертрофированная мышца способна длительное время поддерживать кровоток при пороках сердца.
Мышца правого желудочка развита слабее, она работает против давления 15–25 мм рт. ст. Поэтому компенсация при митральном стенозе, легочном сердце удерживается недолго. Но правожелудочковая гипертрофия имеет большое значение при остром инфаркте миокарда, сердечной аневризме в зоне левого желудочка, снимает перегрузку. Доказаны значительные возможности именно правых отделов в тренировке при занятиях физическими упражнениями.
Утолщение левого желудочка компенсирует пороки аортальных клапанов, митральную недостаточность
Нужно ли лечить нарушения сократительной способности?
Лечение нарушенной сократимости сердечной мышцы является обязательным. Однако, при диагностике подобного состояния необходимо установить причину, приведшую к нарушению сократимости, и лечить это заболевание. На фоне своевременного, адекватного лечения причинного заболевания сократимость миокарда возвращается к нормальным показателям. Например, при лечении острого инфаркта миокарда зоны, подверженные акинезии или гипокинезии, начинают нормально выполнять свою сократительную функцию спустя 4-6 недель от момента развития инфаркта.
Как лечат сниженную сократительную способность
Наиболее точно оценить контрактильность миокарда можно при выполнении вентрикулографии с одновременной регистрацией внутрижелудочкового давления. Множество предложенных для клинической практики формул и коэффициентов лишь косвенно отражает контрактильность миокарда.
Дальнейшее улучшение насосной функции миокарда может быть достигнуто использованием нескольких препаратов, улучшающих сократительную функцию (например, допамина).
Идеальное инотропное средство, по-видимому, должно увеличивать сократимость миокарда, но при этом не действовать на частоту сердечных сокращений. К сожалению, в настоящее время такого средства нет. Однако, уже сейчас врач имеет несколько препаратов, каждый из которых повышает инотропные свойства миокарда.
Возможны ли последствия?
Если говорить о том, каковы последствия данного состояния, то следует знать, что возможные осложнения обусловлены основным заболеванием. Они могут быть представлены внезапной сердечной смертью, отеком легких, кардиогенным шоком при инфаркте, острой сердечной недостаточностью при миокардите и т. д. Относительно прогноза нарушения локальной сократимости необходимо отметить, что зоны акинезии в участке некроза ухудшают прогноз при острой кардиологической патологии и увеличивают риск внезапной сердечной смерти в дальнейшем. Своевременное лечение причинного заболевания значительно улучшает прогноз, а выживаемость пациентов повышается.