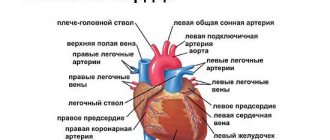
5 / 5 ( 1 голос )
Проводящая система сердца отвечает за его главную функцию — сокращения. Она представлена несколькими узлами и проводящими волокнами. Правильное функционирование этой системы обеспечивает нормальный сердечный ритм.
Если же возникают какие-то нарушения, развиваются разного рода аритмии. В статье представлена система проведения импульсов по сердцу. Описано значение проводящей системы, её состояние в норме и при патологии.
Проводящая система представляет собой сложный комплекс кардиомиоцитов
Открытие
В жаркий летний день в 1906 году Мартин Флэк, студент-медик, изучал микроскопические срезы сердца крота, тогда как его наставник Артур Кейт и его жена катались на велосипеде по красивым вишневым садам возле своего коттеджа в Кенте, Англия. По возвращении Флэк взволнованно показала Кейту “чудесную структуру, которую он обнаружил в ушке правого предсердия крота, именно там, где в эту камеру входит верхняя полая вена”. Кейт быстро понял, что эта структура очень напоминает атриовентрикулярный узел, описанный Сунао Таварой в начале этого года. Дальнейшие анатомические исследования подтвердили ту же структуру в сердцах других млекопитающих, которую они назвали “синусоидальным узлом” (sino‐auricular node). Наконец, был обнаружен долгожданный генератор сердечного ритма.
Начиная с 1909 года, используя гальванометр с двумя струнами, Томас Льюис одновременно записывал данные с двух участков с поверхности сердца собаки, делая точные сравнения прихода волны возбуждения в разные точки. Льюис идентифицировал синусоидальный узел как кардиостимулятор сердца двумя инновационными подходами.
- Во-первых, он стимулировал вышестоящую полую вену (SVC), коронарный синус и левое ушко и показал, что только кривые вблизи синусового узла были идентичны нормальному ритму.
- Во-вторых, было известно, что точка, в которой начинается сжатие, становится электрически отрицательной относительно неактивных точек мышц. В результате электрод возле САУ неизменно имел первичную отрицательность, указывающую: “Узловая область SA — это то место, в котором зарождается волна возбуждения”.
Охлаждение и нагревание синусового узла для изучения реакции сердечного ритма осуществлял G Ganter и другие, которые также указывали на местоположение и первичную функцию синусоидального узла. Когда Эйнтховен был удостоен Нобелевской премии в 1924 году, он щедро упомянул Томаса Льюиса, говоря: “Я сомневаюсь, что без его ценного вклада у меня была бы привилегия стоять перед вами сегодня». [2 — Silverman, M.E.; Hollman, A. (1 October 2007). «Discovery of the sinus node by Keith and Flack: on the centennial of their 1907 publication]
Специальные методы исследования
>
Публикации
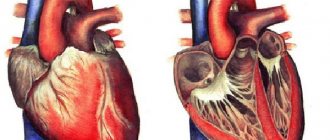
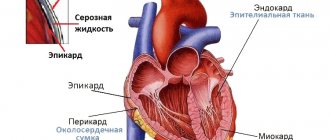
Сердечная мышца состоит из двух отличающихся по структуре и функции элементов – сократительного миокарда и проводящей системы.
Синусовый узел (Кейта–Флака) находится в стенке правого предсердия между устьями полых вен. Это скопление богатых саркоплазмой многоядерных эмбриональных волокон, расположенных в грубоволокнистой соединительнотканной сетке. Импульс от синусового узла распространяется к предсердно-желудочковому узлу (атриовентрикулярному узлу Ашоффа–Тавара ). Предсердно-желудочковый узел имеет такое же строение, как и синусовый, но содержит меньше соединительно-тканных и эластических элементов. Предсердно-желудочковый узел переходит в предсердно-желудочковый пучок, состоящий из волокон, проводящих импульс. Предсердно-желудочковый пучок через мембранозную часть межжелудочковой перегородки проходит на левую сторону, где образует правую и левую ножки. Правая ножка на правой стороне перегородки делится на переднюю среднюю и заднюю ветви. Левая ножка разветвляется по левой стороне перегородки и образует густую сеть волокон Пуркинье Из синусового узла возбуждение распространяется по миокарду предсердии вызывая их сокращение, через 0,02–003 с возбуждение достигает предсердно желудочкового узла и после предсердно желудочковой задержки на 0,04–007 с передается на предсердно желудочковый пучок Через 0,03–0,4 с возбуждение достигает миокарда желудочков после чего наступает систола.
Сердечный цикл подразделяется на систолу и диастолу желудочков, в конце которой совершается систола предсердий.
Объем крови, выбрасываемый желудочком сердца называют ударным, или систолическим объемом сердца а произведение ударного объема на частоту сер дечных сокращений в минуту – минутным объемом. Минутные объемы большого и малого круга кровообращения в норме равны. Минутный объем сердца деленный на площадь поверхности тела, выраженную в квадратных метрах (м2) обозначают сердечным индексом Сердечный индекс выражают в литрах в минуту на 1 м2 по верхности тела л (мин • м2)
Отношение ударного объема к площади поверхности тела называют ударным индексом и выражают в миллиметрах в минуту на 1 м2
мл (мин • м2)
В покое у взрослого человека величина сердчного индекса равна 35 4 л/(мин • м2) При физической нагрузке минутный объем может увеличиваться в 5-10 раз. Нормальное давление в левом желудочке и аорте не превышает 120 мм рт ст а в правом желудочке и в легочной артерии – 25 мм рт ст В норме как между левым желудочком и аортой так и между правым желудочком и легочной артерией разницы (градиента) давления нет. Появление градиента давлений может быть обусловлено затруднением на пути оттока крови или сбросом крови на уровне предсердии желудочков и легочной артерии через дефекты в перегородках и ано мальные межсосудистые сообщения.
Общее периферическое сосудистое сопротивление составляет около 1000 дин/(с • см 5) ив 3–4 раза превышает общее легочное сопротивление. Этим обусловлена разница давления в правом и левом желудочках, в аорте и чегочнои артерии.
Коронарное кровообращение В покое сердце поглощает до 75% кислорода из протекающей через миокард крови (скелетная мышца поглощает 40%) Коронарный кровоток составляет 80 100 мл/мин на 100 см3 массы миокарда (5% сердечного выброса) Коронарный кровоток регулируется изменением сопротивления коронар ных артерий При повышении потребности в кислороде коронарный кровоток воз растает (иногда в 4–5 раз) а поглощение кислорода остается почти постоянным. Количество поглощаемого миокардом кислорода является доминирующим фактором в регуляции коронарного кровотока.
Специальные методы исследования
Для установления точного анатомического диагноза, состояния гемодинамики, степени нарушения сократительной функции миокарда применяют неинвазивные (электрокардиография, фонокар диография, эхокардиография, рентгенография) и инвазивные (зон дирование, ангиокардиография) методы исследования. Эхокардиография дает возможность визуализировать на экране внутрисердечные структуры и с помощью компьютера вы числять основные показатели гемодинамики. Ультразвуковое сканирование позволяет диагностировать дефекты в перегородках сердца, фиброз и кальциноз кла панов, нарушения сократительной функции миокарда вследствие Рубцовых изменений, гипертрофию миокарда и опухоли (миксомы) сердца. Зондирование сердца Во время исследования полостей сердца и сосудов с помощью катетера, соединенного электромагнитным датчиком с мингографом, записывают кривые давления, берут про бы крови для исследования газового состава, вводят контрастное вещество и выполняют рентгенокиносъемку Для исследования левых отделов сердца через катетер, проведенный до правого пред сердия, проводят длинную тонкою изогнутую на конце иглу, кото рой пунктируют межпредсердную перегородку и проникают в левое предсердие (транссептальная пункция) Удалив иглу, катетер про водят в левый желудочек и аорту.
Катетером, проведенным через бедренную или локтевую артерию, достигают восходящей аорты, левого желудочка Применяя специальные катетеры, выполняют селективную коронарографию и левую вентрикулографию.
Кинокардиография имеет большое значение для установления точного диагноза многих врожденных пороков сердца.
Селективная коронарография имеет целью определение прохо димости коронарных артерий При хронической ишемической бо лезни сердца ее производят в нескольких проекциях и одновременно выполняют левую вентрикулографию для определения обширности зон гипо , дис и акинезии.
Обеспечение операций на сердце и крупных сосудах
Предоперационная подготовка кардиохирургических больных складывается из лечебных мероприятий, направленных на умень шение явлений сердечной недостаточности, улучшение функции паренхиматозных органов, ликвидацию нарушений водно электро литного и белкового обмена.
Искусственное кровообращение На период выполнения внут рисердечного этапа операции кровообращение и газообмен обес печивают с помощью аппарата для искусственного кровообраще ния (АИК), который состоит из роликового насоса, оксигенатора, теплообменника и системы управления.
По трубкам, введенным в верхнюю и нижнюю полые вены, кровь вследствие гравитации оттекает в оксигенатор Используют пузырь ковый оксигенатор, в котором кровь смешивается с подаваемым кислородом, и мембранный, в котором газообмен осуществляется через специальную пластмассовую пленку, разделяющую кровь и нагнетаемые газы Это резко уменьшает травму форменных эле ментов и белков крови Насос нагнетает оксигенированную кровь в восходящую аорту или в бедренную артерию Заполняют всю экстракорпоральную систему донорской кровью при операциях у детей и кровезаменителями, плазмой, раствором альбумина для операции у взрослых, корригируя электролитный состав и кислотно-щелочное состояние На каждый литр объема заполнения добавляют 60–80 мг гепарина. Перед подключением магистралей в вену больному также вводят гепарин из расчета 4 мг/кг. По окончании экстракорпорального кровообращения гепарин нейтрализуют введением раствора протамина сульфата под контролем показателей процессов свертывания крови.
При операциях у взрослых используют искусственное кровообращение (при температуре 28–24°С), а при коррекции некоторых сложных врожденных пороков у детей применяют гипотермию Снижение температуры позволяет значительно уменьшить объемную скорость перфузии, а при температуре тела 16–18°С даже остановить кровообращение на 30–40 мин По окончании внутри-сердечного этапа операции температуру крови постепенно повышают и заканчивают перфузию после полного согревания больного до 37°С.
Кардиоплегия. Практически все внутрисердечные операции в условиях искусственного кровообращения выполняют на временно остановленном, расслабленном сердце Для достижения такой обратимой остановки сердца используют специальные кардиоплеги-ческие растворы, которые после пережатия восходящей аорты вводят непосредственно в коронарные артерии через специальные канюли или в корень восходящей аорты Сохранение энергетических ресурсов достигается моментальной остановкой сердца и быстрым его охлаждением с последующим поддержанием темпе ратуры миокарда на уровне 12–16°С В кардиоплегический раствор входят: калий, натрий, хлор, кальций, глюкоза, маннитол, альбумин. Применяют также препараты, защищающие мембрану миоцита, предотвращающие отек и гипоксическое повреждение После операции и возобновления коронарного кровообращения миокард согревается и сердечные сокращения восстанавливаются.
Ранения сердца и перикарда
Наиболее часто раны сердца и перикарда бывают колото-резаными и огнестрельными При ранениях сердца наружная рана мягких тканей обычно локализуется на левой половине грудной клетки спереди или сбоку Однако в 15–17% случаев она расположена на грудной или брюш ной стенке вне проекции сердца Ранения сердца и перикарда нередко комбинируются с повреждением других органов Особенно часто при этом повреждается верхняя или нижняя доля левого легкого. Клиника и диагностика, ранения сердца и перикарда характеризуются следующими признаками – кровотечением, шоком, симптомами тампонады сердца Тяжесть состояния раненых в первую очередь обусловлена острой тампонадой сердца – сдавлением сердца излившейся в полость перикарда кровью. Для возникновения тампонады сердца достаточно наличия 200–300 мл крови, излившейся в полость перикарда Если количество крови достигает 500 мл, то возникает угроза остановки сердца В результате тампонады нарушается нормальное диастолическое наполнение сердца и наступает резкое уменьшение ударного и минутного объема правого и левого желудочков При этом центральное венозное давление резко повышается, а системное артериальное давление резко снижается.
Основные симптомы острой тампонады сердца: цианоз кожи и слизистых оболочек, расширение поверхностных вен шеи, резкая одышка, частый нитевидный пульс, наполнение которого еще больше падает в момент вдоха, снижение уровня артериального давления. Из-за острой анемии головного мозга нередки обморок, спутанное сознание. Иногда бывает двигательное возбуждение. При физикальном исследовании определяют расширение границ сердца, исчезновение сердечного и верхушечного толчка, глухие сердечные тоны. Если одновременно ранено легкое, появляется гемопневмоторакс, на что указывает наличие подкожной эмфиземы, укорочение перкуторного звука и ослабление дыхания на стороне ранения.
При рентгенологическом исследовании обнаруживают расширение тени сердца, которая часто принимает треугольную или шаровидную форму, резкое ослабление пульсации сердца. Последняя в ряде случаев едва заметна. На электрокардиограмме регистрируют снижение вольтажа основных зубцов, признаки ишемии миокарда Лечение: при ранениях сердца необходима немедленная операция, которую выполняют под наркозом Выбор доступа зависит от локализации наружной раны Наиболее часто применяют левостороннюю переднебоковую торакотомию в четвертом–пятом межреберьях При расположении наружной раны рядом с грудиной выполняют продольную стернотомию Перикард вскрывают и быстро обнажают сердце. Временно останавливают кровотечение, закрыв раневое отверстие пальцем После этого полость перикарда освобождают от крови и сгустков. Окончательное закрытие раневого отверстия производят путем ушивания раны узловатыми или П-образными швами из нерассасывающегося шовного материала. При прорезывании швов используют прокладки из мышечной ткани или синтетических полосок Операцию заканчивают тщательным обследованием сердца, чтобы не оставить повреждения в других местах По ходу операции выполняют необходимую интенсивную терапию, которая включает восполнение кровопотери, коррекцию нарушенного гомеостаза. При остановке сердца делают массаж сердца, внутрисердечно вводят тоноген (адреналин). При фибрилляции желудочков выполняют дефибрилляцию. Все мероприятия осуществляют при постоянной искусственной вентиляции легких Прогноз: при ранениях сердца тяжелый. Исход зависит от локализации и размеров раны, тяжести симптомов тампонады, ве личины кровопотери, сроков выполнения операции и полноты реанимационных мероприятий
Врожденные пороки сердца
Врожденные пороки сердца образуются вследствие нарушений процессов эмбриогенеза сердца или задержки его нормального формирования в постнатальном периоде. Среди всех заболеваний сердца они встречаются в 1–2% случаев Около 0,3–0,4% всех детей рождаются с аномалиями развития сердца и магистральных сосудов Существует более 100 различных видов врожденных пороков Врожденные пороки сердца условно можно объединить в следующие группы Первая группа – пороки с внутрисердечными патологическими сообщениями, обусловливающими сброс венозной крови в артериальное русло (справа налево, первично-синие). В эту группу входят- триада, тетрада и пентада Фалло, артезия трехстворчатого клапана, смещение трехстворчатого клапана в сторону правого желудочка с дефектом межпредсердной перегородки, транспозиция сосудов и др. Вторая группа – пороки сердца с внутрисердечными патологическими сообщениями, обусловливающими сброс артериальной крови в венозное русло (слева направо, первично-белые)- дефект (незаращение) межпредсердной перегородки, дефект межжелудоч-ковой перегородки, открытый артериальный проток, аортолегочный свищ, митральный стеноз с дефектом межпредсердной перегородки и др. Третья, группа – врожденные пороки сердца, при которых нарушения кровообращения вызваны сужением магистральных сосудов сердца изолированный с-Геноз легочной артерии, стеноз устья аорты, коарктация аорты.
В данном разделе приводятся сведения о наиболее частых формах врожденных пороков сердца, знания которых необходимы врачу широкого профиля. Изолированное сужение легочной артерии. Изолированный стеноз легочной артерии составляет 2,5–5% от всех больных с врожденными пороками сердца. Различают клапанный и подклапанный стенозы легочной артерии При клапанном стенозе отсутствует разделение клапана на створки. Клапан представляет собой воронку с отверстием, обращенным в просвет легочной артерии Отверстие округлой формы расположено в центре воронки или несколько сбоку Диаметр его колеблется от 2 до 10 мм Всегда имеется постстенотическое расширение основного ствола легочной артерии, достигающее нередко большого диаметра При подклапанном (инфундибулярном) стенозе имеется разрастание фиброзной ткани в виде кольца в области наджелудочкового гребня или в выводном тракте правого желудочка. Стеноз легочной артерии является препятствием на пути тока крови из правого желудочка в малый круг кровообращения Для обеспечения нормального минутного объема правому желудочку приходится выполнять большую работу. Это приводит к выраженной гипертрофии правого желудочка и затем к тоногенной и миогенной дилатации Со временем развивается недостаточность правых отделов сердца с декомпенсацией по большому кругу кровообращения.
Клиника и диагностика: при обследовании обнаруживают одышку, усиливающуюся при физической нагрузке^ сердцебиения, быструю утомляемость При исследовании отмечают наличие сердечного горба, систолическое дрожание во втором–третьем межреберьях у левого края грудины, грубый систолический шум и ослабление II тона над легочной артерией. Артериальное давление понижено до 90/50–95/65 мм рт ст Венозное давление повышено.
На электрокардиограмме правограмма, иногда увеличение зубца Р, укорочение интервала P–Q На фонокардиограмме в точке легочной артерии регистрируется систолический шум в виде ромба При рентгенологическом исследовании имеется увеличение тени сердца за счет правого желудочка, увеличение второй дуги по левому контуру сердца вследствие постстенотического расширения легочной артерии Во втором косом положении – заполнение аортального окна расширенной легочной артерией Легочный рисунок нормальный На рентгенокимограмме видно увеличение зубцов пульсации по контуру правого желудочка, снижение пульсации корней легких. Окончательный диагноз порока ставят на основании результатов внутрисердечного исследования, при котором обнаруживают повышение давления в полости правого желудочка Оно может достигать 300 мм рт ст; отмечают высокий градиент давления между правым желудочком и легочной артерией. Записи давления в правом желудочке и легочной артерии и селективная ангиокар-диография позволяют провести дифференциальный диагноз между клапанным и подклапанным стенозами, определить степень сужения, а также характер дилатации правых отделов сердца. Прогноз- без операции неблагоприятный Продолжительность жизни больных не более 20 лет.
Лечение: хирургическое Операцию выполняют в условиях гипотермии и искусственного кровообращения. При клапанном стенозе рассекают начальный отдел ствола легочной артерии и производят комиссуротомию ножницами или скальпелем – до стенок легочной артерии При инфундибулярном стенозе рассекают выводной тракт правого желудочка, радикально иссекают фиброзное кольцо Если расширить инфундибулярный отдел не удается, то производят вшивание в кардиотомическое отверстие заплаты из синтетического материала.
Врожденный стеноз аорты. Стеноз устья аорты встречается у 5–6% от числа всех больных с врожденными пороками сердца Различают клапанный, подклапанный и надклапанный стенозы.
При клапанном стенозе имеется сращение полулунных створок по комиссурам. Сросшиеся створки имеют форму купола с отверстием на вершине. Часто вместо обычных трех полулунных створок имеются только две. Над суженным клапаном наблюдается пост-стенотическое расширение восходящей аорты Подклапанный стеноз имеет вид фиброзно-мышечного валика или тонкой соединительно-тканной диафрагмы с отверстием в центре Надклапанный стеноз локализуется в нижней трети восходящей аорты и обусловлен гипоплазией ее стенки на ограниченном участке или сужением типа диафрагмы.
Стеноз устья аорты препятствует выбросу крови из левого желудочка в большой круг кровообращения, что способствует выраженной перегрузке левого желудочка и создает условия для его гипертрофии и последующей дилатации. Нарушения гемодинамики, обусловленные стенозом, проявляются в первую очередь расстройствами коронарного и церебрального кровообращения Левожелудочковая недостаточность в связи с большими компенсаторными возможностями миокарда левого желудочка возникает сравнительно поздно, но, возникнув, очень быстро приводит больного к смерти.
Клиника и диагностика при значительном стенозе характерны симптомы, одышка, быстрая утомляемость, приступы сердечной астмы, боли стенокардитического характера, головокружение, обмороки При объективном исследовании обнаруживают резко усиленный и смещенный влево верхушечный толчок, грубое систолическое дрожание в проекции устья аорты Во втором межреберье справа слышен систолический шум, который проводится на сосуды шеи. Пульс слабого наполнения и напряжения, пульсовое давление снижено, систолическое не превышает 80/90 мм рт ст , диастолическое в норме или несколько повышено.
При сфигмографии обнаруживают, что кривая каротидного пульса имеет крутой подъем с зазубриной на вершине в виде петушинного гребня. На электрокардиограмме – левограмма, признаки ишемии миокарда, иногда мерцание предсердий Фонокардиографическая запись систолического шума имеет ромбовидную форму . Рентгенологическое исследование выявляет типичную аортальную конфигурацию сердца с выраженной талией, гипертрофированным и увеличенным левым желудочком, расширение аорты в восходящей ее части На рентгенограмме видны грубые зубцы по контуру левого желудочка Ангиокардиография позволяет точно установить анатомические особенности, место и размеры сужения, а одновременное определение давления в аорте и левом желудочке – цифровое значение градиента давления, вызванного стенозом.
При незначительном сужении устья аорты больные нередко доживают до 40–50 лет При выраженном стенозе прогноз неблагоприятный Больные часто погибают от внезапной остановки сердца вследствие тяжелых нарушений коронарного кровообращения.
Лечение- хирургическое Оно показано при градиенте давления, превышающем 30 мм рт ст Операцию проводят в условиях гипотермии и искусственного кровообращения При клапанном стенозе в случае сохраненных створок и выраженных комиссурах последние рассекают, в результате чего достигается восстановление подвижности створок Подобная комиссуротомия возможна у детей У взрослых вследствие обызвествления и утолщения створок устранение стеноза становится возможным путем иссечения клапана с последующим его протезированием При надклапанном стенозе аорту над местом сужения рассекают в продольном направлении, производят иссечение фиброзного кольца или соединительноткан-ной диафрагмы, и просвет сосуда расширяют за счет вшивания заплаты из синтетического материала в разрез стенки аорты При подклапанном стенозе эффект может быть достигнут лишь путем частичного иссечения суженного участка Необходимо учитывать, что рядом находятся волокна предсердно-желудочкового пучка, повреждение которых может вызвать полную поперечную блокаду сердца.
| назад | вперед |
Далее: Глава 6 Диагностика хронических простатитов.
Вены большого круга кровообращения.
Двуликий янус.
О видах физического упражнения.
3. “бэби-йога”.
Примеры лечения некоторых заболеваний.
Богатство и здоровье — рецепт один и тот же..
Главная
>
Публикации
0.0007
Место нахождения и структура
Синоатриальный узел состоит из группы специализированных клеток, расположенных в стенке правого предсердия, только поперечно к устью полых вен на стыке, где верхняя полая вена входит в правое предсердие. Узел SA располагается в миокарде. Это глубокое образование упирается в сердечные миоциты, принадлежащие правому предсердию, а его поверхностная часть покрыта жировой тканью.
Эта удлиненная структура, которая простирается от 1 до 2 см справа от края ушка, представляет собой гребень правого предсердного придатка, и проходит по вертикали в верхнюю часть концевой канавки. Волокна узла SA являются специализированными кардиомиоцитами, которые смутно напоминают нормальные, сократительные сердечные миоциты. У них есть некоторые сократительные нити, но при этом они не сжимаются так же крепко. Кроме того, волокна СА-узла заметно более тонкие, извилистые и окрашиваются менее интенсивно, чем сердечные миоциты.
Симптомы
Проявления зависят от формы и степени тяжести патологических отклонений. Среди возможных признаков:
- Боли в грудной клетке. Интенсивность различна, от незначительного покалывания до серьезных приступов дискомфорта. Несмотря на яркую выраженность, говорить о происхождении без тщательной диагностики невозможно.
- Ощущение пропускания ударов сердца, трепетания, гулкого биения. При этом тахикардия сменяется обратным явлением. Эпизоды длятся от 15 до 40 минут и чуть более.
- Одышка. Неэффективность работы легочных структур обусловлена гипоксией тканей. Таким способом организм пытается нормализовать кислородный обмен. На начальном этапе, когда дефектов еще нет (размеры сердца обычные, мышечный слой тоже, системы работают стабильно), симптом возникает только при повышенной активности. Заметить его еще сложно. На поздних — появляется интенсивная одышка даже в состоянии покоя. В рамках расширенной диагностики проводятся специфические тесты (велоэргометрия как пример).
- Аритмии иного типа. Помимо ускорения работы сердца фибрилляции, групповые или единичные экстрасистолии.
Опасность конкретного вида определяется в ходе ЭКГ и динамического наблюдения. Потенциально летальные формы развиваются несколько позже от начала основного патологического процесса.
Церебральные структуры страдают в результате гемодинамического нарушения и снижения питания головного мозга:
- Шум в ушах, звон.
- Вертиго. Доходит до того, что пациент не может нормально ориентироваться в пространстве. Страдает внутреннее ухо, мозжечок.
- Цефалгия неопределенного происхождения. По характеру напоминает таковую при повышенном давлении или мигрени.
- Обмороки, синкопальные состояния. До нескольких раз в сутки.
- Психические нарушения. По типу депрессивных эпизодов длительного характера, агрессивности, повышенной раздражительности.
- Когнитивные и мнестические отклонения. Пациент не может вспомнить важные вещи, заполнить новую информацию. Падает эффективность мышления.
- Ощущение онемения конечностей, слабости, сонливости.
Общие симптомы:
- Бледность кожных покровов.
- Цианоз носогубного треугольника.
- Снижение работосуепособности, возможности обслуживать себя в быту.
Симптомы слабости синусового узла определяются церебральными, кардиальными и общими проявлениями.
Иннервация
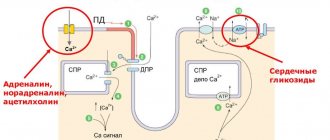
Синусовый узел богато иннервирован парасимпатической нервной системой (десятым черепным нервом (блуждающим нервом)) и волокнами симпатической нервной системы (спинномозговые нервы грудного отдела на уровне хребцов 1-4). Это уникальное анатомическое расположение делает узел СА восприимчивым к явно спаренным и противостоящим вегетативным воздействиям. В состоянии покоя работа узла в основном зависит от блуждающего нерва или его “тонуса”.
- Стимуляция через блуждающие нервы (парасимпатические волокна) вызывает снижение скорости работы узла СА (что в свою очередь уменьшает частоту сердечных сокращений). Таким образом, парасимпатическая нервная система через действие блуждающего нерва оказывает отрицательное инотропное воздействие на сердце.
- Стимуляция через симпатические волокна вызывает увеличение скорости работы узла СА (при этом увеличивается частота сердечных сокращений и сила сокращений). Симпатические волокна могут увеличивать силу сокращения, потому что помимо иннервации синусового и атриовентрикулярного узлов они непосредственно воздействуют на предсердия и желудочки.
Таким образом, нарушение иннервации может приводить к развитию различных расстройств сердечной деятельности. В частности, может повышаться или понижаться ЧСС и возникать клинические признаки.
Классификация
Типизация патологического процесса проводится по ряду оснований.
Исходя из происхождения болезни, говорят о таких видах:
- Первичный СССУ. Развивается на фоне самих кардиальных проблем. Некоторые врачи (теоретики и практики) понимают под указанным термином становление процесса без сторонних факторов. Это крайне редкая ситуация.
- Вторичная разновидность. Формируется под влиянием внесердечных причин. Встречается в 30% зафиксированных случаев.
В зависимости от активности, течения:
- Латентный тип. Определяется в 15% ситуаций. Это наиболее мягкая форма в большинстве случаев, поскольку не имеет симптомов, не прогрессирует на протяжении длительного периода времени. Возможен и обратный вариант, когда движение вперед есть, усугубление тоже, но пациент ничего не чувствует.
- Острый манифестирующий. Характеризуется появлением тяжелого приступа тахикардии или ослабления ЧСС, с выраженными проявлениями со стороны кардиальных структур, нервной системы. Нередко отграничить синдром слабости синусового узла от прочих отклонений с ходу невозможно. Далее течение болезни определяется постоянными рецидивами.
- Хронический тип. Симптоматика присутствует постоянно. Но как таковых обострений нет. Интенсивность проявлений также минимальна. В основном дает знать о себе тахикардией.
По выраженности объективных органических отклонений:
- Компенсированная форма. Сердце пока еще справляется с нарушениями работы. Активизируются адаптивные механизмы, наблюдается адекватная сократимость миокарда.
Подобное положение вещей может сохраняться годами, пациент в таком случае и не подозревает, что болен.
Симптомы отсутствуют или же клиническая картина минимальна. Легкие приступы сердцебиения, незначительная одышка или покалывание в груди. Вот и все, что возникает на фоне данного типа.
- Декомпенсированная форма. Встречается чаще. Это классический вариант, при котором симптоматика достаточно выражена для определения неполадок со здоровьем. Но проявления неспецифичны. Требуется объективная диагностика.
Наконец, исходя их вариантов клинической картины и преобладающего признака:
- Брадикардический вид. Частота сердечных сокращений снижается. Порой до опасного минимума в 40-50 ударов в минуту. Бывает менее. Присутствует угроза острых состояний, вроде инсульта или приступов Морганьи-Адамса-Стокса. Требует имплантации кардиостимулятора.
- Смешанный, брадитахисистолический тип. Отмечается попеременное чередование ускорения и замедления частоты сокращений сердца. Возможно подключение прочих аритмий, что усугубляет прогноз. Качество жизни пропорциональной падает.
Представленные классификации клинически важны, поскольку позволяют определиться с вектором диагностики и выработкой грамотной терапевтической тактики.
Функциональные возможности
- Главный водитель ритма
Хотя некоторые из сердечных клеток обладают способностью генерировать электрические импульсы (или потенциалы действия), которые вызывают сердечное сокращение, синоатриальный узел обычно инициирует сердечный ритм просто потому, что он генерирует импульсы быстрее и сильнее, чем другие области с потенциалом генерации импульсов. Кардиомиоциты, как и все мышечные клетки, имеют рефрактерные периоды после сокращения, в течение которых дополнительные сокращения не могут быть вызваны. В такие моменты их потенциал действия переопределяется синоатриальным или атриовентрикулярным узлами.
В отсутствие внешнего нейронного и гормонального контроля клетки в синоатриальном узле, расположенные в правом верхнем углу сердца, будут естественным образом разряжаться (создавать потенциалы действия) более 100 ударов в минуту. Поскольку синоатриальный узел отвечает за остальную часть электрической активности сердца, его иногда называют основным кардиостимулятором.
Диагностика
Обследованием пациентов занимаются кардиологи. Специалисты по патологиям ЦНС и гормональным проблемам также могут быть привлечены в рамках определения происхождения процесса.
Перечень мероприятий:
- Устный опрос человека и сбор анамнестических данных.
- Измерение артериального давления, подсчет частоты сердечных сокращений.
- Электрокардиография. Основная методика. Предоставляет возможность определить характер функциональных нарушений в краткосрочной перспективе.
- Суточное мониторирование. Суть заключается в оценке АД и ЧСС на протяжении 24 часов.
- Эхокардиография. Визуализация кардиальных структур. Одна из главных методик раннего выявления органических дефектов.
- МРТ по показаниям для получения четких изображений.
- Коронография.
Также оценка неврологического статуса, анализ крови на гормоны, общий, биохимический. Диагностика проводится в амбулаторных или стационарных условиях. Во втором случае происходит быстрее.
Клиническое значение
Дисфункция синусового узла выражается в нерегулярном сердцебиении, вызваннои неправильными электрическими сигналами сердца. Когда синусовый узел сердца неисправен, сердечный ритм становится ненормальным — как правило, слишком медленным. Иногда появляются паузы в его воздействии или комбинации, и очень редко ритм бывает быстрее, чем обычно.
Окклюзия артериального кровоснабжения синусового узла (чаще всего из-за инфаркта миокарда или прогрессирующей болезни коронарной артерии) может вызвать ишемию и гибель клеток в СА узле. Это нередко нарушает пейсмекерную активность САУ и приводит к синдрому слабости синусового узла.
Если узел СА не работает или сгенерированный в нем импульс блокируется до того, как он проходит вниз по электропроводящей системе, группа клеток, расположенных дальше по сердцу, выполняют роль водителей ритма второго порядка. Этот центр обычно представлен клетками внутри атриовентрикулярного узла (AV-узла), который является областью между предсердиями и желудочками, внутри предсердной перегородки.
Если узел AV также терпит неудачу, волокна Пуркинье иногда могут действовать как кардиостимулятор по умолчанию. Если же клетки волокон Пуркинье не контролируют сердечный ритм, то чаще всего по той причине, что они генерируют потенциалы действия с более низкой частотой, чем узлы AV или SA.
Механизм возникновения патологии
Понимание сути развития болезни заключается в определении анатомических и физиологических особенностей.
В основе синдрома лежит нарушение нормальной активности синусового узла. Это специальное скопление клеток, ответственных за генерирование электрического импульса достаточной мощности. В адекватных условиях сердце работает автономно, без сторонних факторов стимуляции. Выработка сигнала — задача водителя ритма.
Под действием тех или иных моментов происходит снижение интенсивности электроимпульса. Он продолжает проводиться по специальным волокнам к атриовентрикулярному узлу и далее по ножкам пучка Гиса, но сила столь мала, что не позволяет сократиться миокарду полностью.
Восстановление проводится радикальными, но не всегда хирургическими методами. Суть заключается в стимуляции «ленивого» сердца.
По мере прогрессирования патологического процесса наблюдается еще большее ослабление в работе миоцитов.
Возникает нарушение сократимости миокарда, снижается кровяной выброс, гемодинамика страдает. Тотальные функциональные дефекты нередко приводят к остановке работы органа, инфаркту или коронарной недостаточности.
Дисфункция синусового узла
Дисфункция узла СА относится к ряду состояний, вызывающих физиологическое несоответствие показателей предсердий. Симптомы могут быть минимальными или включать слабость, непереносимость усилий, учащенное сердцебиение и обморочное состояние. Диагноз ставится на основании ЭКГ. Симптоматическим пациентам требуется кардиостимулятор.
Дисфункция синусового узла включает
- Жизнеопасную синусовую брадикардию
- Чередующуюся брадикардию и предсердные тахиаритмиями (синдром брадикардии и тахикардии)
- Синоатриальную блокаду или временную остановку работы САУ
- Выходную блокаду САУ
Дисфункция синусового узла возникает преимущественно у пожилых людей, особенно при наличии других сердечных расстройств или сахарного диабета.
Остановка синусового узла — это временное прекращение активности синусового узла, наблюдаемое на ЭКГ в виде исчезновения P-волн в течение нескольких секунд.
Пауза обычно вызывает активность эвакуации в более низких кардиостимуляторах (например, предсердный или соединительный), сохраняя частоту сердечных сокращений и функцию, но длительные паузы становятся причиной головокружения и обмороков.
При выходной блокаде СА узла его клетки деполяризуются, но при этом нарушается передача импульсов в миокард предсердий.
- При блокаде САУ 1-й степени импульс немного замедляется, но при этом ЭКГ остается нормальным.
- При блокаде САУ 2-й степени I типа импульсная проводимость замедляется вплоть до полной блокады. На ЭКГ нарушения видны как интервалы P-P, которые постепенно уменьшаются до тех пор, пока P-волна вообще не исчезает. Вместо нее появляется пауза и сгруппированные удары. Продолжительность задержки импульсов составляет менее 2 циклов P-P.
- При блокаде САУ 2-й степени II типа проводимость импульсов блокируется без предшествующего замедления, в результате создается пауза, которая является кратной интервалу P-P и проявляется на ЭКГ сгруппированными сердцебиениями.
- При блокаде САУ 3-й степени проводимость импульсов полностью блокируется; Р-волны отсутствуют, что приводит к полному отказу синусового узла.
Этиология
Дисфункция синусового узла может развиваться, когда электрическая система сердца повреждена из-за органических или функциональных нарушений. Причины дисфункции синусового узла включают:
- Старение. Со временем связанный с возрастом износ сердца может ослабить работу синусового узла и заставить его неправильно функционировать. Возрастное повреждение сердечной мышцы является наиболее распространенной причиной дисфункции синусового узла.
- Лекарственные препараты. Некоторые медикаменты для лечения высокого артериального давления, болезни коронарных артерий, аритмий и других сердечных заболеваний могут вызывать или ухудшать функцию синусового узла. К таким препаратам относятся бета-блокаторы, блокаторы кальциевых каналов и антиаритмические средства. Все же принимать сердечные лекарства чрезвычайно важно и при выполнении врачебных рекомендаций они в большинстве случаев не вызывают проблем.
- Операция на сердце. Хирургические вмешательства с участием верхних камер сердца могут привести к образованию рубцовой ткани, которая блокирует электрические сигналы от синусового узла. Послеоперационные рубцы на сердце обычно являются причиной дисфункции синусового узла у детей с врожденным пороком сердца.
- Идиопатический фиброз узла СА, который может сопровождаться дегенерацией ниже расположенных элементов проводящей системы.
Другими причинами являются наркотики, чрезмерный вагусный тонус и различные ишемические, воспалительные и инфильтративные расстройства.
Симптомы и признаки
Часто дисфункция синусового узла не вызывает симптомов. Только когда состояние становится серьезным, возникают проблемы. Даже признаки болезни могут быть расплывчатыми или вызванными другими патологиями.
Симптомы дисфункции синусового узла включают:
- Обморок или предобморочное состояние, вызванное тем, что мозг не получает достаточное количество крови от сердца. Также может возникнуть головокружение.
- Боль в груди (по типу стенокардической), возникает тогда, когда сердцу не хватает кислорода и питательных веществ.
- Усталость, вызванная нарушением работы сердца, которое не прокачивает кровь достаточно эффективно. Когда кровоток уменьшается, жизненно важные органы недополучают кровь. Это может оставить мышцы без достаточного количества питания и кислорода, вызывая слабость или недостаток энергии.
- Одышка, возникает в основном при присоединении к дисфункции СА узла сердечной недостаточности или отека легких.
- Плохой сон, вызванный ненормальным сердечным ритмом. Апноэ сна, при котором человек испытывает паузы во время дыхания, может способствовать дисфункции синусового узла из-за уменьшения подачи кислорода к сердцу.
- Нарушенное сердцебиение, изменяется чаще всего в сторону его учащения (тахикардии). Иногда ощущается, что ритм неправильный или наоборот чувствуется стук в груди.
Диагностика
После врачебного сбора медицинской истории и проведения физического обследования, назначаются тесты, используемые для диагностики дисфункции синусового узла. Чаще всего к ним относится:
- Стандартная электрокардиограмма (ЭКГ). Широко используется для выявления нерегулярного сердечного ритма. Перед исследованием на грудь, руки и ноги помещаются электроды, чтобы обеспечить разностороннее измерение сердца. Посредством проводов электроды прикрепляются к аппаратуре, которая измеряет электрическую активность сердца и преобразует импульсы в линии, выглядающие как ряд зубцов. Эти линии, называемые волнами, показывают определенную часть сердечного ритма. Во время анализа ЭКГ врач исследует размер и форму волн и количество времени между ними.
- Холтеровский мониторинг. Прибор постоянно регистрирует сердцебиение в течение 24-48 часов. Три электрода, прикрепленные к грудной клетке, подключены к устройству, которое больной носит в кармане или надевает на пояс / плечевой ремень. Дополнительно больной ведет дневник своих действий и симптомов во время ношения монитора. Это позволяет врачам определить, что именно происходило в момент нарушения ритма.
- Монитор событий. Этим методом регистрируется сердцебиение только тогда, когда испытываются симптомы болезни. Монитор событий может использоваться вместо монитора Холтера, если симптомы у больного встречаются реже, чем один раз в день. Некоторые мониторы событий имеют провода, которые соединяют их с электродами, прикрепленными к грудной клетке. Прибор автоматически начинает запись, когда обнаруживает нерегулярное сердцебиение, или больной начинает запись при возникновении симптомов.
- Нагрузочный тест на беговой дорожке. Это тестирование может быть выполнено для определения соответствующего ответа на тренировку, представляемого в виде изменения частоты сердечных сокращений.
Прогноз
Прогноз при дисфункции синусового узла неоднозначен.
При отсутствии лечения, смертность составляет около 2% / год, в основном в результате прогрессирования основного заболевания, нередко представляющего собой структурное поражение сердца.
Каждый год примерно у 5% пациентов развивается фибрилляция предсердий с возникновением таких осложнений, как сердечная недостаточность и инсульт.
Причины
Факторы развития делятся на две группы. Первичные обусловлены нарушением работы самого сердца, также сосудов. Вторичные — экстракардиальными моментами и заболеваниями.
Первичные
- ИБС. Сопровождает пациентов в возрасте от 40 лет. В редких случаях возможны формирования нарушений в ранний период.
Суть заключается в невозможности нормального обеспечения кровью самих сердечных структур.
Из-за постоянной гипоксии развиваются органические нарушения: нарастает мышечная масса, расширяются камеры. Слабость синусового узла — возможный вариант, но наблюдается не всегда.
- Аутоиммунные патологии, затрагивающие кардиальные структуры и сосуды. Васкулит, ревматизм, системная красная волчанка и прочие.
Затрагивают мышечный слой. Деструкция тканей приводит к их замещению рубцовыми фрагментами и развитию кардиосклероза.
Они не могут сокращаться, не обладают эластичностью, отсюда невозможность адекватной работы. Кровь перекачивается с меньшей интенсивностью.
В перспективе нескольких лет это может закончиться тотальной полиорганной дисфункцией или неотложными состояниями.
- Воспаление сердца (миокардит) и окружающих структур. Инфекционного, реже аутоиммунного генеза. Восстановление в стенах стационара, с применением антибиотиков и кортикостероидов. Несвоевременная помощь приводит к деструкции тканей, минимум тяжелой инвалидности, максимум — к летальному исходу.
- Кардиомиопатия. Нарушение разрастания мышечного слоя или же расширении камер сердца. Оба состояния потенциально смертельны без своевременной помощи. Радикальное лечение невозможно, требуется применение поддерживающих препаратов для остановки процесса. Длительность полезного воздействия — вся жизнь.
- Операции на сердце. Даже незначительные на первый взгляд, вроде проведенной радиочастотной абляции, прочих. Безопасных вмешательств на кардиальных структурах не существует. Всегда есть риск осложнений. Так, на фоне прижигания обширного участка либо если обработана функционально активная, здоровая область, вероятность аритмии выше.
- Травмы сердца. К таковым приводят ушибы грудной клетки, переломы ребер. Врожденные и приобретенные органические отклонения развития кардиальных структур. Множественны по характеру. Наиболее типичными считаются пролапс митрального клапана, прочие состояния, вызывающие обратный ток крови (регургитацию), аортальная недостаточность и многие другие. На ранних этапах не проявляют себя никак. Возможно отсутствие симптомов пороков вплоть до наступления летального исхода.
В редких случаях — гипертоническая болезнь запущенного типа.
Вторичные факторы
Внесердечные проблемы менее распространены:
- Интоксикации выраженного характера. Причин состоянию масса. От раковых процессов запущенного этапа до отравления солями металлов, болезней печени декомпенсированного типа.
- Вегетативная дисфункция (ВГСУ) проявляется часто. Возможно временное ослабление работы синусового узла в результате рвоты, кашля, перемены положения тела, метеозависимости, занятий спортом. Дистония также играет роль. Но это не диагноза, а симптом того или иного заболевания.
- Передозировка препаратов антигипертензивного, кардиостимулирующего действия. К подобному же итогу приводит длительное применение этих средств.
- Метаболические процессы, ассоциированные с нарушением обмена калия, магния.
- Сифилис, ВИЧ, туберкулез. Опасные инфекционные или вирусные процессы.
- Возраст от 50 лет. Организм утрачивает возможность адекватно адаптироваться к вредным факторам внешнего и внутреннего характера. Потому риски развития патологий кардиального профиля выше.
- Длительное голодание, кахексия. Складывается как итог объективных процессов (рак, инфекции, болезнь Альцгеймера, сосудистая и иная деменция) или сознательного отказа от пищи (диета, анорексия).
- Поражения эндокринного профиля. Диабет, гипертиреоз (избыточная выработка гормонов щитовидной железы), обратный процесс, дефицитарные состояния по части надпочечников.
В отсутствии данных за органические патологии говорят об идиопатической форме. Это также распространенный вариант.
Восстановление заключается в купировании признаков. Эффективность подобной меры спорная, без этиоропной составляющей действие неполное.
Функции сердца
Прежде чем говорить о классификации пейсмейкеров или водителей ритма, следует сказать об основных функциях сердца:
- Сердце обладает автоматизмом, что означает способность пейсмейкерной системы к самостоятельному вырабатыванию импульсов возбуждения в автоколебательном режиме. Вышележащие отделы проводящей системы оказывают угнетающее действие на нижележащие, так как пейсмейкер первого порядка обладает большим автоматизмом, чем водитель ритма сердца второго, третьего или четвертого порядков.
- Сердце обладает возбудимостью, что означает способность кардиомиоцитов к возбуждению под воздействием раздражителей различного происхождения, химического или физического.
- Сердце обладает проводимостью, что означает способность структур сердца проводить возбуждение от одного участника пейсмейкерной системы к другому вследствие изменения потенциала действия.
- Сердце обладает сократимостью, что означает способность сердечной мышцы к сокращению под воздействием электрических импульсов, и сокращение тем больше, чем больше длина мышечного волокна.
- Сердце обладает рефрактерностью, что означает способность кардиомиоцитов временно быть невосприимчивыми к любым импульсам после сокращения. Функция обеспечивает восстановление потенциала действия в клетках и отдых сердечной мышцы.
АТРИОВЕНТРИКУЛЯРНЫЙ УЗЕЛ
Атриовентрикулярный узел находится справа от межпредсердной перегородки над местом прикрепления створки трехстворчатого клапана, непосредственно рядом с устьем коронарного синуса. Форма и размеры его разные: в среднем длина его достигает 5-6 мм, а ширина — 2-3 мм.
Подобно синусовому узлу, атриовентрикулярный узел содержит также два вида клеток — Р и Т. Однако имеются значительные анатомические различия между синоаурикулярным и атриовентрикулярным узлами. В атриовентрикулярном узле гораздо меньше Р-клеток и незначительное количество сети коллагеновой соединительной ткани. У него нет постоянной, центрально проходящей артерии. В жировой клетчатке за атриовентрикулярным узлом, вблизи устья коронарного синуса, находится большое число волокон и ганглиев блуждающего нерва. Кровоснабжение атриовентрикулярного узла происходит посредством ramus septi fibrosi, называемой еще артерией атриовентрикулярного узла. В 90% случаев она отходит от правой венечной артерии, а в 10% — от ramus circumflexus левой венечной артерии.
Клетки атриовентрикулярного узла связываются анастомозами и образуют сетчатую структуру. В нижней части узла, перед переходом в пучок Гиса, клетки его располагаются параллельно друг другу.