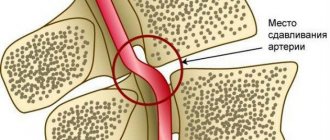
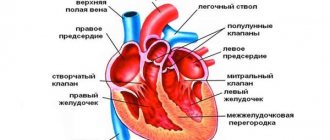
Уровни кровеносной системы
Условно все кровоснабжение органов и систем организма можно подразделить на три уровня:
- Системное кровообращение — образовано крупными сосудами, которые обеспечивают перемещение крови по всему организму.
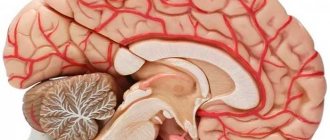
- Органное кровообращение — образовано сосудами среднего диаметра, которые обеспечивают кровоснабжение отдельных органов в зависимости от их потребности в кислороде. Например, головной мозг снабжается кровью очень обильно, так как нуждается в большом количестве энергии, а следовательно, и в кислороде.
- Микроциркуляция — включает в себя наиболее мелкие сосуды, которые находятся в непосредственном контакте с клетками и тканями.
Типовые нарушения лимфодинамики
1. Актуальность темы: патологические процессы, протекающие в капилляро-трофической области, являются ведущим механизмом, лежащим в основе повреждения различных органов и систем. Трофическая функция капилляро-соединительнотканных структур и их тесная взаимосвязь с лимфатическими дренажными структурами крайне ранимы и очень часто повреждаются различными факторами как внешней, так и внутренней структуры.
Кровообращение на участке периферического сосудистого русла, кроме движения крови, обеспечивает обмен воды, электролитов, газов, необходимых питательных веществ и метаболитов по системе кровь — ткань — кровь. В органе или тканях в ответ на функциональные и структурные изменения в них могут возникать местные нарушения кровообращения: артериальная и венозная гиперемия, ишемия, стаз. К местным нарушениям кровообращения могут приводить тромбоз и эмболия.
https://www.youtube.com/watch?v=https:accounts.google.comServiceLogin
Недостаточность лимфообращения —состояние, при котором лимфатические сосуды не выполняют свою основную функцию — осуществление постоянного и эффективного дренажа интерстиция.
Микроциркуляция: что это такое?
Микроциркуляция — это передвижение крови по микроскопической, то есть мельчайшей, части сосудистого русла. Выделяют пять типов сосудов, которые входят в ее состав:
- артериолы;
- прекапилляры;
- капилляры;
- посткапилляры;
- венулы.
Что интересно, не все сосуды этого русла функционируют одновременно. Пока некоторые из них активно работают (открытые капилляры), другие находятся в «спящем режиме» (закрытые капилляры).
Регуляция передвижения крови по мельчайшим кровеносным сосудам осуществляется сокращением мышечной стенки артерий и артериол, а также работой специальных сфинктеров, которые расположены в посткапиллярах.
Проблемы с микроциркуляцией
Нарушение работы капиллярного русла лежит в основе большинства патологических процессов. На микроскопическом уровне происходит спазм артериол либо их закупорка микротромбами из форменных элементов крови. Это приводит к недостатку кислорода, переходу клеток на анаэробный (без участия кислорода) процесс расщепления глюкозы.
В результате в организме накапливаются кислые продукты обмена веществ, в частности, молочная кислота или лактат, что сильно усугубляет метаболические нарушения.
Некоторые заболевания, патогенез которых основан на микроциркуляторных нарушениях:
- Сахарный диабет. Одно из основных осложнений – микроангиопатии, то есть патология именно капиллярного русла. Плохой контроль гликемии приводит к утолщению капиллярных стенок и нарушению транспорта через мембраны. Нарушается питание тканей, на ногах появляются трофические язвы. Поражение касается практически всех сосудов, даже артериол сетчатки в глазах.
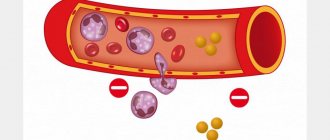
- Ишемическая болезнь сердца (ИБС). Основная причина ИБС – отложение холестерина на стенках сосудов, образование атеросклеротических бляшек. Эти факторы нарушают нормальный периферический кровоток, сосуды становятся ригидными. Страдает не только миокард, но и другие органы. Трофические нарушения на нижних конечностях часто вызваны облитерирующим атеросклерозом сосудов.
- Инсульт или нарушение мозгового кровообращения. Тромбоз или разрыв мозгового сосуда приводит и ишемическому или геморрагическому инсульту соответственно. Повреждение нервных клеток (нейронов) возникает вследствие блокады мельчайшего сосудистого русла.
- Заболевания почек. Почечная патология связана с нарушением элиминации жидкости и продуктов азотистого обмена. Постепенное накопление мочевины также негативно влияет на сосудистую перфузию, нарушая нормальную трофику тканей.
Здесь перечислены далеко не все патологические процессы, патогенез которых основан на микроциркуляторных нарушениях. Наличие системного атеросклероза всегда усугубляет ситуацию. Пациентам с большим количеством холестериновых бляшек и утолщением сосудистых стенок восстановиться после инсульта, например, гораздо сложнее.
до змісту↑
Особенности строения
Микроциркуляторное русло имеет разное строение, в зависимости от того, в каком органе оно находится.
Например, в почках капилляры собраны в клубочек, который образуется из приносящей артерии, а из самого клубочка капилляров после образуется выносящая артерия. Причем диаметр приносящей в два раза больше, чем выносящей. Такое строение необходимо для фильтрации крови и образования первичной мочи.
А в печени находятся широкие капилляры, называемые синусоидами. В эти сосуды из воротной вены поступает и насыщенная кислородом артериальная, и бедная им венозная кровь. Специальные синусоиды присутствуют и в костном мозге.
Патологические состояния
Ток крови в микроциркуляторном русле находится в зависимости от постоянства внутренней среды организма. В том числе на нормальную функцию сосудов наибольшее влияние оказывает работа сердца и эндокринных желез. Однако имеют влияние и другие внутренние органы. Поэтому состояние микроциркуляции отражает работу организма в целом.
Условно все патологические состояния сосудов микроциркуляторного русла можно разделить на три группы:
- изменения внутри сосуда — нарушение тока крови внутри него при увеличении ее вязкости и нарушении стабильности клеток крови;
- нарушение целостности стенки сосуда — повышенная проницаемость сосудистой стенки;
- изменения вне сосуда — эндокринологические болезни, нарушение сердечной деятельности.
Анатомия и физиология микроциркуляторного русла
Под термином микроциркуляция в широком смысле слова понимают не только кровоток и лимфоток в микрососудах, но и обменные процессы, осуществляющиеся через стенку микрососудов, а также интерстициальный (внесосудистый) транспорт жидкости и содержащихся в ней веществ, клеток и различных структур.
К микрососудам относятся:
- сосуды артериолярного типа — артериолы, метартериолы, прекапилляры и капилляры диаметром не превышающие 100 мкм;
- сосуды венулярного типа — посткапилляры, венулы, диаметр которых не превышает 200 мкм;
- лимфатические микрососуды — лимфатические капилляры, посткапилляры и микрососуды, имеющие диаметр не более 300 мкм;
- анастомозы (шунты), соединящие между собой две артериолы (артериоло-артериолярные), две венулы (венуло-венулярные), артериолу с венулой (артериоло-венулярные).
Главное отличие микрососудов от макрососудов заключается в том, что помимо транспортной они выполняют обменную функцию. Необходимо отметить, что обмен веществ осуществляется через стенку всех микрососудов — от артериолы до венулы, — а не только через стенку капилляров, как предполагалось ранее. Особенность лимфатических макро- и микрососудов — постоянный двусторонний обмен из ткани в сосуд и из сосуда в ткань на всем протяжении до впадения конечного участка грудного лимфатического протока в правый венозный угол и в правое предсердие. В связи с этим состав лимфы в каждом участке лимфангиона (расстояние между соседними клапанами лимфатического сосуда) бывает различным. Повышенная проницаемость лимфатических микрососудов объясняется тончайшим строением их стенки, не имеющей непрерывной базальной мембраны, а в лимфатических капиллярах и посткапиллярах базальной мембраны нет. Их стенка состоит из одного ряда черепицеобразно расположенных эндотелиальных клеток. Межэндотелиальные каналы свободно пропускают не только отдельные клетки, но и целые конгломераты, что исключает необходимость существования лимфо-венозных анастомозов.
Одна из важных структур микроциркуляторного русла — прекапиллярный сфинктер (рис. 1), который представляет собой участок прекапилляра, содержащий две гладкомышечные клетки, расположенные в начале прекапилляра. Через него без деформации может пройти только один эритроцит. В более узких капиллярах с диаметром около 5 мкм эритроцит обязательно деформируется, вытягиваясь в длину в 3—7 раз (в зависимости от скорости кровотока и градиента давления в капилляре). По форме эритроцита можно судить о скорости кровотока в микрососуде. При высокой скорости клетки вытянуты, при низкой эритроциты принимают более округлую форму (рис. 2).
Причина, по которой мы подробно останавливаемся на строении прекапиллярного сфинктера, объясняется важностью его роли в развитии патологии. Гладкомышечные клетки прекапиллярного сфинктера обладают сверхчувствительностью к катехоламинам (адреналину, норадреналину). Например, чувствительность гладкомышечной клетки прекапиллярного сфинктера к адреналину в 100 раз больше по сравнению с аналогичной клеткой артериолы диаметром 50 мкм и в 50 раз больше по сравнению с аналогичной клеткой артериолы диаметром 20 мкм (см. рис. 1).
Эта особенность гладкомышечных клеток прекапиллярного сфинктера имеет особое значение. В условиях острого стресса выброс значительного количества катехоламинов сопровождается спазмом коронарных и других сосудов. Возникающая острая боль в области сердца сигнализирует о необходимости принять сосудорасширяющий препарат типа нитроглицерина. Это знают все: и больной, и врач.
Совсем другая ситуация развивается в условиях хронического стресса, под которым мы понимаем состояния, сопровождающиеся длительной неудовлетворенностью человека окружающей его действительностью: долговременные переживания в связи с утратой близких или потерей работы; конфликты в семье или рабочем коллективе, постоянная нехватка времени, недостаточный сон, дефицит положительных эмоций и многое другое, вызывающее у человека раздражение. В этих ситуациях выброс катехоламинов будет незначительным: не будет болевого приступа, нарушений центральной гемодинамики, артериальное давление останется в пределах нормы. Однако сверхчувствительные клетки прекапиллярного сфинктера будут реагировать сокращением даже на ничтожные дозы катехоламинов. Его просвет уменьшится, и через прекапиллярный сфинктер не сможет пройти ни один эритроцит. К тканям, кровоснабжение которых идет через капиллярные сети, сохранится приток плазмы, но не попадет кислород, который переносят эритроциты. Следствием длительного сужения прекапиллярного сфинктера в ответ на небольшие дозы катехоламинов в крови в условиях хронического стресса возникнет хроническая гипоксия тканей и органов, кровоснабжаемых капиллярными сетями.
Рисунок 2. Изменение формы эритроцита при различной скорости кровотока в микрососудах брыжейки тонкой кишки крысы. Вытянутые эритроциты в капилляре (3) и артериоле (5) при нормальной скорости кровотока; овальная форма — при резко замедленном кровотоке (4); «квадратные» эритроциты при замедлении скорости кровотока (1, 2). Биомикроскопия. Увеличение: об. х 70, ок. х 3.
Дальнейший сценарий далеко не самый оптимистичный: от снижения функциональной активности органов до развития различных заболеваний, например онкологических. В условиях гипоксии клетки быстрее деградируют, клетки иммунной системы воспринимают их как чужеродные и фагоцитируют. Быстрая гибель не достигших зрелости клеток и усиленный рост новых, также вскоре разрушающихся, приведут к малигнизации клеток и опухолевому процессу.
Внутрисосудистые изменения
Замедление тока крови в сосудах, которое может проявляться как при специфических заболеваниях, тромбоцитопатиях (нарушении функции тромбоцитов) и коагулопатиях (нарушении свертывания крови), так и при патологиях, которые могут встречаться при разнообразных заболеваниях организма. К таким состояниям относятся агрегация эритроцитов и сладж-синдром. По сути, эти два процесса являются последовательными стадиями одного феномена.
Сначала происходит временное прикрепление эритроцитов при помощи поверхностных контактов в виде столбика (агрегация эритроцитов). Такое состояние обратимо и обычно носит кратковременный характер. Однако прогрессирование его может привести к прочному склеиванию (адгезии) кровяных телец, что уже является необратимым.
Такая патология носит название сладж-феномена. Это приводит к замедлению и полному прекращению тока крови в сосуде. Обычно закупориваются венулы и капилляры. Обмен кислорода и питательных веществ останавливается, что в дальнейшем вызывает ишемию и некроз тканей.
Трансмуральные нарушения микроциркуляции
Через стенку микрососуда циркулируют жидкая часть крови и лимфы (характеризуется понятием: «проницаемость сосудистой стенки» для плазмы) и форменные элементы крови (описывается понятием «эмиграция»).
В соответствии с преобладанием расстройств проницаемости или эмиграции трансмуральные нарушения микроциркуляции компонентов крови и лимфы подразделяют на две категории:
Ú расстройства проницаемости стенок микрососудов для жидкости;
Ú нарушения эмиграции форменных элементов крови через стенку микрососудов.
Нарушение проницаемости стенки микрососуда для жидкости
При различных патологических состояниях объём перемещения плазмы крови и/или лимфы через стенку сосуда может чрезмерно (неадекватно) либо возрастать, либо уменьшаться.
Увеличение перемещения жидкости через стенку сосудов микроциркуляторного русла
Основные причины повышения проницаемости стенок микрососудов приведены на рис. 23.54.
Ы ВЁРСТКА Вставить файл «ПФ_Рис.23.54» МС Ы
Рис. 23.54. Основные причины повышения проницаемости стенок микрососудов для жидкости.
Главное последствие повышения проницаемости стенок микрососудов — потенцирование механизмов циркуляции жидкости:
Ú фильтрации (транспорта жидкости по градиенту гидростатического давления);
Ú трансцитоза(энергозависимого пиноцитоза);
Ú диффузии (переноса жидкости без затрат энергии);
Ú осмоса (направленной диффузии жидкости по градиенту осмотического давления).
Уменьшение проницаемости стенок сосудов микроциркуляторного русла
Причины снижения проницаемости стенок микрососудов:
Ú утолщение стенок микрососудов(например, при хронических васкулитах);
Ú уплотнение стенок микрососудов(например, вследствие их кальцификации).
Наиболее значимым последствиемуменьшения проницаемости стенок микрососудов является снижение эффективности механизмов перемещения через них жидкости:
Ú фильтрации;
Ú диффузии;
Ú трансцитоза;
Ú осмоса.
Нарушение перемещения форменных элементов крови через стенку микрососуда
Эмиграция лейкоцитов через стенку микрососудов (в ткань и обратно) осуществляется в норме постоянно. Лейкоциты выполняют в тканях функцию иммунобиологического надзора за индивидуальным и постоянным антигенным составом организма. Эритроциты и тромбоциты такой способностью не обладают.
При различных патологических состояниях эмиграция лейкоцитов через стенку микрососуда, как правило, возрастает; эритроциты и тромбоциты перемещаются в ткань пассивно с током плазмы крови.
К типовым формам патологии перемещения форменных элементов крови через стенку микрососуда в ткань относят:
Ú чрезмерный выход из микрососудов эритроцитовс развитием микрогеморрагий (например, при васкулитах или геморрагических синдромах);
Ú избыточное перемещение в ткань тромбоцитов(обычно вместе с эритроцитами).
Экстраваскулярные нарушения микроциркуляции
Внесосудистые (экстраваскулярные) нарушения микроциркуляции сопровождаются увеличением или уменьшением объёма межклеточной жидкости, что приводит к замедлению оттока её в сосуды микроциркуляторного русла.
Причина чрезмерного замедления оттока интерстициальной жидкостии избыточного увеличения ее объема — местные тканевые патологические процессы. Наиболее часто это:
Ú воспаление;
Ú аллергические реакции;
Ú рост новообразований;
Ú склерозирование ткани;
Ú венозная гиперемия;
Ú стаз.
Последствия замедления оттока интерстициальной жидкости и избыточного увеличения ее объема:
Ú увеличение содержания в интерстициальной жидкости продуктов нормального и нарушенного метаболизма (ряд таких метаболитов может оказывать цитотоксическое и цитолитическое действие);
Ú дисбаланс ионов (это способствует отёку ткани, нарушает формирование МП и ПД);
Ú образование избытка и/или активация БАВ (например, ФНО-a, прокоагулянтов, мембраноатакующего комплекса), способных усугубить повреждение клеток, потенцировать расстройства крово- и лимфообращения, пластических процессов;
Ú нарушение обмена O2, CO2, субстратов и продуктов обмена веществ;
Ú сдавление клеток избытком интерстициальной жидкости.
Причины чрезмерного замедления оттока интерстициальной жидкости, сочетающегося с уменьшением её оттока из интерстициального пространства:
Ú гипогидратацияорганизма, тканей и органов (например, в результате длительной диареи, плазморрагии, при интенсивном потоотделении);
Ú снижение лимфообразования (например, при ишемии ткани или системной гиповолемии);
Ú уменьшение эффективности фильтрации жидкости в артериолах и прекапиллярах и/или увеличение реабсорбции её в посткапиллярах и венулах (например, при дистрофических и склеротических процессах в тканях).
Последствия чрезмерного уменьшения оттока интерстициальной жидкости сходны с наблюдающимися при увеличении объёма интерстициальной жидкости, сочетающемся с замедлением её оттока (см. выше).
Капилляро-трофическая недостаточность
Капилляро-трофическая недостаточность—состояние, характеризующееся следующими нарушениями, приводящими к расстройству обмена веществ и пластических процессов в тканях и органах:
Ú крово- и лимфотока в сосудах микроциркуляторного русла;
Ú транспорта жидкости и/или форменных элементов крови через стенки микрососудов;
Ú оттока межклеточной жидкости (рис. 23.55).
Ы ВЁРСТКА Вставить файл «ПФ_Рис.23.55» МС Ы
Рис. 23.55. Признаки капилляро-трофической недостаточности.
Последствия капилляро-трофической недостаточности
В результате описанных выше расстройств микроциркуляции крови, лимфы и межклеточной жидкости в тканях и органах развиваются:
Ú различные формы дистрофии;
Ú расстройства пластических процессов (по восстановлению поврежденных и синтезу новых клеток и внеклеточных структур;
Ú нарушения функционирования тканей, органов и организма в целом.
Сладж
Сладж—типовая форма патологии агрегатного состояния крови.
Сладж характеризуется адгезией, агрегацией и агглютинацией форменных элементов крови, обусловливающими сепарацию ее на плазму и плотные конгломераты из эритроцитов, лейкоцитов, тромбоцитов, а также образование тромбов.
Конгломераты и тромбы замедляют кровоток, обтурируют сосуды микроциркуляторного русла и приводят к нарушениям микрогемоциркуляции.
Причины сладжа:
Ú нарушения центральной гемодинамики (например, при сердечной недостаточности, венозном застое, ишемии, патологических формах артериальной гиперемии);
Ú повышение вязкости крови (например, в условиях гемоконцентрации, гиперпротеинемии, полицитемии);
Ú повреждение стенок микрососудов (при местных патологических процессах: воспалении, иммунопатологических состояниях, опухолевом росте и др.).
Патогенез сладжа
Основные звенья патогенеза сладжа представлены на рис. 23.56.
Ы ВЁРСТКА Вставить файл «ПФ_Рис.23.56» МС Ы
Рис. 23.56. Основные звенья патогенеза сладжа. ФЭК — форменные элементы крови.
Последствия сладжа
Сладж является причиной существенных нарушений микрогемоциркуляции и обмена веществ в тканях и органах, которые приводят к:
Ú внутрисосудистым расстройствам микроциркуляции (замедлению, вплоть до стаза; турбулентному току крови; открытию артериоловенулярных шунтов);
Ú нарушениям трансмурального перемещения форменных элементов крови, а также оттоку ее от тканей;
Ú расстройствам метаболизма в тканях и органах с развитием дистрофий и дисплазий.
В целом, совокупность указанных выше изменений приводит к развитию капилляро-трофической недостаточности.
Отсюда следует важный вывод о том, что феномен сладжа может быть:
Ú как причинойрасстройств микроциркуляции (в тех случаях, когда он развивается первично);
Ú так и следствиемвнутрисосудистых нарушений микроциркуляции (при первичном их развитии).
Глава 24
· Типовые формы патологии системы внешнего дыхания
Дыхание — обмен кислорода и углекислого газа – происходит путём их диффузии. Определяющим фактором этого процесса является разница в парциальном давлении газов.
Условно выделяют «внутреннее» (тканевое) и «внешнее» (альвеолярное) дыхание.
Тканевое дыхание— двунаправленная диффузия газов между просветом кровеносных капилляров и клетками (термин «тканевое дыхание» имеет и более широкое значение: утилизация O2 в процессе метаболизма клеток).
Внешнее дыхание— двунаправленная диффузия газов между альвеолами лёгких и кровью капилляров межальвеолярных перегородок через аэрогематический барьер.
Аппарат внешнего дыхания включает:
Ú дыхательные пути;
Ú респираторный отдел лёгких;
Ú грудную клетку(включая её костно-хрящевой каркас и нервно-мышечную систему);
Ú нервные центры регуляции дыхания.
Аппарат внешнего дыхания обеспечивает:
Ú альвеолярную вентиляцию (двунаправленную диффузию кислорода и углекислого через альвеолокапиллярную мембрану);
Ú перфузию ткани лёгких (кровоснабжение их).
Парциальные или комбинированные расстройства функционирования аппарата внешнего дыхания могут привести к дыхательной недостаточности.
Дыхательная недостаточность— состояние, характеризующееся развитием респираторной гипоксии и, как правило, гиперкапнии в результате нарушения газообменной функции лёгких.
Оценка функции внешнего дыхания
Для характеристики функции внешнего дыхания применяют показатели, позволяющие оценить функцию воздухоносных путей и респираторного отдела лёгких (дополнительные сведения о показателях функции внешнего дыхания приведёны в статьях «Ёмкость», «Объём» и «Скорость» приложения «Справочник терминов»).
При исследовании функции лёгких анализируют, главным образом, состояние показателей, характеризующих:
Ú лёгочные объёмы,
Ú объёмную скорость выдоха,
Ú диффузионную способность альвеолокапиллярной мембраны.
Лёгочные объёмыхарактеризуются статическими и динамическими показателями:
Ú показатели статических лёгочных объёмов отражают состояние эластических свойств ткани лёгких и грудной клетки;
Ú показатели динамических лёгочных объёмов характеризуют проходимость дыхательных путей.
Объёмная скорость выдоха представляет собой максимальную скорость движения воздушного потока в дыхательных путях при форсированном выдохе. Скорость воздушного потока зависит от состояния лёгочных объёмов и силы выдоха. Воздушный поток возрастает при увеличении силы выдоха, особенно в его начале (этот поток может составлять в течение первой секунды выдоха более 75% жизненной ёмкости лёгких). На объёмную скорость выдоха влияют также эластическая тяга ткани лёгкого и сопротивление дыхательных путей воздушному потоку.
Диффузионная ёмкость, или диффузионная способность (Дс) аэрогематического барьера—показатель эффективности транспорта определенного газа из альвеол в кровь капилляров лёгких.
Спирометрия (спирография) и ее показатели
Спирометрия (спирография) представляет собой измерение ЖЁЛ и других лёгочных объёмов с помощью спирографа (прибора для непрерывной графической регистрации изменения объёмов вдыхаемого и выдыхаемого воздуха).
Спирограмма регистрируется в момент максимально глубокого вдоха и спокойного выдоха. После этого вдох и выдох записывают повторно, но с максимальным усилием.
Показатели спирометрии позволяют дифференцировать обструктивные и рестриктивные расстройства альвеолярной вентиляции, оценивать степень дыхательной недостаточности и её динамику при лечении.
Многие показатели спирограммы выражают в относительных величинах (чаще в %) от их средних значений в популяции (учитывается пол, возраст, рост). Нормальным считают колебания показателя в диапазоне от 80 до 120%.
· Дыхательный объём (ДО) — объём воздуха, поступающий в лёгкие за один вдох при спокойном дыхании (норма 500–800 мл). Часть ДО, участвующая в газообмене, носит название альвеолярный объём (АО); остаток — около 30% от ДО — это анатомически мёртвоепространство,иливредныйобъём.
· ЖЁЛ— максимальный объём воздуха, изгоняемый из лёгких вслед за максимальным вдохом. ЖЁЛ прогрессирующе снижается при рестриктивных болезнях лёгких. В связи с этим, ЖЕЛ, в сочетании с показателем диффузионной ёмкостью легких, помогает оценить течение болезни и эффективностью ее лечения у пациентов с рестриктивной патологией.
· Форсированная жизненная ёмкость (ФЖЁЛ) оценивается аналогично ЖЁЛ, за исключением того, что дыхание при этом производится с максимально возможной силой и скоростью. Форсированный выдох сопровождается сужением дыхательных путей, замедлением его скорости.
· Объём форсированного выдоха за 1 секунду (ОФВ1) — объём воздуха, изгоняемый с максимальным усилием из лёгких в течение первой секунды выдоха после глубокого вдоха, т.е. это часть ФЖЁЛ, выдыхаемая за первую секунду. ОФВ1 отражает состояние крупных дыхательных путей и часто выражается в процентах от ЖЁЛ (нормальное значение ОФВ1 = 75% ЖЁЛ).
· ОФВ1/ФЖЁЛ — отношение ОФВ1 к ФЖЁЛ (индекс Тиффно), выраженное в процентах (в норме больше или равно 70%). Значение ОФВ1/ФЖЁЛ прямо пропорционально силе выдоха. Этот показатель важен для выявления обструктивных нарушений дыхания, а также для диагностики рестриктивных его расстройств. Снижение только ОФВ1 (ОФВ1/ФЖЁЛ <70%) свидетельствует об обструкции; снижение обоих показателей (ОФВ1/ФЖЁЛ ³70%) указывает на рестриктивную патологию.
· Средняя объёмная скорость выдоха (СОС25%–75%) — скорость потока форсированного выдоха в его середине (т.е. между 25% и 75% ФЖЁЛ); иначе его обозначают как максимальный поток середины выдоха. СОС25%–75% отражает состояние мелких дыхательных путей. Он более информативен, чем ОФВ1 при выявлении ранних обструктивных нарушений.
· Пик объёмной скорости выдоха (мощность выдоха) — максимальная объёмная скорость, которую исследуемый может развить при форсированном выдохе. Это показатель проходимости дыхательных путей на уровне трахеи и крупных бронхов. Зависит от мышечного усилия пациента.
Другие лёгочные объёмы
Получение других показателей легочных объемов требует применения не только спирометрии, но и теста с разведением гелия в легочном воздухе (позволяющего определить объём газа в лёгких).
· Общая ёмкость лёгких (ОЁЛ) — объём воздуха, содержащегося в лёгких на высоте максимального вдоха.
· Функциональная остаточная ёмкость (ФОЁ) — объём воздуха, остающийся в лёгких в конце нормального выдоха. Отражает состояние покоя лёгких и грудной стенки (объём лёгких в условиях равновесия эластической тяги лёгких, направленной внутрь, и тяги грудной клетки, направленной наружу. ФОЁ представлена двумя компонентами:
Ú резервным объёмом выдоха (РОвыд) — часть ФОЁ, которая может быть изгнана из лёгких при максимально усиленном выдохе;
Ú остаточным объёмом лёгких (ООЛ) — объём воздуха, остающийся в лёгких после максимально усиленного выдоха (в норме 25–30% от ФОЁ).
· Соотношения лёгочных объёмов:
ОЁЛ = ЖЁЛ + ООЛ
ООЛ = ФОЁ – РОвыд
Исследование других функций лёгких
· Диффузионная способность (диффузионная ёмкость, Дс) лёгких по окиси углерода (ДсCO) отражает состояние альвеолярно-капиллярной мембраны: аэрогематического барьера. ДсCO определяют измерением количества окиси углерода (CO), поступившей из альвеолярного воздуха в кровь лёгочных капилляров после того, как пациент вдохнул известное количество СО (0,1%). Выражают ДсCO в мл/мин/мм рт.ст.
· Кривая податливости (растяжимости) легких. Эластичность лёгких определяет соотношение изменений лёгочных объёмов и транспульмонального давления (разность давления в альвеолах и в плевральной полости). Для растяжения лёгкого до заданного объёма необходимо определённое усилие, складывающееся из эластической тяги лёгкого, направленной внутрь, и эластической тяги грудной стенки, направленной наружу. В норме в состоянии покоя на момент конца выдоха (т.е. в положении ФОЁ) эластическая тяга лёгкого полностью сбалансирована эластической тягой грудной стенки. При полном вдохе (т.е. при ОЁЛ) лёгкие достигают своей максимальной эластической тяги. При полном выдохе (т.е. при резервном объёме выдоха) грудная стенка достигает своей максимальной эластической тяги. Зависимость транспульмонального давления от объёма лёгких отображается в виде кривой растяжимости лёгких. Податливость, или растяжимость (C) определяется по наклону кривой давление-объём (P—V) над уровнем дыхательного объёма:
C = V/P (в норме 200 мл/см Н20)
Потеря эластической тяги лёгкого (например,
при эмфиземе) увеличивает растяжимость, смещая кривую податливости влево. Увеличение эластической тяги лёгкого (например
,
при рестриктивных заболеваниях лёгких, таких как идиопатический лёгочный фиброз) снижает растяжимость, смещая кривую податливости вниз и вправо.
· Сопротивление дыхательных путей (СДП). Этот показатель отражает состояние крупных дыхательных путей, поскольку 80–90% сопротивления воздушному потоку создают именно они. СДП обычно определяют по динамическим лёгочным объёмам и объёмным скоростям выдоха. Величины СДП повышены при обструктивных болезнях лёгких и снижены при рестриктивных лёгочных заболеваниях.
Спирометрические признаки дыхательной недостаточности
Обструктивные расстройства альвеолярной вентиляции
Объёмные скорости. При альвеолярной гиповентиляции вследствие обструкции дыхательных путей показатель ОФВ1/ФЖЁЛ снижается (менее 70%). Этот показатель тесно связан со временем выдоха. Однако, даже при значительной обструкции периферических дыхательных путей ОФВ1/ФЖЁЛ может быть в пределах средней физиологической нормы. В такой ситуации обструкцию дыхательных путей можно выявить по снижению СОС25%–75% (до 60% или ниже от должной величины).
Лёгочные объёмы. Изменения дыхательных объёмов лёгких могут встречаться при умеренной и тяжёлой обструкции дыхательных путей. Измерение объёмов лёгких помогает распознать перерастяжение лёгких вследствие преждевременного закрытия дыхательных путей (экспираторного коллапса бронхов).
Известно, что во время форсированного выдоха дистальные отделы дыхательных путей закрываются раньше, чем изгоняется воздух, что приводит к перерастяжению легких, вызывающему увеличение ФОЁ, ООЛ и ООЛ/ЖЁЛ.
При нарушениях проходимости мелких дыхательных путей в них образуются «воздушные ловушки», увеличивающие ООЛ, тогда как ФОЁ и ОФВ1 остаются нормальными.
При эмфиземе легких разрушение стенок альвеол и потеря лёгкими эластической тяги вызывают увеличение ОЁЛ.
Рестриктивные расстройства альвеолярной вентиляции
Объёмные скорости. ОФВ1/ФЖЁЛ и СОС25–75% при рестриктивной форме гиповентиляции легких могут быть нормальными или повышенными вследствие увеличенной тяги стенок дыхательных путей.
Лёгочные объёмы
Наиболее информативным признаком рестриктивных нарушений вентиляции легких является снижение ЖЁЛ и ОЁЛ.
Ригидность лёгких при их рестриктивных поражениях увеличивает эластическую тягу лёгких и тем самым снижает ФОЁ.
Ригидность грудной стенки (например,при кифосколиозе) уменьшает лёгочные объёмы, поскольку ограничивает расширение лёгких.
Растяжимость лёгких также ограничена вследствие увеличения их эластической тяги.
Сопротивление дыхательных путей (СДП) воздушному потоку снижено, так как благодаря эластическим силам дыхательные пути расширены на уровне любых лёгочных объёмов.
Газы артериальной крови
Парциальное давление кислорода (рО2) и двуокиси углерода (pCO2), а также pH — важные параметры для оценки функции лёгких. Они указывают на состояние газообмена между лёгкими и кровью.
рО2. При отсутствии патологии рО2 снижается с возрастом вследствие утраты лёгкими эластичности (в норме оно составляет 90 мм рт.ст. в 20 лет и около 70 мм рт.ст. к 70 годам).
Уменьшение рО2 ниже нормы свидетельствует о гипоксемии, однако насыщение тканей кислородом при этом существенно не снижается до тех пор, пока рО2 не упадёт ниже 60 мм рт.ст.
рСО2. Отражает состояние альвеолярной вентиляции (в норме 35–45 мм рт.ст.). Гиперкапния (респираторный ацидоз, высокое рСО2) свидетельствует о гиповентиляции.
pH. Сопоставление артериального pH (в норме 7,35–7,45) с рСО2 дает возможность отличить респираторные нарушения КОС от метаболических. Например,
если раСО2 и pH обратно пропорциональны (один показатель снижается при увеличении другого), расстройство КОС имеет респираторную природу.
Нарушения вентиляционно-перфузионного (V/Q) соотношения
Оптимальные вентиляция легких и лёгочный кровоток обеспечивают достаточную доставку кислорода к тканям и адекватную элиминацию двуокиси углерода из организма.
В среднем соотношение V/Q составляет 0,8 (в норме допускается физиологический дисбаланс V/Q, обусловленный «сбросом» в лёгких примерно 2% объема артериальной крови в венозную через артерио-венозные шунты без газообмена).
Предыдущая24Следующая
Разрушение сосудистой стенки
Нарушение целостности стенки сосуда может возникать как при патологических состояниях всего организма (ацидоз, гипоксия), так и при непосредственном повреждении стенки сосуда биологически активными агентами. В роли таких агентов выступают медиаторы воспаления при васкулитах (воспалении сосудистой стенки).
Если повреждение прогрессирует, отмечается просачивание (диапедез) эритроцитов из крови в окружающие ткани и образование кровоизлияний.
Интраваскулярные (внутрисосудистые) расстройства
Основные внутрисосудистые нарушения указаны на рис. 1
Внутрисосудистые нарушения микроциркуляции
Замедление тока крови и/или лимфы избыточное ускорение тока крови и/или лимфы Нарушение турбулентности тока крови и /или лимфы. Чрезмерное увеличение юкстакапилляр-ного тока крови
Рис. 1 – Внутрисосудистые нарушения микроциркуляции
Причины замедления тока крови и/или лимфы:
- расстройства гемо‑ и лимфодинамики (например, при сердечной недостаточности, венозной гиперемии, ишемии, лимфорее);
- увеличение вязкости крови(например, в результате гемоконцентрации при длительной рвоте, диарее, плазморрагии при ожогах, полицитемии, гиперпротеинемии, внутрисосудистом диссеменированом свёртывании крови);
- уменьшение просвета микрососудов(вследствие сдавления их опухолью, отёчной тканью, образования в них тромбов, попадания эмбола, набухания или гиперплазии эндотелиальных клеток, образования атеросклеротической бляшки и т.п.).
Причины избыточного ускорения тока крови и/или лимфы:
- нарушения гемо- и/или лимфодинамики (например, при патологической артериальной гиперемии или сбросе артериальной крови в венозное русло через артериоловенулярные шунты);
- снижение вязкости крови (при гемодилюции, гипопротеинемии, почечной недостаточности, панцитопении.
https://www.youtube.com/watch?v=ytadvertiseru
Причины турбулентности тока крови:
- повреждение стенок микрососудов и/или нарушение гладкости их (при васкулитах, гиперплазии клеток эндотелия, артериосклерозе, фиброзных изменениях в сосудистой стенке и т.п.).
- изменения агрегатного состояния крови (например, при формировании пристеночных микротромбов, нарушающих ламинарный ток крови).
Чрезмерное увеличение юкстакапиллярного тока крови
Развивается при открытии артерио-венозных и артериоло-венулярных шунтов и проявляется сбросом избытка крови из артерий и артериол в вены и венулы, минуя капиллярную сеть микроциркуляторного русла. Причины:
- спазм артериол и закрытие прекапиллярных сфинктеров при значительном увеличении уровня катехоламинов в крови (при гиперкатехоламиновом кризе у пациентов с опухолью мозгового вещества надпочечников — феохромоцитоме);
- при чрезмерном повышении тонуса симпатической нервной системы (при стрессе).
Трансмуральные нарушения микроциркуляции делят на 2 подгруппы:
- изменения тока жидкости;
- движения форменных элементов крови.
При патологии часто наблюдается увеличение или уменьшение интенсивности перехода веществ через сосудистую стенку не только вследствие изменения интенсивности кровотока, но и в результате истинного нарушения сосудистой проницаемости, которое сопровождается изменением структуры стенки сосудов обмена.
Сосуды обмена характеризуются двумя основными феноменами — осуществление движения крови и способность пропускать в направлении КРОВЬ—ТКАНЬ и обратно воду, растворимые газы и крупномолекулярные (белковые) вещества. Морфологической основой проницаемости является эндотелий и базальная мембрана. Эти образования, а также периваскулярная соединительная ткань образуют гистогематический барьер.
Механизм перехода вещества через сосудистую стенку может быть активный и пассивный.
Активный осуществляется против концентрационного и электрохимического градиентов, и для его осуществления требуется достаточно большое количество энергии (белки и другие макромолекулы).
Пассивный транспорт (перенос воды, растворимых газов и низкомолекулярных веществ) транспорт осуществляется в соответствии с концентрационными и электрохимическими градиентами.
Внесосудистые нарушения
Патологические процессы в организме могут влиять на сосуды микроциркуляции двумя путями:
- Реакцией тканевых базофилов, которые выбрасывают в окружающую среду биологически активные агенты и ферменты, непосредственно влияющие на сосуд и сгущающие кровь в сосудах.
- Нарушением транспорта тканевой жидкости.
Таким образом, микроциркуляция — это сложная система, которая находится в постоянном взаимодействии со всем организмом. Необходимо знать не только основные виды ее нарушений, но и методы диагностики и лечения этих заболеваний.
Опасны ли микроциркуляторные нарушения?
Несомненно, многие нарушения микроциркуляции опасны для здоровья и даже жизни больного, в первую очередь если они возникают остро. Так, нарушения кровотока в мелких сосудах сердечной мышцы, возникшие при остром коронарном тромбозе, приводят к выраженной ишемии миокарда, а через несколько минут или часов – к некрозу (отмиранию) клеток сердечной мышцы – развивается острый инфаркт миокарда. Чем обширнее зона поражения, тем неблагоприятнее прогноз.
При остром тромбозе бедренных артерий и вен любое промедление в плане медикаментозного и оперативного вмешательства может привести к потере конечности.
То же самое касается и лиц с диабетической ангиопатией и синдромом диабетической стопы. Такие пациенты должны быть обучены правильному уходу за своими стопами, чтобы не лишиться ног при развитии гнойной инфекции или гангрены стопы.
В случае длительно существующих процессов в организме, например, при нарушениях микроциркуляции в почках и в головном мозге при гипертонии, нарушение функции органа, конечно, есть, но острой угрозы для жизни не возникает.
Возрастное нарушения кровотока в микрососудах кожи вообще не несет никакой опасности для жизни и здоровья, а вызывает только эстетические проблемы.
Нарушение микрогемодинамики: диагностика
В зависимости от пораженного органа могут использоваться различные методы инструментальной диагностики, которые косвенно могут указать на наличие нарушений микроциркуляции через патологию внутреннего органа:
- электрокардиограмма, эхокардиограмма, коронарография (миокард);
- УЗИ сосудов головы и шеи, доплерография, ангиография (головной мозг);
- УЗИ, скорость клубочковой фильтрации, экскреторная урография (почки);
- УЗИ, ангиография, капилляроскопия, флебография (нижние конечности).
Нарушение микрогемодинамики: лечение
Для улучшения микроциркуляции применяется группа препаратов, называемая ангиопротекторами. Это высокоэффективные лекарственные средства, улучшающие ток крови по сосудам и восстанавливающие сам сосуд. Их основные свойства таковы:
- уменьшение спазма артерий;
- обеспечение проходимости сосуда;
- улучшение реологии (вязкости) крови;
- укрепление сосудистой стенки;
- противоотечный эффект;
- улучшение метаболизма, то есть обмена веществ, в сосудистой стенке.
К основным препаратам, улучшающим микроциркуляцию, относятся следующие:
- «Троксевазин»;
- «Детралекс»;
- «Трентал»;
- «Эмоксипин»;
- «L-лизина эсцинат».
Можно сделать вывод, что, несмотря, на свой небольшой размер и диаметр, сосуды микрогемодинамики выполняют очень важную функцию в организме. Поэтому микроциркуляция — это самодостаточная система организма, состоянию которой можно и нужно уделять особое внимание.
Профилактика нарушения кровообращения
В большинстве диагностированных случаев проблемы с сосудами появляются при неправильном образе жизни. Для поддержания тонуса и улучшения состояния сердечно-сосудистой системы врачи рекомендуют:
Обязательно заниматься спортом, уделяя активным кардионагрузкам до 150 минут каждую неделю. Пользу приносит велотренажер, быстрая ходьба, танцы и плавание. Для тонизирования сосудов применять контрастные обливания конечностей или всего тела, иногда принимать горячие ванны с температурой 40° С. Отказаться от вредных привычек. Никотин вызывает сильные спазмы капилляров, провоцирует их ломкость, сужение, усиливает нарушение кровообращения. Правильно питаться, не забывать про полезные насыщенные жиры, аминокислоты Омега-3 и Омега-6. кальций, калий и селен. При изменении кровообращения нарушения затрагивают весь организм. На начальной стадии проблемы устраняются с помощью лечебной физкультуры, специальной диеты, контроля уровня холестерина и сахара в крови. При позднем обращении придется бороться с хроническими болезнями и серьезными патологиями.