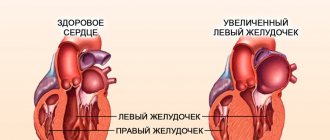
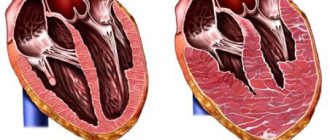
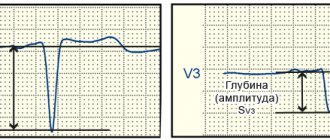
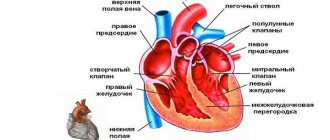
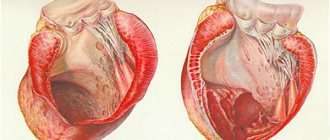
Патофизиология
Развитие истинной аневризмы левого желудочка протекает в две основных фазы: ранней дилатации и позднего ремоделирования. Истинная аневризма левого желудочка (по крайней мере, в 88%) развивается обычно после трансмурального инфаркта миокарда вследствие тромбоза передней межжелудочковой ветви ( ПМЖВ) и недостаточного развития коллатерального кровообращения.
Фаза ранней дилатации у 50% пациентов начинается с момента инфаркта миокарда в течение 48 часов. У остальных пациентов формирования аневризмы происходит в течение 2 недель после инфаркта миокарда. В течение нескольких дней внутренняя поверхность развивающейся аневризмы теряет трабекулярность и становится гладкой, у 50% пациентов формируется тромб левого желудочка.
На 2-3 сутки в зону инфаркта происходит миграция лейкоцитов, что приводит к лизису некротических миоцитов на 5-10 день после инфаркта. В результате разрушения коллагена и миоцитов прочность стенки миокарда к этому времени значительно снижается и возможен разрыв миокарда. Сохранение гибернирующего миокарда в периинфарктной зоне обязательное условие предотвращения развития истинной аневризмы левого желудочка.
Потеря систолической активности в инфарцированной зоне при сохранении сократительной способности в окружающем миокарде вызывает систолическое выпячивание утончение региона миокарда. Согласно закону Лапласа (T = Pr/2h), при постоянном давлении в левом желудочке (P), увеличении радиуса искривления (r) и уменьшении толщины стенки левого желудочка (h) в инфарктной зоне увеличивается напряжение стенки (T).
По отношению к нормальному поврежденный (инфарцированный) миокард более пластичен и подвержен деформации. Таким образом, увеличенное систолическое и диастолическое напряжение стенки левого желудочка приводит к прогрессивному расширению инфарктной зоны, пока формирование рубца не уменьшает пластичность области аневризмы.
Вследствие роста диастолического напряжения и преднагрузки, а также увеличения уровня эндогенных катехоламинов, непораженные области миокарда вынуждены развивать усиление сокращения, что приводит к гипертрофии миокарда. Это в свою очередь вызывает рост потребления кислорода здоровыми отделами миокарда и левого желудочка в целом.
В дополнение к этому при формировании аневризмы происходит снижение ударного объема, так как часть его выбрасывается не в аорту, а в аневризму. Чистая механическая эффективность левого желудочка (внешняя ударная работа минус миокардиальное потребление кислорода) снижается, уменьшая внешнюю ударную работу и еще более увеличивая миокардиальное потребление кислорода.
Аневризма левого желудочка вызывает не только систолическую, но и диастолическую дисфункцию желудочка. Диастолическая дисфункция является следствием увеличенной жесткости фиброзной аневризматической стенки, которая препятствует диастолическому заполнению и увеличивает конечно-диастолическое давление левого желудочка.
Начинается спустя 2-4 недели после инфаркта миокарда, когда появляется высоко васкуляризированная грануляционная ткань, которая замещается через 6-8 недель волокнистой фиброзной тканью. Аритмии, типа желудочковой тахикардии могут развиться в любое время развития желудочковой аневризмы, так как в области периинфарктной зоны развиваются микроочаги re entry.
Терапия нитратами в течение только 2 недель после инфаркта не предотвращает формирование аневризмы. До настоящего времени неясна роль ингибиторов ангиотензин-конвертирующего фермента поскольку они подавляют развитие желудочковой гипертрофии. Реваскуляризация миокарда улучшая коронарную перфузию и перемещение фибробластов в инфарктную область миокарда, является хорошим профилактическим фактором развития аневризм левого желудочка. Применение стериодов, наоборот, может увеличить вероятность формирования аневризмы.
Несмотря на значительные достижения в молекулярной, биомеханической, генетической, нейро-гуморальной и фармакологической областях, понимания строения и функции кардиомиоцита, не следует, однако, забывать тот фундаментальный факт, что высокоспециализированные клетки могут эффективно функционировать лишь в окружении коллагенового остова, который не только располагает их друг относительно друга, но и связывает кардиомиоциты.
Таким образом, создается совокупность морфологических единиц, способных к генерации силы в пределах определенного структурного расположения – мышечной ленты, и к трансформации простого укорочения сократительных единиц в механически эффективное сокращение и расслабление спиральной структуры целого миокарда левого желудочка сердца.
Любое улучшение функции миоцитов в отсутствие адекватного коллагенового каркаса, и, соответственно, улучшение систолической и диастолической функции всего сердца, невозможно. Существует общепринятое мнение, что коллаген играет важную роль в поддержке размеров и формы сердца, а также в постинфарктном ремоделировании.
Он составляет от 1% до 4% всех сердечных белков. Коллагеновые волокна – это надмолекулярные образования, которые состоят из молекул коллагена, уложенных зигзагообразно и перекрещенных для увеличения прочности. Внеклеточный матрикс представлен вязкоупругим окружением из коллагена типа I и III, который связывает миоциты, определяет взаимодействие между миофиламентами и поддерживает взаимоотношение капилляров и миоцитов.
Коллагеновый остов состоит из сети миофибрилл и межклеточных «распорок», которые связывают соседние миоциты, что позволяет миофибриллам оптимизировать развитие мышечного усилия, распределить его внутри желудочковых стенок и предотвратить деформацию саркомеров. Внутри вышеописанной структуры межклеточное пространство заполнено протеогликанами.
Ремоделирование миокарда представляет адаптивный ответ сердца на длительное воздействие физиологических и патогенных факторов. При этом изменяется структура миоцитов и внеклеточного матрикса. Уменьшение перекрестных связей миокардиального коллагена было показано на животных моделях. Так как структурная поддержка, которая обеспечивается фибриллярным внутриклеточным коллагеном, является важной детерминантой формы миоцита и распределения масс, а также составляющей превращения сокращения миоцита в общий сердечный выброс, то ее потеря, из-за деградации зрелого коллагена с заменой его на вновь синтезированный со сниженным количеством перекрестных связей, может непосредственно влиять на систолическую дисфункцию и расширение полостей сердца.
Изменения внеклеточного матрикса необходимы для формирования нового устройства камер сердца. Развитию фиброза, а именно увеличения количества белков внеклеточного матрикса – коллагена I и III типов, обязательно должна предшествовать деструкция коллагеновой сети. Коллаген I типа принимает участие в формировании внеклеточного матрикса фазу позднего ремоделирования, в то время как коллаген III типа – в фазу ранней экспансии.
Всякое изменение внеклеточного матрикса по сути своей означает нарушение баланса между скоростями синтеза и распада белка. Будучи организованным в фибриллярную форму, внеклеточный коллаген является крайне устойчивым к разрушению протеазами, за исключением специфических коллагеназ – матриксных металлопротеиназ (ММП), основным источникам которых в сердце являются фибробласты.
Изменения в структуре коллагена, его распределение в процессе ремоделирования зависит от регуляции ММП на трех уровнях: транскрипции, активации и ингибирования тканевыми ингибиторами металлопротеиназ (TИMMП). TИMMП представляют собой низкомолекулярные белки, которые имеют высокое сродство к каталитическому домену ММП.
Таким образом TИMMП нейтрализуют деградацию коллагена. Гены, кодирующие ММП и ТИММП, расположены совместно и совместно же экспрессируются. Данная система индукции/активации ММП была найдена в сарколемме миоцитов. Она некорректно работает у пациентов с ишемической кардиомиопатией. Коллагеназы могут быть активированы посредством множества механизмов, включая фактор некроза опухолей – альфа (альфа-ФНО), свободные радикалы, инсулино-подобный фактор роста-1, трансформирующий фактор роста-1, который стимулирует пролиферацию фибробластов, катехоламины – то есть все факторы, которые имеют место при ишемии.
Одним из эндогенных активаторов ММП может являться химаза (единственный фермент в ткани миокарда, конвертирующий ангиотензин I в ангиотензин II), повышенный уровень которой определялся при состояниях перегрузки давлением или объемом. Один из донаторов сульфгидрильных групп – окисленный глутатион, встречающийся в зоне миокардиальной ишемии, – тоже активирует латентные коллагеназы и вызывает быстрое разрушение коллагеновых мостиков в «ошеломленном» миокарде и в зоне инфаркта в течение 2-3 часов после окклюзии артерии, когда еще не развивается воспалительный инфильтрат.
Предлагаем ознакомиться: Субэндокардиальный инфаркт миокарда — что это такое
Местный синтез альдостерона миофибробластами вызывает аутокринную стимуляцию системы ренин-ангиотензин-альдостерон. Вместе с ангиотензином II и предсердным натрийуритическим фактором альдостерон стимулирует трансляцию m-РНК коллагена I и III типов.
Еще одним моментом, требующего пристального внимания, является возможная обратимость ремоделирования внеклеточного матрикса. Недавние исследования показали, что длительное использование систем вспомогательного кровообращения обращает вспять сократительную дисфункцию и влияет на экспрессию генов на конечной стадии хронической сердечной недостаточности.
Также было отмечено улучшение эхокардиографических параметров. Таким образом становиться понятно, что прекращение действия фактора, нагрузки, запускающего патологическое ремоделирование и развитие сердечной недостаточности, может привести к обратному развитию структурных и архитектурных изменений. Так как основой активации и модуляции внутриклеточных цепных реакций является механический стресс, то уменьшение последнего, соответственно, достижение контроля над экспрессией и активностью ММП, возможно лишь при использовании объем-редуцирующей хирургии и модификации желудочковой геометрии.
Что такое гипертрофия миокарда
Это аутосомно-доминантное заболевание, предает наследственные признаки мутации генов, поражает сердце. Для него характерно увеличение толщины стенок желудочков. Гипертрофическая кардиомиопатия (ГКМП) имеет классификационный код по МКБ 10 №142. Болезнь чаще бывает асимметричной, поражению больше подвержен левый желудочек сердца. При этом происходит:
- хаотичное расположение мышечных волокон;
- поражение мелких коронарных сосудов;
- образование участков фиброза;
- обструкция кровотока – препятствие выбросу крови из предсердия из-за смещения митрального клапана.
При больших нагрузках на миокард, вызванных заболеваниями, спортом, или вредными привычками, начинается защитная реакция организма. Сердцу необходимо справиться с завышенными объемами работы без увеличения нагрузки на единицу массы. Начинает происходить компенсация:
- усиление выработки белка;
- гиперплазия – рост числа клеток;
- увеличение мышечной массы миокарда;
- утолщение стенки.
Патологическая гипертрофия миокарда
При длительной работе миокарда под нагрузками, которые постоянно повышены, возникает патологическая форма ГКМП. Гипертрофированное сердце вынуждено приспособиться к новым условиям. Утолщение миокарда происходит стремительными темпами. При таком положении:
- отстает рост капилляров и нервов;
- нарушается кровоснабжение;
- меняется влияние нервной ткани на обменные процессы;
- изнашиваются структуры миокарда;
- меняется соотношение размеров миокарда;
- возникает систолическая, диастолическая дисфункция;
- нарушается реполяризация.
Гипертрофия миокарда у спортсменов
Незаметно происходит аномальное развитие миокарда – гипертрофия – у спортсменов. При высоких физических нагрузках сердце перекачивает большие объемы крови, а мышцы, приспосабливаясь к таким условиям, увеличиваются в размерах. Гипертрофия становится опасной, провоцирует инсульт, инфаркт, внезапную остановку сердца, при отсутствии жалоб и симптомов. Нельзя резко бросать тренировки, чтобы не возникли осложнения.
Спортивная гипертрофия миокарда имеет 3 вида:
- эксцентрическая – мышцы изменяются пропорционально – характерна для динамических занятий – плавание, лыж, бег на большие дистанции;
- концентрическая гипертрофия – остается без перемен полость желудочков, увеличивается миокард – отмечается при игровых и статических видах;
- смешанная – присуща занятиям с одновременным использованием неподвижности и динамики – гребля, велосипед, коньки.
Гипертрофия миокарда у ребенка
Не исключено появление патологий миокарда с момента рождения. Диагностика в таком возрасте затруднена. Часто наблюдают гипертрофические изменения миокарда в подростковом периоде, когда активно растут клетки кардиомиоцита. Утолщение передней и задней стенок происходит до 18 лет, затем прекращается. Гипертрофия желудочков у ребенка не считается отдельной болезнью – это проявление многочисленных недугов. Дети с ГКМП часто имеют:
- порок сердца;
- дистрофию миокарда;
- гипертоническую болезнь;
- стенокардию.
Естественное течение
Относительно новые исследования выявили 47-70% 5-летнюю выживаемость пациентов с аневризмами левого желудочка. Причины смерти включают аритмию в 44%, остановку сердца – 33%, инфаркт миокарда – 11% и несердечные причины – 22%.
Факторами, влияющим на выживаемость являются возраст, степень коронарной болезни, продолжительность стенокардии до предшествующего инфаркта, ишемическая митральная недостаточность, желудочковые аритмии, размер аневризмы, сократительной функции жизнеспособного миокарда, КДД левого желудочка. Раннее развитие аневризмы в течение 48 часов после инфаркта также уменьшает выживаемость.
Риск томбоэмболии для пациентов с аневризмами низок (0,35% пациенто-лет), и постоянный прием антикоагулянтов обычно не рекомендуется. Однако у 19% пациентов с видимыми эхокардиографически тромбами после инфаркта миокарда отмечены эпизоды тромбоэмболии. Мерцательная аритмия и большой размер аневризмы – дополнительные факторы риска томбоэмболии.
Разрыв хронических псевдоаневризм левого желудочка встречается реже, чем можно было ожидать. Разрыв левых желудочковых псевдоаневризм может быть наиболее вероятным в острой фазе инфаркта миокарда или при их большом размере. Желудочковые псевдоаневризмы имеют тенденцию вести себя подобно истинным аневризмам.
Клинические признаки
Признаки гипертрофии левого желудочка долгое время отсутствуют. Симптомы появляются только тогда, когда человек не может компенсировать возникшие изменения кровообращения. Концентрическая гипертрофия миокарда левого желудочка может проявляться следующими симптомами:
- головокружением;
- болью в сердце;
- одышкой;
- отеками нижних конечностей;
- нарушением сна;
- снижением трудоспособности;
- слабостью;
- ощущением замирания сердца;
- обмороками;
- лабильностью артериального давления;
- нарушением сердечного ритма по типу мерцательной аритмии или экстрасистолии.
У большинства таких больных появляется боль в области сердца по типу стенокардии. Часто наблюдается повышение кровяного давления. Типичным проявлением гипертрофии миокарда является одышка. На ранних стадиях она беспокоит при работе, а затем появляется в покое. В тяжелых случаях развивается сердечная астма. Многих больных беспокоят периодические приступы удушья.
Возможен акроцианоз (посинение пальцев, носа, губ). Все эти симптомы обусловлены основным заболеванием, приведшим к гипертрофии левого желудочка. Если причиной является гипертрофическая кардиомиопатия, то исходом такой патологии может стать ненасильственная смерть вследствие внезапной остановки сердца.
Гипокинезия, как основной синдром паркинсонизма
Гипокинетический синдром проявляется при паркинсонизме как в конечностях, так и в теле.
Это все вышеназванные разновидности расстройства двигательных функций на фоне пластической гипертонии мышц, включая парадоксальные движения, паллидарный тремор, микрографический почерк, феномены «позы восковой куклы» и «зубчатого колеса», при ходьбе – заносы тела в сторону с падениями, паркинсоновское топтание на месте, ахейрокинез.
Характерна поза с наклоном головы и корпуса вперёд с касанием груди подбородком, с руками, прижатыми к корпусу, согнутыми в лучезапястных и локтевых сочленениях, со сгибанием пальцев в пястно-фаланговых и разгибанием в межфаланговых сочленениях, с оппозицией I пальца остальным пальцам кисти, с ногами, слегка приведенными и полусогнутыми в коленях.
Гипертонус шеи заставляет больного разворачиваться на зов всем туловищем либо максимально поворачивать глаза, при этом голова остается неподвижной.
Расстроена также моторика мышц, обеспечивающих живость мимики, отсюда маскообразность лица (гипомимия) с практически немигающим взглядом, монотонность тихого голос ввиду затруднений с артикуляцией речи (гипофония).
Особенностью гипокинезии при паркинсонизме (помимо сохранения мускульной силы) является ее сочетание с высокой степенью ригидности мышц.
В отличие от спастичности ригидность проявляется:
- положительным симптомом «свинцовой трубочки» (равномерностью мышечного воскообразного сопротивления, как при сгибании свинцовой трубочки) – спастичная мускулатура отвечает феноменом отдачи и «складного ножа»;
- неизменностью сухожильных рефлексов – при спастичности они возрастают.
Иллюстрацией ригидности служит симптом «зубчатого колеса», не свойственный спастичности.
Схожесть двигательных расстройств делает больных паркинсонизмом схожими друг с другом, отличающимися только выражением взгляда.
Последовательность деформирования при акинезии плода включает в себя тип акинезии, которая вызывает сочетание патологии в утробе матери, когда ребенок развивается. Примеры таких симптомов:
- Различные контрактуры;
- Лицевые аномалии;
- Внутриматочное ограничение роста;
- Гипоплазия (недоразвитие) легких.
Примерно 30% детей с последовательностью деформации при акинезии плода рождаются мертвыми. Другие не могут долго жить из-за проблем, связанных с гипоплазией легких.
Механизм развития
Умеренная гипертрофия левого желудочка очень часто протекает бессимптомно и в большинстве случаев обнаруживается случайно после электрокардиографии.
Как лечить гипертрофию левого желудочка, зависит от степени сложности протекания и особенностей первоначального заболевания, на фоне которого возник данный патологический синдром.
Начатое этиологическое исследование не выявило сердечной истории в семье или подобных случаях. Эхокардиография была нормальной как у родителей, так и у близнецов. Кариотип ребенка был нормальным. Была проведена серия биологических анализов и нормализована: гемоглобин крови, определение общего количества карнитина и свободного карнитина в крови, определение катехоламинов мочи, анализ активности глюкозидазы и анализ креатинкиназы. Анатомопатологическое исследование биопсии мышц также было нормальным.
В ходе курса наблюдалось четкое клиническое улучшение с регрессией сердечного ропота и адекватного увеличения веса. Затем было принято решение прекратить исследования и следить за ребенком, эхокардиографическая проверка в течение 1, 3 и 6 месяцев была без аномалий со строго нормальным ростом.
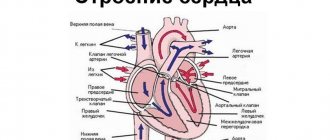
При отсутствии физиологических нарушений сердце выполняет так называемую функцию насоса, с огромной силой выталкивая кровь в аорту. После чего кровь поступает ко всем органам. В момент расслабления левого желудочка происходит поступление порции крови из левого предсердия. Процесс поступления крови непрерывен, а ее количества достаточно для обеспечения полноценного газообмена во всем организме.
После обзора литературы этиология, используемая для этой кратковременной неонатальной гипертрофии сердца, была вторичной реакцией на введение кортикостероидов, чтобы ускорить созревание легких. Потенциальный эффект катехолинического выделения матери во время токсикоза беременности не исключено.
Неонатальная гипертрофическая кардиомиопатия — редкая сущность, описанная в литературе как изолированные клинические случаи, определяемые асимметричной гипертрофией левого желудочка, преимущественно септальной с нормальной систолической функцией. Этот субъект часто проявляет себя в хорошо переносимой клинической форме быстрой регрессии, в отличие от форм, связанных с диабетом по материнской линии, где реституция надпочечников иногда выполняется через один год. Калид и др. Сообщили о 3 случаях гипертрофической кардиомиопатии преходящие у новорожденных, чьи матери получили повторные дозы антенатальных кортикостероидов, авторы считали, что начало гипертрофии желудочков на самом деле зависит от дозы и продолжительности инъекции кортикостероидов у матери до беременности, Однако, с учетом нашего наблюдения, считается, что даже низкие дозы могут вызвать эту патологию, так как мать получила только одно лекарство от бетаметазона, и связь со стрессовыми состояниями с выделениями катехоламинов могла бы потенцировать влияние кортикостероидов на сердечную мышцу и способствуют гипертрофии клеток сердечной мышцы.
При возникновении патологических нарушений сердечно-сосудистой системы выполнение этой функции значительно затрудняется, что приводит к чрезмерным энергетическим затратам. Повышенная нагрузка способствует увеличению мышечной массы сердца. Происходит это практически так же, как и при нарастании мышечной массы после усиленных физических нагрузок в спортзале. И если в случае с этой группой мышц это положительный результат, то для сердечных мышц является патологически опасным состоянием. Дело в том, что питающие сердце сосуды не успевают расти за мышечной массой, вследствие чего происходит недостаточное поступление крови в гипертрофированную ткань. Это, в свою очередь, является причиной различных ишемических изменений в миокарде.
Низкий вес больного ребенка, вероятно, является еще одним фактором. Все эти индексы могут предполагать, что это многофакторная сущность. Другие полагают, что эта транскрипция благоприятствует выражению тяжелой цепи миозина. Повторение этой сущности у часто недоношенных детей с малым весом может служить еще одним признаком задействованных молекулярных механизмов.
Его быстрая регрессия должна напоминать одну из причин метаболизма, в частности, диабет матери или опосредованную ятрогенную причину, включая кортикостероиды. Исчерпывающая этиологическая оценка по-прежнему необходима, но это дорогостоящая и медленная оценка, а консенсус о минимальном балансе, установленном учеными обществами, может улучшить и облегчить управление.
Вернуться к оглавлению
Диагностика
На электрокардиограмме присутствует зубец Q и подъем сегмента ST. Рентгенограмма грудной клетки может выявить увеличение тени сердца, что не является патогномоничным для аневризмы левого желудочка. Левая вентрикулография до недавнего времени была золотым стандартом для установления диагноза аневризмы левого желудочка.
Двумерная эхокардиография – также чувствительный метод для диагностики аневризм, позволяющий не только выявить саму аневризму, но и наличие в ней тромба, а также рассчитать по сегментам локальную и глобальную фракцию выброса. Стресс ЭхоКГ дополнительно способна определить наличие и объем гибернирующих участков миокарда.
Суть проблемы
Гипертрофия левого желудочка сердца часто является следствием перегрузки или нарушения работы клапанного аппарата. Это основной диагностический признак гипертрофической кардиомиопатии. Левый желудочек сердца — это полостное, мышечное образование, которое способно сокращаться и проталкивать кровь. Этой камерой начинается большой круг кровообращения.
Гипертрофия бывает нескольких видов: эксцентрической, концентрической и с обструкцией. Каждая форма имеет свои особенности. Эксцентрическая гипертрофия левого желудочка чаще всего формируется по причине недостаточности клапана, расположенного между левыми отделами сердца. В основе ее развития лежит превышение нормальных показателей объема крови в этом отделе сердца.
Увеличивается вес ЛЖ, и он растягивается. Подобные изменения негативно отражаются на сокращениях сердца. Высокая нагрузка приводит к снижению сердечного выброса. Концентрическая форма ГЛЖ отличается тем, что кровь забрасывается обратно, и миокарду требуется больше силы, чтобы ее протолкнуть в просвет аорты. Это сопровождается утолщением стенок камеры сердца. Иногда наблюдается уменьшение полости желудочка.
Факторы риска акинезии
Болезнь Паркинсона — заболевание, при котором происходит снижение продукции дофамина головным мозгом, что влияет на способность человека контролировать свои мышцы.
Лекарственный паркинсонизм — развивается в результате того, что человек принимает слишком много препаратов, которые ингибируют дофамин.
Прогрессирующий супрануклеарный паралич — это состояние, постепенно повреждающее мозг, при этом сначала нарушается баланс во время ходьбы.
Гормоны — гипотиреоз или низкие уровни гормонов щитовидной железы могут привести к акинезии.
У людей с болезнью Паркинсона мужчины чаще страдают акинезией, чем женщины.
Другие факторы риска:
- брадикинезия или замедленное движение мышц;
- болезнь Паркинсона, которая продолжается в течение длительного времени;
- постуральная нестабильность;
- проблемы с ригидностью мышц.
Гипертрофия левого желудочка сердца – прогноз
Если диагностирована умеренная и незначительная гипертрофия левого желудочка сердца, при проведении лечения и регулярном врачебном наблюдении прогноз благоприятный: пациенты остаются трудоспособными, качество жизни не нарушается, для женщин не исключаются беременность, роды. Тяжелая степень патологии может привести к инвалидизации, летальность составляет 4-5 %.
Прогноз протекания болезни определяется первопричиной подобного нарушения. При начальных стадиях гипертрофии, которая корректируется при помощи гипотензивных препаратов, прогноз достаточно хороший. Хроническая форма развивается очень медленно, и человек с такой болезнью может жить на протяжении нескольких десятков лет. При этом качество его жизни не страдает.
У пожилых людей с ишемией миокарда, а также ранее перенесенными инфарктами развитие хронической стадии предсказать достаточно сложно. Она может развиваться как медленно, так и стремительно, что приводит к инвалидности и потере работоспособности человеком.
Техника операции
Вследствие относительно хорошего прогноза для бессимптомной левожелудочковой аневризмы показания к операции относительны. Однако, у больных, подвергающихся АКШ необходимо восстановить геометрию левого желудочка. С другой стороны, для симптоматических (аритмии, стенокардия, застойная сердечная недостаточность) пациентов, операция предлагает лучший результат, чем медикаментозная терапия.
Оперативное лечение абсолютно показано больным с дискинетическими (акинетическими) аневризмами при увеличении конечно-систолического индекса {amp}gt; 80 мл/м2 и конечно-диастолического индекса {amp}gt; 120 мл/м2 ) , а также угрозе разрыва или развития ложной аневризмы, точно так же как и при врожденных аневризмах левого желудочка.
Согласно последним исследованиям, миокард представляет мышечную ленту, завернутую в спираль с определенным углом. Межжелудочковая перегородка состоит из трех мышечных слоев и вносит колоссальный вклад в выброс и присасывание крови. Диастола, как и систола, обеспечивается активным мышечным сокращением.
Принимая во внимание описанные выше патологические изменения, вызванные постинфарктной аневризмой, становится ясно, что ее пластика является патогенетически оправданной. Теоретически, такой подход обеспечит снижение напряжения в стенке левого желудочка и снижение потребности миокарда в кислороде (на основании закона Лапласа), нивелирует перегрузку объемом и переориентирует направление мышечных волокон в более физиологическую сторону с усилением механической эффективности выброса и присасывания.
Предлагаем ознакомиться: Аритмия у ребенка: что это такое и что делать?
Исключение из сокращения нефункционирующих сегментов и восстановление правильной ориентации миофибрилл может повысить коэффициент полезного действия базальных и средних сегментов интактного миокарда. В этой связи важным моментом операции является формирование левого желудочка в виде «готической», а не «романской» арки.
Относительные противопоказания к операции включают чрезмерный риск анестезии, отсутствие жизнеспособного миокарда вне аневризмы, низкий ({amp}lt; 2,0 л•мин/м2) сердечный индекс, выраженная митральная недостаточность. Глобальная фракция изгнания может быть менее полезной для оценки показаний к операции, чем сегментарная фракция изгнания оставшейся части миокарда левого желудочка.
Ангиопластика возможна только у пациентов с подходящей коронарной анатомией, одно- или двухсосудистом поражении и противопоказаниями к операции.
Выполняется стандартная срединная стернотомия. ИК осуществляется в режиме нормо- или умеренной гипотермии. Используется анте- и ретроградная кровяная кардиоплегия. Проводится внешняя ревизия левого желудочка для идентификации области рубца и утончения стенки. Разрез аневризмы выполняется вертикально, отступая влево от ПМЖВ на 1 см.
Выполняется резекция аневризмы по одному из методов, описанных ниже. Затем при необходимости проводится пластика или протезирование митрального клапана и полная реваскуляризация миокарда. Отключение аппарата ИК часто требует инотропной поддержки. Как правило, используется допамин (5 мкг/кг/мин.), а также нитроглицерин для предотвращения спазма коронарных артерий и нитропруссид натрия для снижения постнагрузки.
Дополнительная инотропная поддержка не увеличивает сердечный выброс и может привести к аритмии и тахикардии. Поскольку левый желудочек плохо растяжим, ударный объем фиксирован (КДО левого желудочка ≈ 150 мл), ЧСС 90-115 уд. в мин. достаточна, чтобы поддержать сердечный индекс {amp}gt; 2,0 л•мин/м2. Контрпульсация может также быть необходима у пациентов со сниженной контрактильностью миокарда.
Гипертрофия миокарда – классификация
Для удобства работы в медицине принято различать такие виды гипертрофии миокарда:
- обструктивная – вверху перегородки, по всей площади;
- необструктивная – симптомы выражены слабо, диагностируются случайно;
- симметрическая – поражаются все стенки левого желудочка;
- верхушечная – мышцы сердца увеличены лишь сверху;
- асимметричная – затрагивает только одну стенку.
Эксцентрическая гипертрофия
При этом виде ГЛЖ происходит расширение полости желудочка и одновременно равномерное, пропорциональное уплотнение мышц миокарда, вызванное ростом кардиомиоцитов. При общем увеличении массы сердца относительная толщина стенок остается неизменной. Эксцентрическая гипертрофия миокарда может поражать:
- межжелудочковую перегородку;
- верхушку;
- боковую стенку.
Концентрическая гипертрофия
Для концентрического типа заболевания характерно сохранение объема внутренней полости при повышении массы сердца за счет равномерного увеличения толщины стенок. Существует другое название этого явления – симметричная гипертрофия миокарда. Возникает болезнь как результат гиперплазии органелл миокардиоцитов, спровоцированной высоким давлением крови. Такое развитие событий характерно для артериальной гипертензии.
Причины расстройств движения
Расстройства двигательной активности обусловлены расстройством функции мозговых структур, ответственных за динамику движения.
Так, наступление акинезии может быть следствием повреждения основания мозга либо его лобных долей по причине энцефалопатий, ассоциированных с:
- тяжелыми видами почечной (уремический кататонический синдром) либо печеночной недостаточности (печеночная депрессивная акинезия);
- патологией кроветворения (тяжелые вариации течения пернициозной и гемолитической анемии);
- болезнями системы дыхания (энцефалопатия на почве гипоксических расстройств).
Либо она может быть вызвана тяжелыми интоксикациями и нейроинфекциями.
Причиной гипокинезии может стать дисфункция структур, составляющих экстрапирамидную (строиопаллидарную) систему, в которую входят такие образования подкорки как паллидум и красные ядра – начало монаковского экстрапирамидного тракта, осуществляющего реализацию безусловных рефлексов, проводя импульсы от всех отделов большого мозга ниже коры к передним рогам мозга спинного.
В свою очередь, патологические изменения в экстрапирамидной системе могут быть спровоцированы различными психическими и неврологическими состояниями.
Гипокинезия может также стать следствием гиподинамии – недостатка движения либо дефицита мускульной активности локального характера с производством однообразных движений, не требующих высоких энергозатрат.
К тем же результатам приводят и хронические производственные и бытовые интоксикации и иные факторы.
Наиболее характерными являются симптомы гипокинезии при паркинсонизме.
Возможные причины акинезии включают:
- Аномалии развития нервной системы;
- Заболевания соединительной ткани, такие как хондродисплазии;
- Водянка плода;
- Заболевания матери или употребление наркотиков.
Любые изменения в утробе, которые вызывают недостаточный кровоток и уровень кислорода, могут привести к акинезии плода.
Врачи выделили две мутации генов, которые связаны с повышенными рисками для развития акинезии плода. Если у человека имеются родственники с патологией, то он должен провести тест на мутации генов DOK7 и RAPSN, которые связаны с акинезией.
Признаки заболевания
Сердечная патология долго ничем себя не проявляет. Но со временем увеличенная мышечная масса начинает оказывать действие на системный кровоток. Появляются первые признаки недомогания. Они обычно связаны с большой физической нагрузкой. С развитием болезни проявления беспокоят больного и в покое.
Симптомы гипертрофии левого желудочка:
- Одышка, перебои в сердце, нехватка воздуха.
- Головокружения, обморочные состояния.
- Ангинозные (сжимающие, давящие) боли за грудиной.
- Перепады АД.
- Высокое давление, плохо поддающееся терапевтическим мерам.
- Отеки конечностей и лица к вечеру.
- Приступы удушья, беспричинного кашля в положении лежа.
- Синюшность ногтей, носогубного треугольника.
- Сонливость, головные боли неясной природы, слабость.
Заметив у себя подобные признаки, надо поспешить к кардиологу.
Лечение
Лечение зависит от того, что вызывает симптомы акинезии. Например, при акинезии, связанной с препаратами, необходимо прекратить принимать лекарственные средства, которые вызывают проблему.
При болезни Паркинсона зачастую врачи назначают препараты, которые увеличивают количество дофамина в организме. Они могут помочь, поскольку снижение уровня дофамина вызывает нервно-мышечные симптомы, связанные с болезнью Паркинсона. Примеры таких препаратов включают леводопу и карбидопу, а также агонисты дофамина.
Люди с болезнью Паркинсона или другими расстройствами могут обратиться к врачу лечебной физкультуры, который поможет им научиться двигаться безопасно. В настоящее время нет лечения данного состояния.
В зависимости от спровоцировавшей расстройство причины лечение будет принципиально отличаться по применяемым методам.
При наличии опухоли мозга производится оперативное её иссечение, при факторе интоксикации (бытовой, производственной) необходимо принять меры по пресечению воздействия на организм токсического соединения.
Нейроинфекции лечатся применением медикаментов, эффективных в отношении вызвавшего патологию возбудителя, а последствия их воздействия устраняются использованием всего арсенала препаратов, которые улучшают кровоснабжение мозга и медикаментов-детоксикантов.
К превентивным мерам относятся мероприятия, направленные на недопущение в организм возбудителей нейроинфекций, предотвращение травм головы и риска токсического воздействия производственных и бытовых ядов.
Увеличение двигательной активности работниками умственного труда (предотвращение гиподинамии) также является существенной мерой предотвращения расстройств динамики движения.
Патогенез болезни
Гипертрофия практически всегда является сопутствующим синдромом различных долго протекающих сердечных заболеваний. Основными причинами возникновения гипертрофии левого желудочка являются:
Патофизиология основных синдромов: сердечная недостаточность
Авторы не заявляют о каком-либо конфликте интересов. Все авторы внесли свой вклад в написание этой рукописи и прочитали и утвердили окончательный вариант рукописи. Сердечная недостаточность — это сокращение работоспособности миокарда, которое больше не способно удовлетворить потребности организма, стресс и даже отдых. Многие патологические ситуации могут привести к сердечной недостаточности. Если их патофизиология остается, чаще всего, запутанной, мы можем выделить основные задействованные механизмы.
- курение и чрезмерное употребление алкоголя;
- избыточный вес;
- долгие изнурительные физические нагрузки;
- стеноз аортального клапана;
- гипертоническая кардиопатия.
Наиболее часто гипертрофия возникает на фоне артериальной гипертензии. В 60-70% клинических случаев изменение массы миокарда обусловлено стойким артериальным давлением.
Увеличение пост-разряда может привести к сердечной недостаточности, когда оно длительное и продолжительное. Это относится к хронической гипертензии, а также к сужению аортального клапана. Увеличение предварительной нагрузки может привести к аналогичному результату, когда, например, недержание мочи в аортальном клапане вызывает систолическую регургитацию, так что теледиастолический объем желудочка увеличивается.
Наконец, функциональное ухудшение сердечной мышцы само по себе вызывает сердечную недостаточность при дисфункции миокарда. Фактически, эта классификация остается частично произвольной, поскольку дисфункция миокарда приводит к увеличению систолического объема и, следовательно, к объемной перегрузке, когда желудочек не сливается должным образом в систолу. Это то же самое, когда после зарядки увеличивается, когда провал желудочка не может эффективно бороться. Тем не менее, хронологическая последовательность изменений отличается в зависимости от причинно-патологической патологии, и морфологические перестройки, возникающие из них, также различны.
Лишний вес тоже является предпосылкой возникновения ГЛЖ, так как увеличенный в размерах организм нуждается в повышенной величине кровоснабжения, что приводит к развитию патологических изменений миокарда.
Порок сердца является основной врожденной предрасположенностью развития гипертрофии миокарда по причине нарушения оттока крови от желудочка.
Эти перестройки, обозначенные общим термином ремоделирования, появляются скорее в направлении расширения желудочка, когда первоначальная причина представляет собой объемную перегрузку. Дилатация является глобальной или локальной. Ремоделирование в основном связано с гипертрофией желудочковой мышцы в случае увеличения постобработки.
Таким образом, париетальное напряжение является центральным параметром сердечной недостаточности. Расход энергии миокарда действительно пропорционален напряжению стенки. Чем больше давление, тем больше диаметр полости желудочка и чем меньше стенок желудочка.
Вернуться к оглавлению
Результаты
Госпитальная летальность значительно снизилась за последние годы и составляет 3-7%. Основной причиной смерти является левожелудочковая недостаточность – 64%. Факторами риска послеоперационной летальности являются: пожилой возраст, неполная реваскуляризация миокарда, женский пол, экстренная операция, протезирование митрального клапана, фракция выброса левого желудочка {amp}lt; 30%, дооперационный сердечный индекс {amp}lt; 2,1 л.мин/м2, среднее давление в легочной артерии {amp}gt; 33 мм рт.ст., уровень креатинина {amp}gt; 180 мг/л.
Наиболее частым осложнением в госпитальном периоде является синдром малого сердечного выброса, а также желудочковые аритмии и легочная недостаточность.
В отдаленном послеоперационном периоде улучшается функция левого желудочка: возрастает фракция выброса, уменьшается КДО и КСО левого желудочка, диастолическое наполнение и комплайнс, увеличивается толерантность к физической нагрузке. Средний класс стенокардии снижается с 3,5 до 1,2, а класс сердечной недостаточности по классификации NYHA с 3,0 до 1,7. Результаты непосредственно зависят от метода ремоделирования левого желудочка, демонстрируя явное отсутствие преимуществ линейной пластики.
5-летняя выживаемость составляет 58-80%, 10-летняя – 34-57%. 57% смертельных случаев являются следствием повторных инфарктов миокарда. Дооперационными факторами риска отдаленной летальности являются возраст, фракция выброса {amp}lt; 35%, КДД Левого желудочка {amp}gt; 20 мм рт.ст., и митральная недостаточность.
Лечение аневризмы левого желудочка в Минске – европейское качество за разумную цену.
Профессор, доктор медицинских наук Ю.П. Островский
Метки: акинезия, кардиология, такой
Об авторе: admin4ik
« Предыдущая запись
Народные средства
Народные средства можно применять в качестве дополнительной терапии к основному лечению. Использовать их можно только после проведения диагностики и с разрешения врача. Народное лечение подразумевает под собой применение лекарственных трав, которые помогают избавиться от причины, спровоцировавшей заболевание, его симптоматики и направлены на нормализацию самочувствия.
Для приготовления отвара потребуется смесь багульника, пустырника, сушеницы и почечного чая. Все компоненты нужно перемешать в равных пропорциях, затем взять 2 ст. л. смеси и залить 300 мл кипятка. Прокипятить на медленном огне, охладить, процедить и принимать 3 раза в день.
Укрепить сердечную мышцу поможет крепкий настой зверобоя. Перед его потреблением нужно добавлять немного меда. Хороший эффект оказывает земляничное варенье с молоком, сухофрукты, курага, клюква с сахаром, изюм.