© Автор: Сазыкина Оксана Юрьевна, кардиолог, специально для СосудИнфо.ру (об авторах)
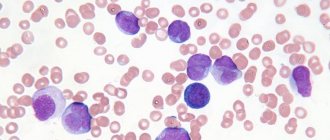
Тромбоэмболические осложнения являются довольно серьезной проблемой в хирургии, потому что не только вызывают тяжелое течение послеоперационного периода, но и могут привести к внезапной гибели пациента. По статистике, около 100 тысяч пациентов в России ежегодно погибают от внезапной тромбоэмболии легочной артерии (ТЭЛА). Летальность при развитии массивной тромбоэмболии легочной артерии составляет около 5%. Тромбоэмболия представлена тромбами, образующимися в просвете сосудов и разносящимися с потоком крови по организму. Чаще тромбы образуются в просвете вен нижних конечностей, а затем попадают в правую половину сердца и далее в артерии легких.
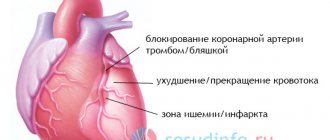
Вне зависимости от размера тромба происходит закупорка артерии того или иного диаметра, вследствие чего участок легочной ткани, кровоснабжаемый отходящими от закупоренной артерии ветвями, не получает должного питания, и ткань отмирает. Чем больше тромб, тем шире просвет закупоренной артерии, тем большее число ветвей не получают крови, тем в более обширном участке легкого гибнут клетки. Гибель, или некроз, клеток называется инфарктом легкого. Это патогномоничный морфологический признак для тромбоэмболии легочной артерии (ТЭЛА).
тромбоэмболия легочной артерии с последующим инфарктом легкого
Если инфаркт легкого вследствие обтурации легочной артерии тромбом привел к поражению большого количества легочной ткани, наступает острая сердечно-легочная и дыхательная недостаточность, что без лечения приводит к летальному исходу. Вот почему профилактика тромбоэмболии в постоперационном периоде является одной из актуальных проблем хирургии.
Но тромбоэмболия легочной артерии представляет опасность для больных не только хирургического, но еще и урологического, травматологического, гинекологического и акушерского профиля. То есть для всех больных, которым планируется или уже проведено оперативное вмешательство.
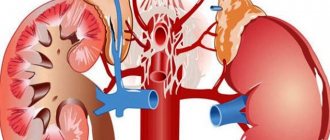
Кроме тромбоэмболии легочной артерии, к тромбоэмболическим осложнениям относится тромбоз нижней полой вены и острый флеботромбоз нижних конечностей. Эти тромбозы не только являются непосредственным фоном для развития ТЭЛА, но и сами по себе несут угрозу для здоровья пациента.
тромбоз глубоких вен голени (слева) и нижней полой вены (справа)
Причины тромбоэмболии
Причинные факторы венозных тромбоэмболических осложнений (ВТЭО) можно условно подразделить на нарушения нормального кровотока в венах нижних конечностей, а также на предрасполагающие факторы.
К первой группе причин можно отнести все факторы, способствующие активации так называемой триады Вирхова, суть которой заключается в следующем. Образование тромба в просвете сосуда возможно в том случае, если в вене замедляется ток крови, присутствует нарушение целостности сосудистой стенки, а также имеется склонность к гиперкоагуляции крови. Все эти условия возникают во время раннего постоперационного периода у пациентов с заболеваниями, требующими экстренного или планового хирургического вмешательства.
Так, развитие ВТЭО возможно при следующих состояниях (в скобках указан процент больных с венозными тромбоэмболическими осложнениями из общего числа прооперированных):
- Операции на органах брюшной полости, в том числе лечебная или диагностическая лапароскопия (19)%,
- Гинекологические операции, в том числе лечебно-диагностическое выскабливание полости матки и операция кесарева сечения (11.2%),
- Урологические операции, в том числе резекция аденомы простаты (7.1%),
- Нейрохирургические операции (24%),
- Операции по поводу злокачественных опухолей различной локализации (30%),
- Протезирование коленного или тазобедренного суставов, а также сочетанная травма и переломы, требующие операции или длительной иммобилизации (обездвиживания) пациента (84%).
К предрасполагающим факторам относятся:
- Пол – у женщин тромбы в венах образуются чаще в силу гормональных особенностей,
- Возраст – чем старше человек, тем выше вероятность тромбообразования в венах,
- Образ жизни – «сидячая» и малоподвижная работа способствуют застою крови в венах,
- Наличие варикозно расширенных вен в нижних конечностях – чем больше узлов и чем выше несостоятельность клапанов вен, тем медленнее ток крови по сосуду и выше склонность к агрегации тромбоцитов,
- Прием гормональных контрацептивов (КОКи – комбинированные оральные контрацептивы), которые значительно изменяют реологические свойства крови,
- Наследственные нарушения свертывающей системы крови – тромбофилия, или склонность к повышенному тромбообразованию.
Основная профилактика ТЭЛА при различных ситуациях
Закупорка легочной артерии тромбом (ТЭЛА) чаще всего происходит при тромбозе глубоких вен голени.
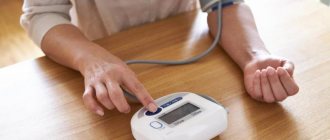
Поэтому у пациентов с высоким риском легочной тромбоэмболии проводится профилактика при помощи эластической компрессии и введения антикоагулянтов.
Она показана до и после хирургических вмешательств, особенно длительных и обширных операций, в травматологической практике, при ишемическом инсульте, у беременных женщин.
Приказ Минздрава по профилактике ТЭЛА
Особая роль закупорки легочной артерии в осложнениях послеоперационного периода отражена в нормативных документах. Это связано с тем, что ТЭЛА стоит на третьем месте среди причин смерти после инфаркта миокарда и инсульта, а 90% летальных исходов вызваны несвоевременной диагностикой и лечением. Поэтому всем пациентам, которые отнесены в группу риска, рекомендуется:
- максимально ранняя двигательная активность после операции, родов – вставание и активная ходьба;
- исключение длительного стояния или пребывания в сидячем положении с опущенными ногами;
- ношение компрессионного трикотажа (чулки) 1 — 2 класса компрессии, бинтование эластичными бинтами до и во время хирургического вмешательства (кроме операций на нижних конечностях);
- в послеоперационном периоде введение антикоагулянтов или пневматическая компрессия при противопоказаниях к Гепарину и его аналогам;
- ношение эластичного лечебного трикотажа в период стационарного и амбулаторного лечения.
Рекомендуем прочитать статью о профилактике тромбозов. Из нее вы узнаете о том, что такое тромбофилия, симптомах, диагностике и лечении тромбофилии.
А здесь подробнее о том, как предотвратить тромбофлебит после операции.
Группы риска ТЭЛА
Противотромботическая терапия показана таким категориям больных:
- при длительном постельном режиме – гиподинамия приводит к формированию нестабильных тромбов, которые склонны к разрушению и отрыву от стенки;
- в случае запланированной операции – стресс, болевой синдром стимулируют формирование кровяных сгустков, длительная операция, особенно в полости малого таза, нижних конечностей повышает риск венозного тромбоза. Любое повреждение тканей также провоцирует выброс факторов свертывания. Кровопотеря и централизация кровообращения повышают вязкость крови и тромбофилию;
- при использовании общего наркоза – слишком сильная или продолжительная анестезия вызывают гиперкоагуляцию, провоцируют застой крови в ногах;
- после введения цельной крови или эритроцитарной массы;
- пожилого возраста – после 40 лет падает антисвертывающая активность, нарушается структура сосудистой стенки, падает сердечный выброс и возврат венозной крови к сердцу, риск тромбоза возрастает при предшествующей гиподинамии;
- со злокачественными новообразованиями – активизируется свертывание крови;
- с избыточной масса тела – тромбозы связаны с нарушением жирового обмена;
- имевшийся в прошлом венозный тромбоз, тромбоэмболию, варикозную болезнь.
К дополнительным факторам риска относится сердечная недостаточность, мерцательная аритмия, бактериальный эндокардит, миокардит, кардиомиопатия. Нередко ТЭЛА выявляют у пациентов с сахарным диабетом, сепсисом, врожденной тромбофилией, антифосфолипидным синдромом.
Беременность, особенно осложненная гестозом, родовой и послеродовой периоды также включены в перечень факторов риска. Провоцировать ускоренное образование тромбов может применение гормонов для контрацепции, лечения климакса, болезни почек и кишечника, инфаркт и инсульт, противоопухолевая лучевая или химиотерапия.
Как проводится профилактика
Помимо общих принципов предупреждения ТЭЛА (активность, компрессия, гепаринотерапия) имеются особенности в различных клинических ситуациях.
Перед операцией
Если обнаружен высокий риск развития легочной тромбоэмболии, то необходимо:
- сократить предоперационный стационарный период – обследовать в амбулаторных условиях;
- использовать гимнастику, массаж, физиотерапию, если нет противопоказаний;
- исключить переедание;
- применять эластичное бинтование нижних конечностей или компрессионный трикотаж;
- принимать транквилизаторы и психотерапию для снижения выброса гормонов стресса.
Смотрите на видео о развитии ТЭЛА:
До операции ликвидируют дефицит объема крови, нормализуют гематокрит. При повышенной свертывающей активности применяется Рефортан внутривенно, а также Гепарин или Фрагмин с большой осторожностью, чтобы не вызывать кровотечений, за 24 — 12 часов любые антикоагулянты отменяют.
В травматологии и послеоперационном периоде
Непосредственно антикоагулянтная терапия проводится при помощи Гепарина не менее 3 дней и низкомолекулярных аналогов – Цибор, Фрагмин, Клексан.
Их рекомендуется применять 2 раза в день вначале вместе с Гепарином, снижая его дозу, а затем самостоятельно.
Минимальный срок гепаринотерапии составляет 2 недели, а при онкологических заболеваниях ее нередко продлевают до 3 месяцев. Крайне важно при этом не допустить кровотечений.
Помимо этих препаратов после крупных ортопедических операций применяют:
- антиагреганты при повышенном уровне тромбоцитов – Кардиомагнил, Плавикс;
- растворы для поддержания гематокрита на уровне 30 — 33%;
- ранний перевод на обычное питание, так как белковые, а особенно жировые эмульсии повышают образование тромбов;
- обезболивающие и противовоспалительные препараты;
- переливание свежезамороженной плазмы при дефиците факторов противосвертывающей системы.
У больных ишемическим инсультом
В остром периоде инсульта у почти у каждого седьмого пациента возникает ТЭЛА. Трудность выявления этого осложнения связана с тем, что часто тромб образуется в парализованной конечности, закупорка сосуда протекает бессимптомно, а из-за нарушения сознания жалобы отсутствуют. Если провести профилактическую антикоагулянтную терапию, то вероятность тромбоэмболии снижается до 0,7%.
В связи с этим пациентам, у которых имеется ожирение, варикоз вен нижних конечностей, застойная сердечная недостаточность, поражения легких, постоянный венозный катетер, показана профилактика ТЭЛА. Для этого применяется:
- адекватное введение растворов или питьевой режим для поддержания высокой текучести крови;
- разработка парализованных конечностей с первых дней болезни;
- бинтование или компрессия лечебным трикотажем на протяжении всего периода постельного режима;
- Фраксипарин, Клексан подкожно один раз в сутки;
- Тромбо Асс, Аспирин кардио в дозе 150 — 300 мг в день.
У беременных
ТЭЛА считается самой частой причиной материнской смертности. Ее риск при беременности возрастает в 5 — 6 раз, а в послеродовом периоде, особенно после кесарева сечения, вероятность еще выше.
Наиболее подвержены легочной тромбоэмболии пациентки после 35 лет, а также те, у которых обнаружены:
Для профилактики ТЭЛА у беременных применяется Гепарин. Его вводят до 2 месяцев при умеренном риске тромбоэмболии и не менее трех – при высоком. После родов женщины могут быть переведены на Варфарин, Прадакса, Ксарелто. Чаще всего не отменяют кормления грудью на фоне антикоагулянтной терапии.
Виды профилактики ТЭЛА
В зависимости от целей, выделяют первичные и вторичные меры предупреждения легочной тромбоэмболии, а помимо традиционного медикаментозного, используется и хирургический метод.
Первичная и вторичная
Для предупреждения образования тромбов в венозной сети проводится первичная профилактика. Она включает:
- выявление группы риска;
- ношение компрессионного трикотажа;
- максимально раннюю двигательную активность после родов, операций;
- применение массажа и лечебной гимнастики;
- поддержание нормальных показателей содержания тромбоцитов и вязкости крови;
- применение Гепарина, низкомолекулярных аналогов с переходом на Варфарин при операциях, травмах;
- нормализацию веса тела;
- при путешествиях – достаточный питьевой режим, компрессионные чулки, запрет на алкоголь, движения;
- исключение курения;
- контроль артериального давления, при наследственной предрасположенности – дополнительно коагулограммы и D-димера;
- выбор контрацепции без гормональных препаратов.
Вторичная профилактика направлена на предотвращение рецидива при уже развившейся ТЭЛА. Она предусматривает введение антикоагулянтов в терапевтических дозах и оперативное лечение. Для длительного применения чаще всего рекомендуется Варфарин.
Как оценить риск возникновения ВТЭО?
Любой врач хирургической специальности, планирующий оперативное вмешательство своему пациенту, должен уметь оценить риски возникновения тромбоэмболических осложнений, и в частности, риск развития ТЭЛА.
Оценка рисков ВТЭО определяется исходя из характера хирургического вмешательства:
- Низким риском тромбоэмболических осложнений в послеоперационном периоде у хирургических больных характеризуются неосложненные малые операции. Риск ТЭЛА при их проведении составляет менее 0.2% от числа всех прооперированных, в том числе с 0.002% летальных случаев в результате массивной тромбоэмболии. К подобным относятся лапароскопические вмешательства, чрезуретральные урологические манипуляции на простате.
- Средняя степень риска с частотой возникновения тромбозов у менее, чем 5% прооперированных пациентов, характерна для больших операций. К ним относятся удаление желчного пузыря, аппендэктомия с осложнениями (флегмонозный, гангренозный аппендицит), операция кесарева сечения или ампутация матки, удаление части желудка или кишечника, удаление аденомы простаты с чрезпузырным доступом.
- К вмешательствам, которые сопровождаются высокой частотой ВТЭО (более 80% тромбозов в глубоких венах голеней, более 40% тромбозов в нижней полой вене и более 10% ТЭЛА, в том числе с летальным исходом), относятся расширенные операции – удаление злокачественных новообразований, травматологические и ортопедические с протезированием суставов операции, а также нейрохирургические вмешательства.
В связи с этим первая группа операций подразумевает под собой низкую степень риска ВТЭО, вторая группа – умеренную степень риска, и третья группа – высокую степень риска ВТЭО.
Профилактика, диагностика и лечение послеоперационной тромбоэмболии легочной артерии
Ключевые слова: послеоперационная ТЭЛА, гепаринопрофилактика, бемипарин. Тромбоэмболия легочной артерии (ТЭЛА) является одной из довольно частых и грозных неотложных ситуаций, в т.ч. в послеоперационном периоде. Причина ТЭЛА – это окклюзия ствола или мелких ветвей артерий малого круга кровообращения тромбоэмболами с развитием правожелудочковой, а затем и бивентрикулярной сердечной недостаточности. В структуре летальности от сердечно-сосудистых заболеваний ТЭЛА занимает третье место после инфаркта миокарда и инсульта. В экономически развитых странах 0,1% населения ежегодно погибают от данной патологии [1, 3, 9]. Дать точную оценку частоте послеоперационной ТЭЛА не представляется возможным, поскольку часто это состояние протекает бессимптомно. При жизни диагноз ТЭЛА устанавливается менее чем в 70% наблюдений. Летальность среди пациентов без патогенетической терапии, по данным различных авторов, составляет 40% и более, при массивной ТЭЛА достигает 70%, а при своевременно начатой терапии колеблется от 2 до 8% [1, 9]. По данным ряда авторов, ТЭЛА является причиной 5% летальных исходов после общехирургических и 23,7% – после ортопедических операций. Легочная эмболия занимает одно из ведущих мест в акушерской практике: смертность от этого осложнения колеблется от 1,5 до 2,7% на 10 тыс. родов, а в структуре материнской смертности составляет 2,8–9,2% [2]. В европейских странах, в частности во Франции, частота ТЭЛА составляет до 100 тыс. случаев в год, в Англии и Шотландии с ТЭЛА госпитализируются 65 тыс., а в Италии – 60 тыс. пациентов ежегодно [8]. В США в год выявляют до 150 тыс. больных, переносящих ТЭЛА как осложнение различных заболеваний. Среди госпитализированных пациентов 70% приходится на долю терапевтических больных [8]. По данным Фрамингемского исследования, смерть от ТЭЛА составляет 15,6% от всей внутригоспитальной летальности, причем на хирургических больных приходится 18% случаев, а 82% составили больные с терапевтической патологией [1, 9]. Следует понимать, что источник тромба, который достигает малого круга кровообращения, главным образом находится в сосудах бассейна нижней полой вены, а именно – в венах нижних конечностей и малого таза. Чаще всего первичный тромб находится в илеокавальных сегментах или проксимальных отделах вен нижних конечностей (подколенно-бедренном сегменте). Венозный тромбоз с локализацией в дистальных отделах глубоких вен нижних конечностей (голени) осложняется ТЭЛА в 1–5% случаев. В последнее время появились сообщения об учащении случаев ТЭЛА из бассейна верхней полой вены (до 3,5%) в результате постановки венозных катетеров в отделениях реанимации и блоках интенсивной терапии [1, 9]. Наиболее опасными для развития ТЭЛА являются «флотирующие тромбы», имеющие точку фиксации в дистальном отделе венозного русла; остальная их часть расположена свободно и на всем протяжении не связана со стенками вены, причем их протяженность может колебаться от 5 до 20 см. «Флотирующий тромб» обычно формируется в венах меньшего калибра, и процесс тромбообразования распространяется проксимально в более крупные: из глубоких вен голени – в подколенную вену, затем в глубокую и общую бедренную артерию, из внутренней – в общую подвздошную, из общей подвздошной – в нижнюю полую вену [1]. Размеры тромбоэмболов определяют их локализацию в сосудах легочной артерии, обычно они фиксируются в местах деления сосудов легкого. По данным различных авторов, эмболизация ствола и главных ветвей легочной артерии имеет место в 50%, долевых и сегментарных – в 22%, мелких ветвей – в 30% случаев. Одновременное поражение артерий обоих легких достигает 65% от всех случаев ТЭЛА, в 20% – поражается только правое, в 10% – только левое легкое, нижние доли поражаются в 4 раза чаще, чем верхние [9]. Факторы риска венозного тромбоэмболизма (ТЭЛА в частности) следующие: пожилой возраст, длительная обездвиженность (вследствие пареза конечностей, после травм, в послеоперационном периоде, при частых и продолжительных перелетах в самолетах или поездках в автомобилях и т.д.), онкологические заболевания, травмы (особенно переломы крупных костей), хирургические вмешательства и внутрисосудистые инвазивные манипуляции (подключичный катетер и др.), прием некоторых лекарственных препаратов (заместительная гормональная терапия, использование оральных контрацептивов, химиотерапия), хроническая сердечная или дыхательная недостаточность, беременность и послеродовый период, тромбофилия. Имеются данные о том, что ТЭЛА ассоциируется также с такими проблемами, как ожирение, метаболический синдром, артериальная гипертензия, курение, сердечно-сосудистые события (инфаркт миокарда, инсульт). Так, тромбоэмболические осложнения, по данным разных авторов, встречаются у 30–60% больных с инсультами, обусловившими паралич нижних конечностей, у 5–35% пациентов после перенесенного инфаркта миокарда, более чем у 12% лиц с застойной сердечной недостаточностью. Серьезным фактором риска является наличие заболеваний вен нижних конечностей в анамнезе, особенно тромбоз глубоких вен. Частота ТЭЛА увеличивается с возрастом: средний возраст больных ТЭЛА составляет 62 года, при этом большинство (не менее 65%) пациентов старше 60 лет, а у больных старше 80 лет ТЭЛА встречается в 8 раз чаще, чем у лиц моложе 50 лет [1, 9]. Тромбы из вен нижних конечностей и таза с током крови попадают в правое предсердие, затем в правый желудочек, где происходит их фрагментация. Из правого желудочка тромбы попадают в малый круг кровообращения. Массивная легочная эмболия сопровождается повышением давления в легочной артерии, а это приводит к увеличению общего сосудистого сопротивления в легких. Возникают перегрузка правого желудочка, падение сердечного выброса и развитие острой сердечно-сосудистой недостаточности. Диагностика послеоперационной ТЭЛА представляет собой нелегкую задачу. Симптомы ТЭЛА не имеют четкой специфичности, клиническая картина ассоциируется с обострением таких заболеваний, как ишемическая болезнь сердца, хроническая сердечная недостаточность, заболевания легких или является одним из осложнений онкологических заболеваний, травм, обширных хирургических вмешательств. Наиболее характерными симптомами ТЭЛА являются «тихая» одышка инспираторного типа с частотой до 24 уд./мин. и выше, тахикардия более 90 уд./мин., бледность с пепельным оттенком кожных покровов. При массивной ТЭЛА имеет место (в 20% случаев) выраженный цианоз лица, шеи и верхней половины туловища. Загрудинные боли при эмболии основного ствола легочной артерии носят раздирающий характер (раздражение афферентных окончаний, заложенных в стенке артерии). Резкое уменьшение коронарного кровотока вследствие снижения ударного и минутного объемов сердца может вызвать стенокардитические боли. Острое набухание печени при правожелудочковой недостаточности обусловливает сильные боли в правом подреберье, часто сочетающиеся с симптомами раздражения брюшины и парезом кишечника. Развитие острого легочного сердца проявляется набуханием шейных вен, патологической пульсацией в эпигастрии. На аорте выслушивается акцент II тона, под мечевидным отростком – систолический шум, в точке Боткина – ритм галопа. Центральное венозное давление может быть значительно повышено. Выраженная артериальная гипотензия, вплоть до развития шока, указывает на массивную ТЭЛА. Кровохарканье, отмечаемое у 30% больных, обусловлено развитием инфаркта легкого [1, 7, 9]. Методы инструментальной диагностики требуют проведения специальных процедур, имеющих ограниченное распространение. К ним относятся, прежде всего, ангиография малого круга кровообращения («золотой стандарт» диагностики ТЭЛА) и сцинтиграфия легких. При ангиографии прямыми признаками ТЭЛА являются дефект наполнения в просвете сосуда и «ампутация» (т. е. обрыв) сосуда, а косвенными – расширение главных легочных артерий, уменьшение числа контрастированных периферических ветвей, деформация легочного рисунка. Рентгенологические исследования малоинформативны. Наиболее характерными симптомами острого легочного сердца (в 15% случаев) как проявления ТЭЛА являются расширение верхней полой вены и тени сердца вправо, а также набухание конуса легочной артерии, которое проявляется сглаживанием талии сердца и выбуханием второй дуги за левый контур. Может наблюдаться расширение корня легкого (в 4–16% случаев), его «обрубленность» и деформация на стороне поражения. При эмболии в одну из главных ветвей легочной артерии, в долевые или сегментарные ветви при отсутствии фоновой бронхолегочной патологии наблюдается обеднение («просветление») легочного рисунка (симптом Вестермарка). Дисковидные ателектазы, отмечаемые в 3–8% случаев, обычно предшествуют развитию инфаркта легкого и обусловлены обструкцией бронха геморрагическим секретом или увеличенным количеством бронхиальной слизи, а также снижением выработки альвеолярного сурфактанта. Инфаркт легкого развивается на 2–3-и сутки после эмболизации и клинически проявляется болями в грудной клетке при дыхании и кашле, одышкой, тахикардией, крепитацией, влажными хрипами в легких, гипертермией. В настоящее время алгоритм диагностики ТЭЛА основан преимущественно на использовании компьютерной томографии (КТ) – чувствительного, неинвазивного и относительно доступного метода обследования, однако предварительно необходимо исключить пациентов, которым КТ не потребуется (для больных высокого риска – с помощью эхокардиограммы (ЭхоКГ), для больных невысокого риска – с помощью оценки вероятности ТЭЛА и определения уровня D-димера). КТ на сегодняшний день признана экспертами наиболее приемлемым методом подтверждения наличия тромба в легочных сосудах, рекомендованным для рутинной клинической практики. У больных высокого риска достаточно обычной (однодетекторной) КТ, чтобы подтвердить или исключить ТЭЛА, однако у больных невысокого риска рекомендуется использовать мультидетекторную КТ, которая позволяет более четко визуализировать сегментарные и субсегментарные ветви легочной артерии и достоверно подтвердить или исключить ТЭЛА. Если нет возможности использовать мультидетекторную КТ, у таких пациентов либо устанавливается диагноз ТЭЛА при положительных результатах однодетекторной КТ, либо требуется двойной контроль для исключения ТЭЛА, когда негативные результаты однодетекторной КТ сопоставляются с данными венозной компрессионной ультрасонографии, и если оба метода обследования не обнаружат тромбов, только тогда диагноз ТЭЛА можно снять. На ЭКГ острая перегрузка правого желудочка вследствие высокого давления в малом круге кровообращения приводит к появлению зубцов SI и QIII (так называемый тип SI-QIII). В отведении V1, V2 возрастает амплитуда зубца R. Возможно появление зубца S в отведениях V4–V6. Сегмент ST дискордантно смещается книзу в отведениях I, II, aVL и кверху – в отведениях III, aVF, иногда V1 и V2. Одновременно появляется выраженный отрицательный зубец Т в отведениях V1–V4, а также в II и aVF. Перегрузка правого предсердия может привести к появлению высокого зубца Р в отверстиях II и III (P-pulmonale). Признаки острой перегрузки правого желудочка чаще наблюдаются при эмболии ствола и главных ветвей легочной артерии, чем при поражении долевых и сегментарных ветвей. С помощью ЭхоКГ можно проводить оценку параметров гемодинамики и структурного состояния миокарда, степени выраженности гипертензии малого круга кровообращения, наличия тромботических масс в полостях сердца, исключить пороки сердца и оценить результаты лечения. Наиболее часто обнаруживают дилатацию правых отделов сердца и легочной артерии, парадоксальное движение межжелудочковой перегородки, трикуспидальную регургитацию, отсутствие коллабирования нижней полой вены, открытое овальное окно, что встречается редко. В результатах лабораторных тестов высокий титр D–димера может свидетельствовать о наличии у пациента венозного тромбоза и ТЭЛА лишь в том случае, если исключены другие состояния, протекающие с образованием фибрина, например очаги некроза и воспаления (при заболеваниях органов брюшной и грудной полости, абсцессах, после недавно перенесенных оперативных вмешательств и травм). В то же время, этот показатель может быть использован в качестве метода скрининга в связи с высокой чувствительностью. Однако показателей, однозначно указывающих на возникновение ТЭЛА, не существует. Вероятность ТЭЛА предварительно можно оценить по шкале M.W. Roges и P.S. Wells (2001) [7]: • клинические симптомы тромбоза глубоких вен нижних конечностей – 3 балла; • при проведении дифференциальной диагностики ТЭЛА более вероятна, чем другие заболевания – 3 балла; • тахикардия >100 уд./мин. – 1,5 балла; • иммобилизация или хирургическое вмешательство на протяжении последних 3 дней – 1,5 балла; • тромбоз глубоких вен нижних конечностей или ТЭЛА в анамнезе – 1,5 балла; • кровохарканье – 1 балл; • онкологическая патология в настоящее время или давностью до 6 мес. – 1 балл. Если сумма не превышает 2 баллов, вероятность ТЭЛА низкая; при сумме баллов 2–6 – умеренная; более 6 баллов – высокая. Кроме того, в последние годы в Европе нередко используется так называемая Женевская шкала [4]: • тахикардия ≥95 уд./мин. – 5 баллов; • тахикардия 75–94 уд./мин. – 3 балла; • клинические признаки тромбоза глубоких вен нижних конечностей (боль при пальпации вены + отек одной конечности) – 4 балла; • подозрение на тромбоз глубоких вен нижних конечностей (боль в одной конечности) – 3 балла; • подтвержденные тромбоз глубоких вен нижних конечностей или ТЭЛА в анамнезе – 3 балла; • хирургическое вмешательство или перелом на протяжении последнего месяца – 2 балла; • кровохарканье – 2 балла; • онкологическая патология – 2 балла; • возраст старше 65 лет – 1 балл. Если сумма не превышает 3 баллов, вероятность ТЭЛА низкая; при сумме баллов 4–10 – умеренная; ≥11 баллов – высокая. Основными направлениями лечения ТЭЛА являются гемодинамическая и респираторная поддержка, реперфузия (тромболизис или хирургическое удаление эмболов из легочных артерий), антикоагулянтная терапия. При этом стратегия лечения существенно зависит от степени риска [1, 7]. Антикоагулянтную терапию следует начинать немедленно у пациентов с высокой или средней вероятностью ТЭЛА еще в процессе диагностики, не дожидаясь окончательного подтверждения диагноза. Учитывая высокий риск быстрого развития угрожающих жизни осложнений, необходимость агрессивной терапии и тщательного ее клинико-лабораторного контроля, целесообразно все лечебно-диагностические мероприятия у больных с подозрением на острую ТЭЛА проводить в отделениях интенсивной терапии. Лечение ТЭЛА у пациентов высокого риска: 1. Начинают лечение с быстродействующих прямых антикоагулянтов с последующим, насколько возможно ранним переходом на непрямые. 2. Для профилактики дальнейшего прогрессирования правожелудочковой недостаточности необходимо устранить системную артериальную гипотензию. С этой целью рекомендуется применять вазопрессоры. У пациентов с низким сердечным выбросом и нормальным АД могут быть использованы инотропы, такие как добутамин и дофамин. 3. Не рекомендуется агрессивная инфузионная терапия. 4. Пациентам с гипоксемией необходимо проведение оксигенотерапии. 5. У пациентов высокого риска с ТЭЛА, сопровождающейся кардиогенным шоком и/или артериальной гипотензией, показана тромболитическая терапия. 6. Если тромболизис абсолютно противопоказан или оказался неэффективным, альтернативными методами реперфузии являются хирургическая эмболэктомия и в качестве альтернативного метода реперфузии может рассматриваться также чрескожная катетерная эмболэктомия или фрагментация тромба. Лечение ТЭЛА у пациентов невысокого (умеренного или низкого) риска: 1. Антикоагулянтная терапия. 2. Рутинное использование тромболитической терапии у больных невысокого риска не рекомендовано, но ее целесообразность может быть рассмотрена у некоторых пациентов с умеренным риском. Тромболизис наиболее эффективен у пациентов, которым реперфузия была проведена в первые 48 ч после начала ТЭЛА, однако тромболитическая терапия может быть успешной и у тех больных, у которых первые симптомы ТЭЛА появились 6–14 дней назад. Тромболитическая терапия не показана у пациентов с низким риском. Для тромболитической терапии при ТЭЛА в настоящее время одобрено применение трех препаратов [1]: 1. Стрептокиназа либо по обычной схеме – нагрузочная доза 250 тыс. МЕ (в течение 30 мин.), далее 100 тыс. МЕ в час в течение 12–24 ч, либо по ускоренной – 1,5 млн МЕ в течение 2 ч. 2. Урокиназа либо по обычной схеме – нагрузочная доза 4400 МЕ/кг массы тела (в течение 10 мин.), далее 4400 МЕ/кг массы тела в час в течение 12–24 ч либо по ускоренной схеме – 3 млн МЕ в течение 2 ч. 3. Тканевой активатор плазминогена (альтеплаза): 100 мг в течение 2 ч или 0,6 мг/кг массы тела в течение 15 мин. (максимальная доза 50 мг). В современных условиях особую роль отводят профилактике ТЭЛА, которая, согласно приказу Минздрава РФ от 09.06.2003 № 233 «Об утверждении отраслевого стандарта “Протокол ведения больных. Профилактика тромбоэмболии легочной артерии при хирургических и иных инвазивных вмешательствах”», заключается в следующих мероприятиях: • Выявление пациентов с высокой степенью риска возникновения ТЭЛА. • Максимально ранняя активизация больного в послеоперационном периоде: подъем и активная ходьба (однако противопоказана длительная статическая нагрузка в положении стоя, сидя). • Эластическая компрессия нижних конечностей (бинты эластические или чулки 1 или 2 компрессионного классов). Эластические бинты или чулки используются до операции, во время операции (кроме операций на нижних конечностях) и после операции вплоть до выписки из стационара. • Перемежающаяся пневмокомпрессия (рекомендована к использованию при противопоказаниях к гепаринопрофилактике). • Применение лекарственных препаратов. Алгоритм профилактики прямыми антикоагулянтами заключается в назначении гепарина натрия в суточной дозе 15 000 МЕ, при массе тела ниже 50 кг суточную дозу гепарина снижают до 10 000 МЕ. Гепарин вводят под кожу живота, интервал между инъекциями составляет 8 ч. Продолжительность профилактической гепаринизации – не менее 3 дней. Продолжительное кровотечение служит абсолютным противопоказанием к назначению антикоагулянтов. Алгоритм профилактики непрямыми коагулянтами включает в себя применение низкомолекулярных гепаринов первого поколения: дальтепарина, надропарина, эноксипарина. Эти препараты удобны тем, что могут быть введены подкожно один раз в сутки в дозах 0,6 мл/сут (0,8 мл/сут при массе тела выше 120 кг), 5000 ед/сут (7500 ед/сут при массе тела свыше 120 кг) или 40 мг/сут (60 мг/сут при массе тела выше 120 кг) соответственно. Антиагреганты. При уровне тромбоцитов, превышающем норму, показано назначение антиагрегантов: ацетилсалициловая кислота, тиклопидин, клопидрогел в общетерапевтических дозах. Несмотря на то, что приказ №233 регламентирует использование нефракционированного гепарина и низкомолекулярных гепаринов первого поколения, следует помнить, что в нашем арсенале уже есть препарат низкомолекулярных гепаринов второго поколения. В настоящее время он активно изучается, и количество данных о его клиническом применении ограничено. Тем не менее, уже проведены исследования, характеризующие его эффективность у пациентов после ортопедических, гинекологических и других видов операций. Бемипарин (Цибор®) – это низкомолекулярный гепарин второго поколения. Он обладает самой низкой молекулярной массой, равной 3600 Да и самым продолжительным периодом полувыведения (5,3 ч). Предварительные результаты недавних исследований позволяют предположить, что низкомолекулярные гепарины, в частности бемипарин, могут использоваться для лечения и профилактики тромбоэмболических осложнений, в т.ч. и вне стационара, у пациентов с нетяжелой ТЭЛА и у больных раком [5]. Такая возможность была исследована в двойном слепом многоцентровом исследовании CANBESURE (n=703) [6]. В это исследование были включены пациенты старше 40 лет, которым было проведено хирургическое вмешательство по поводу ранее диагностированных злокачественных опухолей (первичных или метастатических) желудочно-кишечного тракта, мочевыводящих путей или женской репродуктивной системы. В исследование включались только пациенты с ожидаемой продолжительностью жизни не менее 3 мес., у которых операция проводилась под общим наркозом или спинномозговой анестезией и длилась не менее 30 мин. Перед рандомизацией все пациенты получали бемипарин подкожно в дозе 3500 МЕ 1 р/сут в течение 8±2 дня (первая доза вводилась через 6 ч после операции). Затем больных случайным образом разделили на группу продолжения тромбопрофилактики бемипарином в том же режиме в течение дополнительных 20±2 дней и группу плацебо-контроля. Через 28 дней после операции проводилась двусторонняя восходящая венография. Отдаленные результаты наблюдали в течение 3 мес. Главной конечной точкой эффективности служила совокупность симптоматических и бессимптомных тромбозов глубоких вен (ТГВ), нефатальных ТЭЛА, а также случаев смерти от любых причин. Проводился также проспективный учет дополнительной комбинированной конечной точки, включавшей в себя проксимальные ТГВ, симптоматические нефатальные ТЭЛА и случаи смерти по причине ТЭЛА. Главная конечная точка эффективности была зарегистрирована у 10,1% пациентов группы бемипарина и 13,3% больных в группе плацебо. Хотя различия между группами не достигли статистически достоверного уровня (р=0,263), уровень относительного риска развития ТЭЛА в группе бемипарина оказался ниже на 24,4%. Частота наступления дополнительной конечной точки оказалась достоверно ниже в группе бемипарина (0,8% против 4,6%, p=0,016), а относительный риск развития ТЭЛА в группе бемипарина оказался ниже на 82,4% по сравнению с группой плацебо. Риск геморрагических осложнений при продлении тромбопрофилактики бемипарином на 3 нед. достоверно не увеличился. Серьезные кровотечения развились у 0,6% больных группы бемипарина против 0,3% группы плацебо (недостоверные различия, p=0,572). Результаты исследования CANBESURE позволяют сделать вывод, что продленная до 4 нед. тромбопрофилактика бемипарином в дозе 3500 МЕ/сут после абдоминальных или тазовых операций по удалению злокачественных опухолей достоверно снижает риск развития тяжелых тромбоэмболий без повышения риска геморрагических осложнений, по сравнению со стандартным недельным курсом тромбопрофилактики прямыми антикоагулянтами. В заключение следует сказать, что послеоперационная ТЭЛА остается актуальной современной проблемой. Несмотря на наличие большого объема литературных данных, выбор схемы лечения и профилактики послеоперационной ТЭЛА ложится на плечи лечащего врача и зависит от обеспеченности лечебного учреждения.
Литература 1. Котельников М.В. Тромбоэмболия легочной артерии (современные подходы к диагностике и лечению). М., 2002. 2. Макаров О.В., Озолиня Л.А., Пархоменко Т.В., Керчелаева С.Б. Профилактика тромбоэмболических осложнений в акушерской практике // Рос. мед. журн. 1998. № 1. С. 28–32. 3. Darryl Y. Sue, M.D. Pulmonary Disease // Frederic S. Dongard (ed.): Current: Critical Care Diagnosis & Treatment. US – a lange medical book. First Edition. P. 496. 4. Le Gal G., Perrier A. Contemporary approach to the diagnosis of non-massive pulmonary embolism // Curr. Opin. Pulm. Med. 2006..Vol. 12(5). P. 291–298. 5. Martanez-Gonzilez J., Vila L., Rodriguez C. Bemiparin: second-generation, low-molecular-weight heparin for treatment and prophylaxis of venous thromboembolism // Expert. Rev. Cardiovasc. Ther. 2008. Vol. 6(6). P. 793–802. 6. Monreal B.M., Vignoli A., Lecumberri V.R. et al. Bemiparin in oncology // Drugs. 2010. Vol. 70 (Suppl. 2). P. 35–42. 7. Rodger M., Wells P.S. Diagnosis of Pulmonary Embolism // Thromb. Res. 2001. Vol. 103. P. 225–238. 8. Sharma G.V.R.K., Schoolman M., Sasahara A.A. Diagnosis and Treatment of Pulmonary Embolism // Melvin M., Sheinman, M.D. (eds.) Cardiac Emergencies. W.B. Saunders Company, 1984. P. 349. 9. Task Force Report. Guidelines on diagnosis and management of acute pulmonary embolism. European Society of Cardiology // Eur. Heart J. 2000. Vol. 21. P. 1301–1336.
Какими симптомами проявляются тромбоэмболические осложнения?
Такие осложнения, как тромбоз глубоких вен нижних конечностей, характеризуют выраженные болевые ощущения в голени и в стопе, сопровождающиеся синим или фиолетовым цветом кожи ниже места тромбоза. Эти симптомы обусловлены тем, что при закупорке вены кровь не оттекает от конечности, приводя к распирающей боли. Даже незначительный дискомфорт в одной или в обеих конечностях после операции не должен оставаться без внимания врача.
острый тромбоз вен ног
Тромбоэмболия легочной артерии имеет проявления различной степени выраженности. Иногда в силу незначительности симптоматики ТЭЛА мелких ветвей может остаться нераспознанной, приводя к осложнениям со стороны легких и сердца, например, к развитию хронической тромбоэмболической легочной гипертензии.
больной с ТЭЛА
Обычно ТЭЛА мелких ветвей сопровождается приступами сухого кашля или кровохарканья с болью в грудной клетки различной локализации. Часто у пациента отмечаются приступы внезапной одышки и чувство нехватки воздуха. Может присутствовать потеря сознания.
Массивная ТЭЛА характеризуется выраженным болевым синдромом в грудной клетке, одышкой, кровохарканьем и цианозом (посинением) кожи лица, шеи, мочек ушей и груди строго до горизонтальной линии между сосками. Мгновенно может наступить клиническая смерть, без лечения переходящая в биологическую смерть. В некоторых случаях пациент может просто встать и умереть.
Диагностика ВТЭО
Диагноз тромбоза глубоких вен голени или нижней полой вены может быть подтвержден с помощью УЗИ сосудов.
рентген-признаки ТЭЛА (рис.: ННЦ «Институт кардиологии Н.Д. Стражеско»)
ТЭЛА подтверждается с помощью рентгенографии органов грудной клетки, но отсутствие характерных рентгенологических признаков не является обоснованием для исключения диагноза. Другими словами, диагноз тромбоэмболии даже при нормальной рентгенограмме ОГК может быть установлен на основании клинических данных.
Обязательным исследованием при подозрении на ВТЭО является исследование крови на Д-димер, а также исследование свёртывающей системы крови (показатели МНО, фибрин, время свертывания крови, ассоциированное частичное тромбиновое время – АЧТВ, протромбиновое время – ПТВ и протромбиновый индекс – ПТИ).
После комплексной оценки полученных данных начинается лечение.
Лечение тромбоэмболических осложнений
Любому врачу необходимо помнить, что смертность при массивной ТЭЛА без лечения составляет более 90%, поэтому терапию нужно начинать как можно раньше.
Основной принцип лечения заключается в растворении тромба и в коррекции нарушения в свёртываемости крови. В связи с этим в отделении реанимации пациенту внутривенно вводят следующие препараты:
- Низмолекулярные гепарины – гепарин в дозе 31-33 000 ЕД/сут в течение 5-7 дней или эноксапарин в дозе 180 мг/сут в течение 5-7 дней,
- Препараты для проведения тромболизиса – стрептокиназа в дозе 250 000 ЕД в первые 30 минут, затем 100 000 ЕД в первые сутки или альтеплаза в дозе 100 мг в первые сутки.
Из таблетированных препаратов применяется варфарин в дозе 10 мг в течение 5-7 дней.
кава-фильтр, улавливающий тромбы
При наличии показаний пациенту может быть проведено хирургическое лечение тромбозов – установка кава-фильтра в просвет нижней полой вены или эмболэктомия нижней полой вены.
Показаниями для операции являются следующие:
- Рецидивирующая ТЭЛА при проведении адекватной антикоагулянтов терапии,
- Обширный или прогрессирующий тромбоз нижней полой вены,
- Планирующаяся или проведенная операция у пациента с перенесенной ТЭЛА.
Как предотвратить тромбофлебит после операции
Тромбофлебит занимает одно из первых мест в структуре заболеваемости после хирургического вмешательства. Нередко он протекает бессимптомно, и его проявлением становится лишь внезапная тромбоэмболия легочной артерии. Поэтому необходима профилактика тромбофлебита у послеоперационных больных с помощью немедикаментозных методов и лекарственных средств.
Что такое тромбофлебит
Тромбофлебит – сочетание воспаления венозной стенки и образования тромба. Его развитие провоцирует комбинация двух факторов: повышенная свертываемость крови и венозный застой.
| ⇐ Предыдущая12345678Следующая ⇒ профилактические мероприятия в отношении тромбозов вен должны учитывать этиопатогенетические факторы. В связи с этим следует особое внимание уделять больным с повышенным риском возникновения венозных тромбозов. Наибольший процент тромбозов вен и тромбоэмболических осложнений, как было отмечено выше, наблюдается у хирургических больных. В послеоперационном периоде профилактика включает в себя раннюю мобилизацию больных, возвышенное положение конечностей в постели на 20-30° выше уровня кровати, эластичное бинтование конечностей во время операции и в течение всего периода постельного и полупостельного режима. У больных, перенесших острый тромбоз вен или после операций по поводу заболевания вен, длительность эластичного бинтования конечности определяется клинической картиной. Эластичная компрессия, сдавливая подкожные и мышечные вены, значительно ускоряет кровоток по глубоким венам (в 5-7 раз в покое). Лечебная физкультура и дыхательная гимнастика назначаются в дооперационном периоде и в первые часы или сутки после операции.Перемежающая пневматическая компрессия, производимая с помощью специальных аппаратов, значительно снижает частоту послеоперационных тромбозов и эмболии. В настоящее время предложены и применяются в практике различные виды пневмомассажеров. С этой же целью применяется пассивное тыльное сгибание стопы при помощи педали, приводимой в действие мотором. Метод электрического стимулирования мышц голени состоит в следующем: проводится стимуляция мышц каждые 2 с при помощи гальванического тока, передаваемого двумя электродами, один из которых помещается на задней поверхности верхней трети голени, другой – на тыльной поверхности стопы. Интенсивность тока регулируется таким образом, чтобы получить быстрое негрубое сгибание стопы, что обеспечивает перемежающее проталкивание крови по венам голени.Специфическая профилактика включает в себя антитромботическую терапию и проводится больным с разными факторами риска.К другим профилактическим мерам операционных и послеоперационных тромбозов относятся: устранение тканевой гипоксии и водно-электролитных нарушений, своевременное восстановление нормальных величин ОЦК, предупреждение гипотензий, адекватное обезболивание при операции. 117. ДВС-синдром у хирургических больных. Меры профилактики, основные принципы лечения ДВС-синдрома.ДВС-синдром – наиболее распространенный вид патологии гемостаза. Его основой является генерализованное свертывание крови в сосудах микроциркуляторного русла с образованием большого количества микротромбов и агрегатов кровяных клеток. При этом происходит блокировка нормального кровообращения в большинстве органов и систем, приводящая к развитию в них глубоких дистрофических изменений. Вслед за интенсивным свертыванием крови развиваются гипокоагуляция (снижение способности крови к свертыванию), тромбоцитопения (снижение количества тромбоцитов в единице объема крови) и геморрагии (кровотечения).
Вместе с тем тяжесть, распространенность и скорость развития ДВС-синдрома очень разнообразны – от молниеносных смертельных форм до латентных (скрытых) и затяжных, от генерализованного свертывания крови до региональных и органных тромбогеморрагий.Лечение ДВС-синдрома:Лечение ДВС-синдрома зависит от стадии процесса. В первую очередь необходимо устранить причину, вызвавшую активацию тром – бокиназы (тромбопластина). Если видимая причина отсутствует, то необходимо начать посиндромную терапию, направленную на восстановление адекватной гемодинамики, микроциркуляции, дыхательной функции легких, коррекции метаболических нарушений. ВI стадии ДВС-синдрома рекомендуется (обязательно!) применять гепарин по 100—400 ЕД/кг (суточная доза) подкожно 3— 6 раз в сутки или внутривенно путем постоянной инфузии (от 400—500 до 2000 ЕД/ч и более) через дозатор.
Введенный непосредственно в плазму гепарин из расчета 0,1—0,25 ЕД/мл повышает активность AT-III по отношению к факторам Ха и 1Ха в 1000(!) раз, обрывает процесс внутрисосудистого свертывания и тем самым не дает развиться коагулопатии потребления. Для нормализации реологических свойств крови и улучшения микроциркуляции в последнее время широко рекомендуется применение 6% или 10% оксиэтилированного крахмала до 10 мл/кг или реополиглюкина в той же дозировке. С этой же целью назначают: внутривенно курантил 10—20 мг в сутки, папаверин 3—5 мг/кг (в сутки), компламин 10—20 мг/кг в сутки. Во II стадии ДВС-синдрома доза СЗП увеличивается до 10— 15 мл/кг в сутки. Гепарин в микродозах добавляется только в СЗП. Переливание сухой плазмы и фибриногена противопоказано(!). Введение СЗП следует проводитьструйно. В III стадии (гипокоагуляции) показано введение ингибиторов протеаз (контрикал, трасилол — 1000—2000 Атр ЕД/кг массы телаОдним из наиболее перспективных и безопасных методов лечения ДВС-синдрома является лечебный плазмаферез. Его эффект обусловлен деблокированием системы мононуклеарных фагоцитов и выведением из кровотока продуктов коагуляции и фибринолиза, белков «острой фазы» воспаления, циркулирующих иммунных комплексов и других соединений, обуславливающих развитие синдрома эндотоксикоза. Эксфузируют не менее 70—90% ОЦП с возмещением СЗП в полном объеме. ⇐ Предыдущая12345678Следующая ⇒ Данная страница нарушает авторские права? | |
| Причины повышения свертываемости: | Причины венозного застоя: |
|
|
При сочетании этих факторов на поврежденной сосудистой стенке в условиях замедленного кровотока скапливаются тромбоциты, которые окутываются плотной сетью фибрина и образуют тромб.
Такой сгусток может оторваться от своего основания и попасть в сердце, а через его камеры – в систему легочной артерии.
Так развивается тромбоэмболия легочной артерии – опасное для жизни состояние.
Почему вероятность развития заболевания выше после операции
У большинства больных после хирургического вмешательства имеется несколько из перечисленных факторов развития тромбофлебита. Самый важный из них – обездвиживание пациента.
Наиболее высока вероятность тромбофлебита у пациентов после эндопротезирования суставов, поскольку в этом случае имеется и непосредственное травмирование сосудов. При операциях неортопедического характера степень риска тромбоза определяется сочетанием факторов свертывания крови и типом операции.
Разработаны критерии, согласно которым вероятность тромбофлебита делится на три степени:
- низкая (до 10%) – при длительности операции до 30 минут и отсутствии неблагоприятных факторов, помимо возраста, а также при длительности вмешательства более 30 минут у пациентов моложе 40 лет без других условий риска;
- средняя (10 – 40%) – продолжительные операции на внутренних органах, возраст больного старше 40 лет или другие отрицательные факторы, операции короче 30 минут у пациентов с перенесенным ранее тромбофлебитом;
- высокая (40 – 80%) – переломы или ортопедические операции на нижних конечностях, операции при онкологических заболеваниях, паралич нижних конечностей, ампутация конечностей.
Одним из факторов тромбоза является повреждение вен. Так, течение послеоперационного периода может осложнить тромбофлебит после катетера.
Меры профилактики тромбофлебита
В зависимости от группы риска заболевания используются немедикаментозные и лекарственные способы его предотвращения.
Профилактика тромбоза вен нижних конечностей
Перечисленные ниже способы показаны не только при ортопедических, но и при любых других вмешательствах, связанных с риском тромбообразования:
- ранняя активация пациента, усаживание в кровати в первый день после операции;
- эластическое бинтование или использование компрессионных чулок перед операцией и после нее;
- пневматическая компрессия с помощью наложенных на нижние конечности манжет, в которые периодически нагнетается воздух;
- при очень высоком риске – имплантация кава-фильтра – «ловушки для тромбов», устанавливаемой хирургическим путем в просвет нижней полой вены.
Профилактика после операции
Помимо перечисленных выше мер немедикаментозной профилактики врачи используют лекарственные препараты:
- нефракционированный гепарин применяется при умеренном риске тромбоза;
- низкомолекулярные гепарины («Фраксипарин», «Клексан» или «Фрагмин») являются препаратами выбора для предупреждения тромбофлебита;
- фондапаринукс («Арикстра») показан при высоком тромбоэмболическом риске при ортопедических операциях;
- «Варфарин».
Эти лекарственные средства назначаются в течение недели, некоторые из них требуют лабораторного контроля показателей свертывания крови (гепарин, варфарин).
Онкологическим больным рекомендуют продолжать введение низкомолекулярных гепаринов в течение как минимум месяца после вмешательства.
Тромбофлебит после катетера: лечение и профилактика заключаются в смазывании кожи над местом катетеризации гепарин-содержащими препаратами, промывании катетера гепаринизированным раствором, регулярном осмотре места катетеризации.
Предупреждение обострения заболевания
Чтобы избежать обострения тромбофлебита, необходимо проводить его профилактику. Особенно это касается людей, которым предстоит оперативное вмешательство. Им рекомендуется:
- избегать полной неподвижности;
- при постельном режиме держать ноги на валике высотой 15 – 20 см;
- пить больше жидкости;
- не подвергать ноги перегреванию;
- использовать компрессионный трикотаж;
- по назначению врача принимать венотонические препараты и средства, улучшающие текучесть крови.
Рекомендуем прочитать статью о тромболитической терапии. Из нее вы узнаете о показаниях к тромболизису, методике проведения процедуры, возможных осложнениях.
Народные методы борьбы с тромбофлебитом после операции
Ни один из народных методов не будет столь же эффективен, как медикаментозная профилактика тромбообразования. Однако можно использовать такие способы:
- компресс на голени из капустных листьев;
- растирание настойкой цветков сирени и каштана на спирте;
- содовые компрессы;
- выполнение упражнений с сокращениями икроножных мышц (подъем «на цыпочки», сгибание и разгибание стоп);
- употребление внутрь настоя череды, зверобоя, кориандра, ромашки по 100 мл дважды в день.
Профилактика тромбообразования после хирургических операций основана на ранней активизации больного, использовании компрессионного трикотажа, лекарственных средствах, лечебной физкультуре. Дополнительно могут применяться и народные рецепты, улучшающие кровоток в венах нижних конечностей.
Источник: https://CardioBook.ru/profilaktika-tromboflebita-u-posleoperacionnyx-bolnyx/