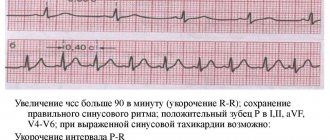
Для растворения тромба используют ферментные препараты, способные разрушать нити фибрина. Их применяют в первые часы после инсульта, инфаркта миокарда, легочной тромбоэмболии. Введение происходит обычным внутривенным способом или локальным подведением медикамента к тромбу. Самым частым и тяжелым последствием тромболитической терапии является кровотечение.
Что это такое?
Тромболизис при инфаркте миокарда представляет собой медицинскую процедуру введения в сосудистое русло человека того или иного ферментного препарата, способствующего растворению тромба, препятствующего нормальному кровообращению. В настоящее время разработано достаточно большое количество лекарственных средств, используемых для тромболизисной терапии. С каждым годом число данных процедур в повседневной медицинской практике только увеличивается. Это позволяет значительно увеличить выживаемость и качество жизни пациентов с инфарктом миокарда. Если тромболизис не выполнялся, то после проведенного лечения людям нередко приходится выходить на инвалидность.
Способы выполнения тромболизиса
Тромболизис проводят двумя основными методами:
локальный тромболизис
- Системным;
- Локальным.
Первый способ выгоден тем, что лекарство можно ввести в вену, не имея представления, где затаился тромб. С током крови препарат разносится по всему кругу кровообращения, где на своем пути встречает препятствие в виде кровяного сгустка и растворяет его. Но у системного тромболизиса есть существенный недостаток: необходима повышенная доза лекарства, а это дополнительная нагрузка на всю кровеносную систему.
При проведении локального тромболизиса препарат вводится непосредственно в место локализации тромба. Препарат подается через катетер, поэтому метод так и назвали – катетерный тромболизис. Тем не менее, этот способ сложнее первого в исполнении и сопряжен с определенной опасностью. При выполнении процедуры доктор наблюдает за движением катетера с помощью рентгена. Преимущество этого метода в малой инвазивности. Его применяют даже в случае наличия большого количества хронических заболеваний у пациента.
Показания к применению при инфаркте миокарда
Со временем корректируется набор клинических состояний, при которых рекомендована тромболизисная терапия. В настоящее время показания к тромболизису при инфаркте миокарда следующие:
- наличие повышения сегмента ST на электрокардиографии, а также других признаков острого инфаркта миокарда;
- не более 12 ч со времени возникновения ишемических болей;
- впервые возникшая полная блокада правой ножки пучка Гиса на фоне ишемических болей в загрудинной области.
Если соблюдены все эти условия, то медицинский работник начинает проводить тромболизис при инфаркте миокарда. Оценка возможности проведения данной процедуры должна выполняться при первом контакте пациента с характерными жалобами с медицинским работником.
ТРОМБОЛИТИЧЕСКАЯ ТЕРАПИЯ ИНФАРКТА МИОКАРДА
В статье обобщен мировой опыт использования тромболитических препаратов при остром инфаркте миокарда, приведены данные о сравнительной эффетивности различных препаратов для тромболитической терапии. Основной акцент сделан на раннее начало лечения. Даны рекомендации для корригирования осложнений тромболитической терапии.
The paper summarizes worldwide experience in using thrombolytics in the treatment of acute myocardial infarction, provides evidence for comparative efficacy of different drugs for thrombolytic therapy. Great emphasis is laid on early treatment. Recommendations are given for correction of complications due to thrombolytic
therapy.
И.Н. Бокарев, С.А. Довголис. Московская медицинская академия им. И.М. Сеченова I.N. Bokarev, S.A. Dovgolis I.M. Sechenov Moscow Medical Academy
И
нфаркт миокарда (ИМ) – самое частое и грозное патологическое состояние, требующее неотложного медицинского вмешательства. Еще в начале 60-х годов оно приводило к быстрой смерти 30-50% заболевших. Создание палат интенсивной терапии, оборудованных аппаратурой для мониторного наблюдения за нарушениями ритма, в сочетании с внедрением электроимпульсной терапии и новых противоаритмических препаратов снизило смертность от ИМ почти наполовину. Тромболитические препараты, которые на сегодня являются главными в лечении ИМ, позволили в ведущих клиниках мира снизить смертность от этого заболевания до 7% и даже до 5%. Тромболитические препараты были впервые применены в клинической практике благодаря стараниям В. Тиллета и С. Шерри еще в 1949 г. а в 1958 г. тот же С. Шерри вместе с А. Флетчером и Н. Алкерсиг уже доложили об успешном применении стрептокиназы (СК) для лечения больных ИМ. Однако необходимость тромболитических препаратов при этой патологии была всеми признана лишь после 1989 г. Несомненные заслуги отечественных ученых в области практического применения тромболитической терапии хорошо известны в мире. В 1961 г. отечественный фибринолизин, созданный Г.В. Андреенко под руководством Б.А. Кудряшова, был впервые применен в клинике А.Л. Мясникова Е.И. Чазовым. Е.И. Чазову принадлежит мировой приоритет внутрикоронарного введения тромболитика больному ИМ в 1976 г.
Как обстоит дело с тромболитической терапией ИМ сегодня, и что должен знать об этом каждый практический врач?Тромбоз лежит в основе ИМ почти в 95% случаев.
Обычно он развивается после разрыва атеросклеротической бляшки. Бляшки с большой липидной «сердцевиной» и инфильтрацией макрофагами фиброзной поверхности особенно подвержены разрыву.
Гибель клеток миокарда происходит в направлении от субэндокарда к эпикарду.
Основными факторами, определяющими конечный размер ИМ, являются время до реперфузии миокарда и развитость коллатерального кровотока.
Это определяет лечебную тактику, цель которой – достижение ранней и стойкой реперфузии окклюзированного сосуда, результатом чего будут сохранение миокарда, уменьшение распространения ИМ и снижение электрической нестабильности миокарда. Восстановление проходимости поврежденного сосуда способствует улучшению остаточной функции левого желудочка (ЛЖ), уменьшению смертности, осложнений ИМ и улучшению выживаемости. Реперфузия может ограничить распространение ИМ несколькими путями. Она уменьшает величину, до которой расширяется зона ИМ, и величину, до которой удлиняется перинфарктная зона. Даже при отсутствии уменьшения размера ИМ сохранение слоя эпикарда может способствовать тому, что пораженная зона будет меньше растягиваться. Путь заживления инфарцированного миокарда может быть настолько же важным, как и первоначальное уменьшение размера ИМ. Поздняя реперфузия ишемизированного инфаркта миокарда также вызывает уменьшение некроза мышечных пучков и сохранение сократительной функции миокарда. Наконец, реперфузия может уменьшить риск электрической нестабильности. Ранняя смерть при ИМ наступает внезапно в результате фибрилляции желудочков. Больные, у которых произошла реперфузия, по данным электрофизиологического исследования, в меньшей степени страдают желудочковыми аритмиями, и у них реже наблюдается нарушение поздней реполяризации на ЭКГ. Известно, что влияние реперфузии на уменьшение размера ИМ улучшает выживаемость, однако на отклонение от линейной зависимости между ранней реперфузией и смертностью, видимо, влияют несколько факторов. Чтобы реперфузия была максимально полезна, она должна быть не очень ранней, но длительной. Реокклюзия сопровождается удвоением риска смерти. Различия между отдельными тромболитическими препаратами в уровне реокклюзии трудно установить, для этого нужны большие исследования. Было изучено несколько путей введения троболитических препаратов от внутрикоронарного тромболизиса до внутривенного введения как в стационарах, так и на дому. Большие клинические исследования ясно показали, что внутривенный тромболизис связан с более низким уровнем смертности у больных с острой болью в грудной клетке и подъемом ST в первые 12 ч от появления симптомов.
Доказательства эффективности.
| В настоящее время в мире применяют следующие типы тромболитических средств: стрептокиназу (СК), урокиназу, ацилированный комплекс плазминогена с СК (АПСАК) и тканевый активатор плазминогена (ТАП). Последний имеет некоторые преимущества, но высокая стоимость препарата ограничивает его применение. |
Отечественный фибринолизин оказался менее эффективным и в настоящее время не производится. Сравнительные исследования тромболитической терапии с плацебо четко показали уменьшение смертности на 25-30% независимо от применяемого тромболитического препарата. В настоящее время проведено 10 больших проспективных рандомизированных исследований по оценке влияния раннего тромболизиса на смертность. Исследование GISSI-1 (первое кооперированное итальянское испытание тромболитических средств при ИМ), большое исследование по раннему внутривенному тромболизису явилось вехой, которая отметила начало эры рутинного применения тромболитических препаратов у больных в раннем периоде острого (ОИМ). В этом исследовании 11 712 больных, доставленных в первые 12 ч ОИМ и не имевших противопоказаний к тромболитической терапии, после рандомизации получали лечение внутривенной инфузией 1 500 000 ЕД СК в течение 1 ч или обычное лечение без СК. Смертность за 21 день в группе получавших СК составила 10,7% по сравнению с 13% в контрольной группе (уменьшение смертности на 18%, р = 0,0002). Не было отмечено эффекта у больных, леченных СК позднее 6 ч от начала болей. У леченных в течение 6 ч уровень смертности был 10,2% по сравнению с 12,8% в контрольной группе (уменьшение смертности на 20%). Чем раньше было начато лечение, тем выше была его эффективность. Так, у больных, которых начали лечить в период 3 – 6 ч, СК приводила к снижению смертности на 17% (с 14,1 до 11,7%). Если его начинали в период от 0 до 3 ч, то снижение смертности составило 23% (с 12 до 9,2%). У леченных в 1-й час от начала симптомов снижение смертности достигало 47% (с 15,4 до 8,2%). ISIS-2 (второе международное исследование, посвященное изучению выживаемости при ИМ) также было очень важным. Исследователи сообщили исходные и конечные данные о 17 187 больных с подозрением на ОИМ, включенных в исследование в течение 24 ч от начала болей. Больные были рандомизированы двойным слепым методом. Изучали эффект внутривенного введения СК (1 500 000 ЕД за 60 мин) или аспирина внутрь (160 мг в день в течение 1 мес), или и того и другого. Больных исключали из исследования, если прошло более 24 ч от появления симптомов. Не было ограничений по возрасту. Изучали влияние СК на уровень сердечно-сосудистой смертности за 5 нед и позже, влияние на сердечно-сосудистую смертность за 5 нед. Кроме того, анализировали влияние СК на сердечно-сосудистую смертность у леченных ранее 4 ч от начала болей, у леченных в период 4–12 ч и в период 12 – 24 ч. При анализе смертности за 5 нед от момента включения было обнаружено, что из 8592 больных, леченных СК, от сердечно-сосудистых причин умерли 786 (9,1%) по сравнению с 1016 из 8592 больных, леченных плацебо (снижение смертности на 23%, р<0,00001). Эта разница соизмерима с 18% снижением смертности в исследовании GISSI-1. За период от 5 нед до 1 года уровень смертности в группе СК и плацебо был соответственно 5,7 и 6,2%. В ISIS-2 только у 56% больных исходно наблюдался подъем ST, у 8% была депрессия ST, у 6% – блокада ножки пучка Гиса, у 27% – Q-зубец или инверсия зубца Т, или то и другое, у 2% ЭКГ была в норме. Исследования GISSI-1 и ISIS-2, а также исследования, проведенные в Нидерландах, ФРГ, Новой Зеландии, штате Вашингтон, представили убедительные доказательства того, что СК, введенная в ранние сроки ИМ больным без противопоказаний, уменьшает смертность на 20-30%. Аналогичные данные были получены для ТАП и АПСАК. В исследовании ASSET (англо-скандинавское исследование раннего тромболизиса) 5011 больных с подозрением на ОИМ в первые 5 ч от начала болезни после рандомизации получали 100 мг альтеплазы (rТАП; 10 мг болюс, 50 мг в 1-й час, по 20 мг во 2-й и 3-й час) или плацебо. Организаторы ASSET не придерживались ЭКГ-критериев диагностики ИМ, но исключали больных старше 75 лет. Около 18% больных при включении в исследование имели нормальную ЭКГ. Через 1 мес общий уровень смертности в группе лечения составил 7,2% по сравнению с 9,8% в группе плацебо (уменьшение смертности на 26%, р = 0,0011). Европейская кооперативная группа сообщила о рандомизированном двойном слепом изучении эффективности rТАП (100 мг) у 721 больного с болью в грудной клетке и подъемом сегмента ST в первые 5 ч от начала болей. Обе группы получали аспирин и гепарин. Исследователи изучали влияние лечения на функцию ЛЖ. Смерть в течение 14 дней и смерть в течение 3 мес были приняты в качестве вторичных конечных точек. 14-дневная летальность составила 2,8% (10 из 355) в группе rТАП и 5,7% (21 из 366) в группе плацебо. Наблюдалось снижение смертности на 51% (p = 0,06). Фракция выброса (ФВ) оказалась в 2,2 раза выше в группе rТАП по сравнению с группой плацебо (соответственно 50,7 и 48,5). Размер ИМ, оцениваемый по общему высвобождению гидроксибутиратдегидрогеназы, был меньше на 20% в группе гТАП (р = 0,0018). Британская исследовательская группа AIMS провела многоцентровое двойное слепое плацебо-контролированное исследование влияния АПСАК (30 ЕД внутривенно за 5 мин) у больных моложе 70 лет, поступивших не позже 6 ч от начала болей с подъемом сегмента ST на ЭКГ. Комитет, мониторировавший данные, рекомендовал преждевременное прекращение исследования после повторного анализа промежуточных данных, когда было набрано 50% предполагаемого числа пациентов. В предварительном сообщении о 1004 больных 30-дневная смертность составила 12,2% (61 из 502) в группе плацебо и 6,4% (32 из 502) в группе АПСАК (р = 0,0016). Общее уменьшение смертности среди больных, включенных в исследование в интервале 4 – 6 ч от начала болезни, составило 47%, снижение было значительно больше у включенных в исследование в первые 4 ч (соответственно 52 и 41%). Общая польза лечения сохраняется и даже увеличивается в период между 30 днями и 1 годом. Смертность за 1 год составила 19,4 и 10,8% соответственно в группах плацебо и АПСАК (уменьшение смертности на 44%; р = 0,0006). Однако есть данные, говорящие о том, что терапия СК и АПСАК имеет равную эффективность. В двух исследованиях – European Cooperative Study и TIMI (Thrombolysis in Myocardial Infarction) – сравнивали влияние rТАП и СК на проходимость артерий или на уровень реперфузии. В Европейском кооперативном исследовании 129 больных получали или rТАП, или СК в среднем через 3 ч после начала ИМ. Проходимость инфарцированной артерии изучали через 90 мин после начала инфузии, она составляла соответсвенно 70 и 55% (р = 0,058). В рамках исследования TIMI также применялась rТАП и проводилась артериография перед началом лечения. Авторы наблюдали 70 и 43% уровень проходимости артерии через 90 мин после начала инфузии соответственно rТАП и СК у 290 больных, леченных в среднем через 4,75 ч после начала болей. Таким образом, уровень проходимости артерий в двух исследованиях был идентичен для гТАП (70%) и минимально отличался для СК (55% в Европейском кооперативном исследовании и 43% в TIMI). В исследовании TIMI из 232 больных с окклюзированной артерией реперфузия в течение 90 мин наблюдалась у 62 и 31% больных, леченных соответственно rТАП и СК. В обоих исследованиях при применении rТАП изменения свертывающей системы были незначительными, хотя геморрагические осложнения наблюдались при лечении как СК, так и rТАП (в основном формирование гематом в месте пункции артерий). Вывод однозначен: под влиянием rТАП и СК происходит тромболизис с последующей реперфузией, ограничением размера ИМ и улучшением ремоделирования ЛЖ, что, очевидно, является механизмом уменьшения смертности. Имеется линейная зависимость между смертностью и временем от появления симптомов до начала тромболитической терапии.
Исследование FTT (Fibrinolitic Therapy Trialists) показало зависимость лишь до 12 ч от появления симптомов. В течение 1-го часа после появления симптомов эффект тромболитических препаратов менее значим, его максимум выявлен при введении лекарства через 2 – 3 ч от начала болезни. Затем польза от лечения четко уменьшается с увеличением времени от появления симптомов. Эффект позднего тромболизиса при ОИМ, т. е. лечения, начатого после 6 ч от появления симптомов, остается не до конца ясным. В исследовании ISIS-2 среди больных, леченных в первые 4 ч, уровень смертности в группах СК и плацебо составил соответственно 8,2 и 12,1% (уменьшение на 32%). Среди больных, леченных в период 4 – 12 ч, смертность от сердечно-сосудистых причин составила соответственно 10,3 и 11,8% (уменьшение на 13%) и среди больных, леченных в период 12 – 24 ч, – 10,7 и 10,8% (уменьшение на 0,9%). Среди больных, леченных в течение 1 ч, 5-недельная смертность в группе СК уменьшилась на 42% (аналогично уменьшению 3-недельной смертности на 47% в исследовании GISSI-1). Исследование LATE (влияние отсроченного тромболизиса на выживаемость при ИМ), организованное для решения вопроса о пользе позднего тромболизиса при применении ТАП, показало следующее. 5711 больных с симптомами и параметрами ЭКГ, характерными для ОИМ, рандомизированно получали альтеплазу (100 мг внутривенно за 3 ч) или плацебо между 6 – 24 ч от начала симптомов. Обе группы больных получали аспирин. Их наблюдали в течение 6 мес, а 73% – в течение 1 года. Анализ выживаемости выявил уменьшение смертности в группе альтеплазы (397 / 2836 смертей) по сравнению с плацебо (444 / 2875). Смертность за 35 дней составила соответственно, 8,86 и 10,31%, относительное уменьшение на 14,1%. Дополнительный анализ выживаемости при лечении до 12 ч от появления симптомов показал значительное уменьшение смертности при использовании альтеплазы: смертность за 35 дней составила 8,9% против 11,97% для плацебо, относительное уменьшение на 25,6% (р = 0,0299). Для леченных в период 12 – 24 ч уровень смертности был равен соответственно 8,7 и 9,2%, что позволяет предположить наличие некоторой пользы при лечении позже 12 ч. Данное исследование показало, что время начала тромболизиса альтеплазой может быть увеличено до 12 ч от появления симптомов ОИМ.
| Польза фибринолитической терапии отмечалась у всех, кроме больных с депрессией ST. Абсолютная польза была наибольшей в подгруппах с наибольшим риском, определяемым гемодинамическими маркерами больших инфарктов или общими факторами, такими как более старший возраст. Исследования показали, что степень подъема ST является маркером потенциальной пользы тромболитических препаратов. Больные с большим подъемом ST должны надеяться на наибольший эффект от данного лечения. |
Вопрос о зависимости эффективности тромболитической терапии от локализации ИМ
представлялся важным, так как почти всегда можно точно определить локализацию ИМ: переднюю, боковую, нижнюю или циркулярную в зависимости от локализации подъема ST на первой ЭКГ. Гораздо труднее выявить наличие истинного нижнего Q-инфаркта у больных, поступивших с депрессией ST в передней стенке. В исследовании GISSI-I и других выявлено, что при переднем ИМ уровень смертности более высокий и поэтому больные с передним ИМ получают наибольшую пользу от тромболитической терапии. Эффективность тромболитической терапии у больных с нижним ИМ менее очевидна в исследовании GISSI-1, но была показана польза от применения СК и аспирина в ISIS-2. У больных с передним ИМ, получавших тромболитическую терапию, выявлено уменьшение смертности на 30% по сравнению с 15% у больных с нижним ИМ. В то же время многие клиницисты считают, что тромболитическая терапия показана больным с гипотензией, кардиогенным шоком, особенно больным с нижним ИМ и вовлечением правого желудочка.
Анализ эффективности тромболитической терапии в зависимости от возраста
показал следующее. У больных моложе 55 лет риск для жизни без тромболитической терапии не очень высок. Абсолютная польза лечения увеличивается с возрастом пациентов. Почти 50% всех смертей больных, госпитализированных по поводу ОИМ, приходится на возрастную группу старше 75 лет. В исследованиях тромболитической терапии, кроме ISIS-2 и GISSI-1, исключали больных старше 70 лет (AIMS) или 75 лет (ASSET, Eur. Coop. Study). В исследовании ISIS-2 показано снижение смертности при использовании СК на 16% за 5 нед (18,2 и 21,6%) в группе больных старше 70 лет, на 26% (10,6 и 14,4%) в группе больных 60-69 лет и на 28% (4,2 и 5,8%) в группе больных моложе 60 лет. В исследовании GISSI-1 сообщается об уменьшении смертности на 13% через 3 нед в группе больных старше 75 лет, на 8% в группе 65-75 лет и на 26% в группе не старше 65 лет. Здесь же показано, что риск кровотечений не зависит от возраста.
В настоящее время ведутся работы по объективизации эффективности старых и созданию более эффективных новых тромболитических препаратов. Чтобы доказать преимущества нового лекарства перед его предшественниками того же класса, требуется исследование с участием по крайней мере 20 000 пациентов.
Два больших исследования – GISSI-2 (20 891 больной) и ISIS-3 (41 229 больных) – были организованы для выявления преимуществ альтеплазы перед СК (GISSI-2) или альтеплазы и анистреплазы перед СК (ISIS-3). В обоих исследованиях была выявлена одинаковая летальность при лечении разными тромболитическими препаратами. Применение СК сопровождалось значительно меньшей частотой возникновения инсультов по сравнению с таковой при использовании анистреплазы и альтеплазы.
Частота (в %) побочных проявлений при проведении тромболитической терапии
| Осложнение | GISSI-1 (5860; СК) | ISIS-2 (8592; СК) | ASSET (2512; ТАП) |
| Большое кровотечение | 0,3 | 0,5 | 1,4 |
| Малое кровоточение | 3,7 | 3,5 | 6,3 |
| Аллергическая реакция | 2,3 | 4,4 | 0 |
| Анафилаксия | 0,1 | 0 | 0 |
| Гипотензия | 3,0 | 10,0 | НР |
| Инсульт | 1,1 | 0,7 | 1,1 |
| Внтричерепное давление | НР | 0,1 | 0,3 |
Примечание. НР — не регистрировалось.
Исследование INJECT имело целью определить, влияет ли новый препарат ретеплаза (рекомбинантный активатор плазминогена) на смертность так же, как и СК. 6010 больных рандомизированно получали ретеплазу (3004 больных) или СК (3006 больных). В обеих группах лечения в течение 6 мес получены одинаковые результаты в плане частоты эпизодов кровотечения, расширения или рецидивирования ИМ и внутрибольничных инсультов с последующей нетрудоспособностью. У леченных ретеплазой отмечено меньше случаев ишемии и несколько больше аллергических реакций. Количество диагностированных инсультов было выше среди леченных ретеплазой, но у ряда больных, леченных СК, инсульты также имели место. Смертность в течение 35 дней у больных, леченных ретеплазой, была приблизительно на 0,5% ниже, чем при лечении СК. В двух ангиографических исследованиях RAPID 1 и RAPID 2 с участием 324 больных оценивали проходимость сосуда после ОИМ при лечении ретеплазой или альтеплазой. В исследовании RAPID 1 изучали различные режимы введения ретеплазы по сравнению с 3-часовой инфузией альтеплазы. В исследовании RAPID 2 сравнивали двойной болюсный режим ретеплазы с ускоренным введением (инфузия в течение 90 мин) альтеплазы. Результаты этих исследований показали, что ретеплаза открывает больше артерий и быстрее, чем альтеплаза. Ангиография через 60 и 90 мин показала более высокий уровень проходимости и в 3 раза больший уровень перфузии миокарда при применении ретеплазы по сравнению с таковыми при использовании альтеплазы. В RAPID 1 через 90 мин уровень перфузии составил 63% для ретеплазы по сравнению с 49% для альтеплазы (р < 0,05), в RAPID 2 уровень перфузии был равен соответственно 60 и 45% (р < 0,05). Ретеплаза была более удобной и простой в применении, не было неожиданных осложнений. Ангиографический профиль для ретеплазы, продемонстрированный в этих двух исследованиях, позволяет предполагать, что этот новый тромболитический препарат обладает преимуществами перед альтеплазой; примечательно, что его применение может привести к более ранней и более полной проходимости коронарной артерии. В двух недавних исследованиях, проведенных в Европе, GREAT (исследование по раннему введению анистреплазы) и EMIP (Европейский проект по ИМ), показаны возможность, безопасность и эффективность ранней тромболитической терапии перед поступлением в больницу. В исследовании GREAT анистреплазу (АПСАК) вводил врач общей практики на дому. В EMIP этот же препарат вводился персоналом скорой помощи. В обоих исследованиях догоспитальное введение уменьшало время между появлением симптомов и началом тромболитической терапии и сопровождалось более низким уровнем смертности. Последние данные, полученные в исследовании Европейской кооперативной группы, показали, что польза от тромболитической терапии сохраняется по крайней мере 5 лет. Дополнительные преимущества могут быть получены при применении новых методов тромболизиса, заключающихся в ускоренном введении тромболитических препаратов, в частности СК и ТАП.
В 1993 г. в исследование GUSTO (глобальные применение СК и ТАП на окклюзированных артериях) был включен 41 021 больной; эти больные рандомизированно получали альтеплазу (ускоренное введение) и гепарин внутривенно; комбинацию альтеплаза, СК и гепарин внутривенно; СК и гепарин внутривенно; СК и гепарин подкожно. Впервые показано, что новая методика тромболитической терапии, заключающаяся в ускоренном введении ТАП, уменьшает смертность еще на 15% по сравнению с СК и незначительно увеличивает риск внутричерепного кровоизлияния. Исследователями были получены ожидаемые и неожиданные результаты. Ускоренный режим введения ТАП сопровождался быстрым восстановлением перфузии и кровотока III степени по TIMI по сравнению с любым режимом введения СК. Многочисленные измерения показали лучшую систолическую функцию ЛЖ после ускоренного введения ТАП. Кроме того, на фоне ускоренного введения ТАП уровень смертности на 30-й день и через 1 год был ниже, что эквивалентно сохранению 10 и 11 жизнй на 1000 леченых больных. Мы тоже сообщали о подобных наблюдениях при лечении 190 больных, поступивших по поводу острого ИМ с зубцом Q в первые 6 ч от начала заболевания. Всем больным проводилась тромболитическая терапия СК. 160 больным (1-я группа) СК вводили по стандартной методике (1 500 000 ЕД внутривенно в течение 1 ч), а 30 больным (2-я группа) – по быстрой схеме (750 000 ЕД в 20 мл физиологического раствора за 5 – 7 мин). Тромболизис был признан эффективным у 110 (68,8%) больных 1-й группы и у 25 (83,3%) больных 2-й группы. Ранние ретромбозы (до 180 мин) возникли соответственно в 7 (4,4%) и 2 (6,7%) случаях. Госпитальная летальность составила 15 (9,4%) случаев в 1-й группе и 2 (6,7%) случая во 2-й. Не было достоверных различий между группами по частоте рецидивов ОИМ, острой аневризмы, стенокардии, недостаточности кровообращения, аритмий и блокад. Применяемые в настоящее время методы тромболизиса не гарантируют реперфузию миокарда. Ранняя и полная реперфузия достигается менее чем у 50% больных через 90 мин после начала лечения, и реокклюзия происходит примерно у 20 – 25% болных в течение 1-го года наблюдения. Более того, только 3 – 4% больных получают тромболитический препарат в течение 1-го часа появления симптомов, когда польза может быть максимальной. Поэтому необходимость совершенствования подходов к лечению ОИМ не вызывает сомнений.
Схема проведения тромболитической терапии при ИМ
Показания
• Боль в грудной клетке, типичная для острой ишемии миокарда, длительностью до 12 ч. Боль не устраняется нитратами и не имеет явной причины внесердечного происхождения. Позже 12 ч тромболизис следует проводить пациентам с наиболее неблагоприятным прогнозом, у которых можно ожидать наибольшей пользы (старше 75 лет, в случаях обширного поражения, продолжающихся ангинозных болей, артериальной гипотензии). В этих случаях можно рассчитывать на спасение 10 жизней на 1000 леченых. • Изменения на ЭКГ: – недавно или предположительно недавно появившиеся зубцы Q продолжительностью более 0,03 с с амплитудой более 0,2 мВ; эти изменения должны отмечаться в 2 из 3 «нижних» (II, III, aVF) или 2 из 6 прекардиальных (V1 – V6) отведениях или в I и aVL; – недавно или предположительно недавно появившийся подъем ST на 0,1 мВ и более; подъем ST измеряют на расстоянии 0,02 с от окончания зубца S; – блокада ножки пучка Гиса. Если систолическое АД превышает 180 мм рт. ст., сначала надо добиться его снижения, предпочтительно с помощью внутривенного введения атенолола или лабеталола.
Противопоказания
• Абсолютные: – кровотечение на момент обследования; – инсульт; – желудочно-кишечное кровотечение в течение последнего месяца; – недавно перенесенное (в предшествующие 3 нед) большое хирургическое вмешательство, большая травма или травма головы; – расслаивающая аневризма аорты; – известные геморрагические диатезы. • Относительные (возможный риск должен тщательно сопоставляться с пользой): – преходящие ишемии мозга в предшествующие 6 мес; – лечение оральными антикоагулянтами – антивитаминами К; – беременность; – недавняя травматическая сердечно-легочная реанимация (более 10 мин); – рефрактераня артериальная гипертония (АД > 180/100 мм рт. ст.); – недавняя пункция несдавливаемого сосуда; – недавнее лечение сетчатки лазером.
Методика
Желательно, чтобы промежуток от поступления больного в стационар до начала тромболитической терапии не превышал 30 мин. Внутривенное введение СК осуществляют следующим образом: 1 500 000 ЕД вводят в 100 мл 5% глюкозы или 0,9% натрия хлорида за 30 – 60 мин. Введение гепарина не обязательно, возможно его подкожное введение по 12 500 ЕД 2 раза. Специфическими противопоказаниями является предшествующее (до 5 дней) применение СК или анистреплазы. ТАП (альтеплазу) вводят по следующей схеме: 15 мг препарата внутривенно болюсом, затем по 0,75 мг/кг в течение 1 ч внутривенно за 30 мин, далее 0,5 мг/кг в течение 1 ч; общая доза 100 мг. Гепарин вводят внутривенно в течение 48 ч. АПСАК (анистреплазу) вводят в дозе 30 ЕД внутривенно в течение 5 мин. Специфическими противопоказаниями являются предшествующее применение СК или анистреплазы за 5 дней и известная аллергия на СК/анистреплазу. Урокиназу вводят в дозе 2 000 000 ЕД внутривенно болюсом или 1 500 000 ЕД боолюсом + 1 500 000 ЕД в течение 1 ч. Гепарин вводят в течение 48 ч. При появлении признаков реокклюзии или повторного ИМ с подъемом ST или блокадой ножки пучка Гиса следует вновь провести тромболизис или ангиопластику. В период от 5 дней до 2 лет нельзя повторно применять СК или АПСАК. Антитела к СК сохраняются по крайней мере в течение 2 лет. Применение альтеплазы и урокиназы не приводит к образованию антител. Оценка эффективности тромболитической терапии
Существует несколько маркеров успешности тромболитической терапии. Уменьшение подъема ST в 12 стандартных отведениях ЭКГ через 1 – 4 ч после начала тромболизиса – самый простой и полезный клинический признак для оценки эффективности тромболитической терапии. Предсказательное значение этого показателя может быть усилено путем комбинирования его с уровнем миоглобина сыворотки и тропонина Т, которые могут быть быстро определены. Дополнительными признаками эффективности тромболитической терапии могут быть прекращение ангинозной боли и значительное (на 40 – 100%) повышение актвности ферментов, прежде всего креатинфосфокиназы. Появление реперфузионных аритмий – ускоренный идиовентрикулярный ритм, желудочковые экстрасистолы, желудочковая тахикардия, фибрилляция желудочков, атриовентрикулярные (АВ) блокады и др. – также может приниматься во внимание, но может рассматриваться и в качестве осложнения. Следует отметить, что сократительная способность миокарда при реперфузии восстанавливается не сразу (феномен «оглушенного миокарда»).
Осложнения
Тромболитическая терапия может сопровождаться нежелательными реакциями. Вероятность возникновения осложнений зависит от учета абсолютных и относительных противопоказаний, выбора препарата и метода проведения тромболитической терапии. Реперфузионные аритмии – чамое частое осложнение тромболитической терапии и одновременно косвенное свидетельство ее эффективности – отмечаются у 20 – 60% больных. Чаще всего встречаются ускоренный идиовентрикулярный ритм, желудочковые экстрасистолы, пароксизмы неустойчивой желудочковой тахикардии, преходящая АВ-блокада, фибрилляция желудочков. Лечение аритмий осуществляется по тем же принципам, как и аналогичных нарушений ритма и проводимости, не связанных с реперфузией. Реокклюзия коронарной артерии наблюдается в 15 – 20% случаев и часто протекает бессимптомно. У части больных реокклюзия проявляется возобновлением ангинозной боли и ухудшением гемодинамики. Для предупреждения и лечения этого осложнения вводят нитроглицерин и гепарин внутривенно капельно. Артериальную гипотензию обычно коррегируют посредством скорости введения тромболитического препарата. Если этого недостаточно, то назначают инфузионную терапию и кортикостероидные гормоны (преднизолон по 30 – 60 мг, а при отсутствии эффекта – дофамин по 2 – 5 мкг/кг в 1 мин). Аллергические реакции требуют немедленного прекращения введения тромболитического препарата и, в зависимости от клинических проявлений, назначения антигистаминных препаратов, кортикостероидных гормонов, бронхолитических средств, а при развитии анафилактического шока – адреналина. Если возникает необходимость в электрокардиостимуляции или гемодинамическом мониторинге, целесообразно сделать это до начала тромболитической терапии. Пункция подключичной или внутренней яремной вены противопоказана. Грозным осложнением тромболитической терапии является внутричерепное кровоизлияние. Широкому внедрению новых способов введения тромболитических препаратов препятствует соображение о том, что улучшение реперфузии может привести к более частому возникновению внутричерепных кровоизлиянияй. Более часто они наблюдаются при применении фибринспецифических средств по сравнению с СК. Это продемонстрировано в исследованиях GUSTO 2 А, TIMI 9 и HIT 3. Геморрагический инсульт обычно развивается у больных старческого возраста с неконтролируемой артериальной гипертензией и отягощенным неврологическим анамнезом, поэтому данной категории больных тромболитическая терапия противопоказана. При развитии геморрагического инсульта его лечение проводится так же, как и без проведения тромболитической терапии. При дозе СК 1 500 000 ЕД за 1 ч риск внутричерепных кровоизлияний составляет 1 – 10 на 1000 леченых больных. Желудочно-кишечные кровотечения различной степени тяжести можно ожидать у 5% больных, мочеполовые кровотечения – с той же частотой. Частота внутричерепного кровоизлияния после rТАП зависит от дозы. При дозе 150 мг она составляет 15 – 20 на 1000, а при дозе 100 мг – 5 – 10 на 1000. Внутричерепные кровоизлияния при применении АПСАК четко не зарегистрированы. Даже при эффективном тромболизисе сохраняется повышенный риск возникновения ишемии, поскольку остается атеросклеротическая бляшка. В связи с этим у больных сохраняется риск рецидива и повторного ИМ в дальнейшем. У части больных, несмотря на терапию аспирином и гепарином, после успешного тромболизиса вновь возникают боль в грудной клетке, повторный тромбоз коронарной артерии с развитием ИМ. Коронарный тромболизис слабо влияет на те гемодинамические факторы в пораженной атеросклерозом коронарной артерии, которые способствуют активации фибриногена и образованию тромба, он лишь на какое-то время восстанавливает коронарный кровоток. Больным после успешного тромболизиса с целью предотвращения повторного тромбоза коронарной артерии показана экстренная операция коронарного шунтирования или балонная ангиопластика с постановкой стента. Колебания риска ОИМ в течение суток, вероятно, обусловлены суточными колебаниями активности коагуляции и эффектом подъема с постели после сна. Влияет ли различный баланс между коагуляцией и фибринолизом на физиологическом уровне на эффект тромболитических препаратов, остается неясным. Делаются попытки разработать более безопасные и эффективные тромболитические средства. Информированность населения о симптомах ИМ и развитие более быстрой и эффективной системы неотложного реагирования также могут улучшить исход тромболитической терапии благодаря укорочению времени между появлением симптомов и введением тромболитического препарата. Современный врач должен знать, что наиболее раннее введение тромболитического препарата больному ИМ является наилучшим способом спасти человека и обеспечить сохранность гемодинамики.
Рекомендуемая литература:
1. Алперт Дж., Френсис Г. Лечение инфаркта миокарда. Практическое руководство. Пер. с англ. – М.: Практика, 1994. – С. 196–201. 2. Бокарев И.Н., Павлов А.В., Янкин В.В., Кажарская Э.Е., Довголис С.А., Инокентьев И.К., Мартынова И.Г., Ландо Л.Г., Федорова С.Ю., Леперский А.Л., Блохина И.В., Улыбышева М.А. Быстрый тромболизис препаратами стрептокиназы при остром инфаркте миокарда. /Тромбозы, геморрагии, ДВС-синдром. Вопросы лечения. Международная конференция. Москва. 2–4 апреля 1997 г. 3. Кардиология в таблицах и схемах. Под ред. М. Фрида и С. Грайнс. Пер. с англ.- М.: Практика, 1996. – С. 149–50. 4. Международное руководство по инфаркту миокарда. Под ред.
Абсолютные противопоказания
Данная процедура считается достаточно сложной и далеко не всегда легко переносится пациентами. Медиками установлен целый список условий, которые могут препятствовать ее проведению. На сегодняшний день выделяют следующие абсолютные противопоказания к тромболизису при инфаркте миокарда:
- Наличие расслаивающейся аневризмы аорты.
- Геморрагический инсульт в анамнезе менее 6 месяцев назад.
- Нарушения системы свертывания крови.
- Артериальная гипертензия, резистентная к антигипертензивной терапии (при помощи лекарственных препаратов не удается уменьшить уровень систолического артериального давления ниже 220 мм. рт. ст., а диастолического — ниже 110 мм. рт. ст.).
- Оперативные вмешательства менее 3 недель назад.
- Желудочно-кишечные кровотечения менее 1 месяца назад.
- Черепно-мозговая травма менее 3 недель назад.
При всех этих состояниях тромболизисная терапия не проводится. Это обусловлено тем, что риск развития серьезных, угрожающих жизни осложнений, больше, чем положительный эффект от выполнения процедуры.
Результаты тромболизиса
Не только тромболизис помогает врачам спасти жизнь пострадавшему человеку и восстановить кровообращение в сосудах. Некоторые другие методы тоже дают подобный эффект. Исследования показали, что своевременное проведение тромболизиса:
- способствует скорейшему выздоровлению,
- снижает срок пребывания в больнице,
- увеличивает шансы на сохранение работоспособности после инфаркта.
Хотя при инфаркте больная сердечно-сосудистая система дает сбой, восстановить ее работу возможно. Если этим занимаются квалифицированные врачи, результат гарантирован.
Относительные противопоказания
Имеются ситуации, при которых проведение тромболизисной терапии нежелательно, но возможно в тех случаях, когда предполагаемая польза от процедуры превышает возможный вред от нее.
На сегодняшний день выделяют следующие относительные противопоказания к тромболизису при инфаркте миокарда:
- Транзиторные ишемические атаки менее 6 месяцев назад.
- Беременность.
- Послеродовый период (менее 28 суток после разрешения беременности).
- Постоянное использование прямых антикоагулянтов.
- Длительная сердечно-легочная реанимация, сопровождающаяся травматизацией пациента.
- Наличие гастральных язв в стадии обострения.
- Печеночная недостаточность.
- Инфекционный эндокардит.
- Пунктирование крупных сосудов, недоступных для компрессии.
- Любые кровоизлияния в сетчатку.
Несмотря на большое количество относительных противопоказаний, чаще всего медики проводят тромболизис при инфаркте миокарда, не взирая на их наличие, так как без этой процедуры велика вероятность развития самых тяжелых последствий для пациентов.
Виды тромболизиса
Существует два вида тромболизиса: ранний и поздний. Поздним считается тромболизис, проведенный в течение 3-6 часов после закупорки сосудов тромбом. Он восстанавливает кровоснабжение сердца, поддерживает функционирование левого желудочка и предупреждает развитие летального исхода. Наиболее эффективным является ранний тромболизис, который проводят в первые часы сердечного приступа.
К показаниям для проведения тромболитической терапии относятся:
- Первые 12 часов от начала болевого синдрома.
- Наличие приступа острой боли в области груди, который длится больше 30 минут.
- Регистрация на ЭКГ подъема сегмента ST.
- Выявление на электрокардиограмме признаков полной блокады левой ножки пучка Гиса.
Возможные побочные эффекты
Данная процедура зачастую протекает достаточно тяжело для больного. Нежелательные реакции развиваются примерно у 1% пациентов, перенесших тромболизис при инфаркте миокарда. Среди наиболее распространенных побочных эффектов:
Сложность процедуры, а также возможное развитие побочных эффектов является одними из причин, по которым тромболизис при инфаркте миокарда чаще всего проводится в отделении реанимации (если пациент находится в стационарных условиях).
Осложнения после тромболизиса
К осложнениям тромболитической терапии относятся:
- Кровотечения различной интенсивности и локализации.
- Нарушение сократительной функции миокарда и развитие сердечной недостаточности.
- Аллергическая реакция и развитие анафилактического шока.
- Мозговой геморрагический инсульт.
- Реперфузионные (связанные с возвратным кровотоком из предсердий в аорту) нарушения ритма сердца.
- Повторная закупорка сосудов сердца.
- Стойкое снижение артериального давления.
- Повышение температуры тела, появление озноба и сыпи.
Мозговой геморрагический инсульт чаще развивается у лиц с факторами риска, к которым относят:
- Использование при тромболитической терапии альтеплазы.
- Высокие показатели артериального давления.
- Возраст пациента, превышающий 65 лет.
- Вес пациента меньше 70 килограмм.
Проведение тромболизиса способствует восстановлению кровотока и обеспечивает питание сердечной мышцы. В большинстве случаев тромболизис предотвращает развитие летального исхода, и сохраняет жизнь пациентов.
Критерии успешности проведения процедуры
В случае если тромболиз проведен успешно, то наблюдаются следующие явления:
- У пациента быстро уменьшаются, а затем исчезают болезненные ощущения.
- Возвращение показателей электрокардиографии в норму.
- Развитие мерцательной аритмии (фибрилляции предсердий) в процессе проведения тромболитической терапии.
- Возвращение к нормальным уровням показателей кардиоспецифических биохимических маркеров некроза.
Также во время проведения тромболизиса оценивается общее состояние пациента и другие показатели его здоровья (частота сердечных сокращений, дыхания, уровень артериального давления и прочие).
Ход процедуры
Тромболитическая терапия при инфаркте проводится либо врачами скорой помощи, либо в реанимационном отделении. После поступления пациента в больницу, все подготовительные мероприятия должны осуществляться в течение часа. За это время больного необходимо обследовать на сопутствующие заболевания и наличие противопоказаний к процедуре.
Инфаркт миокарда – это опасная патология, при которой каждая минута может спасти жизнь человеку. Во время выполнения тромболизиса врач должен придерживаться таких рекомендаций:
- до введения тромболитических препаратов устанавливают мочевые катетеры;
- на протяжении первых суток после лечения нельзя в крупные артерии вставлять катетеры;
- в течение суток запрещены любые внутримышечные инъекции;
- при подборе дозировки должны учитывать вес больного.
Также читают: Как предотвратить инфаркт? Возраст не является противопоказанием для применения тромболитиков. Чем меньше времени прошло от начала приступа, тем больше эффекта будет от проведенной терапии. Это связано с тем, что свежие тромбы обладают более мягкой консистенцией и легче рассасываются.
Со временем они уплотняются, что значительно затрудняет процесс лечения.
Для проведения тромболитической терапии используют:
- Пуроплазу – проурокиназу рекомбинантную.
- Альтеплазу. Это фибрин-специфический антиген. Его вводят после 4 часов.
- Тенектеплазу. Средство используют для ведения в догоспитальном периоде.
Также в процессе лечения часто применяют Актилизе в следующей дозировке:
- На протяжении первых трех часов делается струнное введение 15 мг Актилизе. После этого инфузионным способом вводят 50 мг. Через час на протяжении 60 минут – еще 35 мг вещества. Нельзя вводить больше 100мг препарата.
- Если лечение проходит в срок от 6 до 12 часов, то сначала струнным способом вводят 10 мг, после этого – 59 мг инфузионно. Затем раз в полчаса вводят по 10 мг, пока общая дозировка не достигнет 100 мг.
Врач, который осуществляет процедуру, должен строго следовать инструкции.
Препараты для тромболизиса
На протяжении предыдущих десятилетий основным препаратом для проведения тромболизисной терапии являлось лекарственное средство «Стрептокиназа». Оно относится к группе прямых тканевых активаторов плазминогена. Этот препарат относительно дешевый, но при этом недостаточно эффективен, также он нередко вызывает развитие серьезных побочных эффектов. В настоящее время все большее распространение получили непрямые тканевые активаторы плазминогена, основными из которых являются:
Тромболизис при инфаркте миокарда, проведенный непрямыми тканевыми активаторами плазминогена чаще проходит без негативных реакций и имеет неплохую эффективность. Основным их недостатком является относительно высокая стоимость в сравнении с препаратом «Стрептокиназа».
Что такое тромболизис
Тромболизис – процесс, направленный на растворение образовавшегося в кровеносном сосуде тромба. В организме здорового человека он происходит постоянно, предотвращая образование маленьких тромбов. Процесс растворения происходит с помощью специальных ферментов.
Если сформировались крупные тромбы, организм неспособен самостоятельно их растворить. В лучшем случае в сгустке может появиться небольшое отверстие, однако этого недостаточно для нормального кровообращения.
По мере образования новых тромбов питание жизненно важных органов ухудшается, а риск инфаркта (отмирания клеток сердечной мышцы) возрастает. Если ничего не предпринимать, в тканях начинается некроз, а сокращение мышцы ухудшается, что способно привести к внезапной остановке сердца.
Важно! Тромболизис проводится медиками в условиях стационара или скорой помощи. Суть метода заключается во введении препаратов, способных растворить тромб в кратчайшие сроки.
Своевременно проведенный тромболизис позволяет остановить инфаркт миокарда, защитив большую часть сердечной мышцы. Процедура полноценно восстанавливает кровоснабжение и питание клеток сердца.
Механизм действия препаратов
Данные лекарственные средства обеспечивают связывание фермента с плазминогеном, расположенном на фибрине. Под воздействием препаратов плазминоген превращается в плазмин, проникая при этом внутрь фибрина. В дальнейшем плазмин разрушает фибрин, тем самым обеспечивая распад тромба.
При выполнении тромболизиса могут образовываться микротромбы. Также введение тканевых активаторов плазминогена способствует увеличению активности тромбоцитов. Все это требует сопутствующей антитромбоцитарной терапии.
Препараты для введения
Эффективность процедуры зависит не только от квалификации специалиста, который её проводит, но также и от качества лекарственных средств, вводимых в вену. Несмотря на обилие разнообразных тромболитиков, не все средства одинаково эффективны. Существует несколько основных групп медпрепаратов, чаще всего используемых при проведении тромболитической терапии.
- Быстрого положительного результата можно достичь при использовании во время процедуры препарата «Проурокиназа». Однако этот медикамент не подойдёт тем пациентам, у которых плохая свёртываемость крови или существует риск церебрального кровоизлияния.
- Наиболее безопасными и наряду с этим не менее действенными и эффективными являются препараты «Алтеплаза» или «Актилизе» — способны в сжатые сроки облегчить состояние пациента. Могут применяться спустя 5−6 часов после возникновения первых симптомов ишемического инсульта. Однако для лечения этими медикаментами требуется введение гепарина.
- Препараты нового поколения «Анистреплаза», «Тенектеплаза» и «Метализе» не требуют применения гепарина после введения, что значительно упрощает процесс лечения больного. Более того, в результате внутривенного введения лекарства вероятность развития аллергических реакций сводится к минимуму.
- Очень редко используются препарат старого поколения — «Стрептокиназа». Он является самым простым и дешёвым среди имеющихся аналогов, и одновременно с этим лекарство обладает мощным тромболитическим эффектом. Способен вызывать серьёзные аллергические реакции и провоцировать развитие гематом, поэтому «Стрептокиназа» используют в редких случаях и не чаще одного раза.
- Лекарство «Урокиназа» является относительно новым средством, обладающим мощным эффектом. Показатели выживаемости значительно выше, чем у аналогов (не менее пятнадцати процентов). Однако для лечения ишемического инсульта при помощи «Урокиназа» требуется использование гепарина.
Перечисленные препараты имеют в составе преимущественно натуральные компоненты. Однако независимо от состава и терапевтического эффекта самостоятельно их использовать для устранения признаков инсульта мозга категорически запрещается. У тромболитических медикаментов имеется немало противопоказаний и побочных эффектов, которые врач обязательно учитывает перед тем, как вводить внутривенно препарат.
Порядок действий медицинских работников
На сегодняшний день нередко практикуется проведение тромболизиса при инфаркте миокарда на догоспитальном этапе. Для этого лучше всего подходят такой лекарственный препарат, как «Тенектеплаза». Он отличается от прочих прямых тканевых активаторов плазминогена низкой вероятностью развития осложнений, а также простотой в обращении. «Тенектоплазу» вводят внутривенно струйно.
«Альтеплазу» также иногда используют для тромболизиса при инфаркте миокарда на догоспитальном уровне. Перед ее применением пациенту вводят 5000 ЕД гепарина. Затем внутривенно болюсно вводится 15 мл «Альтеплазы». После этого капельно пациенту вводится по 0,75 мл препарата на каждый килограмм веса пациента в течение 30 минут. При этом больному постоянно вводится гепарин.
«Стрептокиназу» рекомендуется вводить только в условиях стационара. При использовании данного препарата тромболизис при инфаркте миокарда выполняют в отделении реанимации. Пациенту внутривенно капельно вводят 1500000 ЕД препарата, разведенного на 100 мл физиологического раствора в течение 0,5-1 часа. В случае с данным медикаментом, перед его введением также используется гепарин в объеме 5000 ЕД. В дальнейшем гепарин используется не менее, чем через 4 часа после окончания инфузии «Стрептокиназы».
На каждом бланке протокола тромболизиса при инфаркте миокарда указано, что выполнять данную процедуру стоит не позднее 12 часов после возникновения первых симптомов заболевания. После проведения тромболизисной терапии необходимо в течение 12 часов доставить в специализированный стационар с целью проведения стентирования или балонной ангиопластики. Соблюдение данного порядка значительно повышает шансы пациента на положительный исход заболевания.
Виды
В зависимости от времени проведения тромболизиса, процедура может быть:
- селективной;
- неселективной.
В первом случае введение препаратов осуществляют на протяжении первых шести часов от начала острого нарушения кровообращения. Главной особенностью неселективной методики является выполнение реанимационных мероприятий на протяжении первых трех часов.
С учетом метода введения лекарственных средств тромболизис бывает:
- локальным. Если в условиях стационара было проведено обследование с применением оборудования для внутрисосудистого введения, разжижающие средства подводят как можно ближе к пораженному месту;
- системным. Его применяют, когда нет информации о том, в каком месте расположен тромб, вызвавший приступ инфаркта миокарда. Препараты при этом вводят обычным способом в вену.
Что должен сделать пациент?
Инфаркт миокарда обычно развивается в тех случаях, когда у пациента уже имеется другая сердечно-сосудистая патология. Чаще всего данное заболевание характеризуется сильной болью в загрудинной области, сопровождающейся иррадиацией в левое плечо, кисть, лопатку, живот или шею, а также выраженной слабостью. При возникновении данных симптомов пациенту рекомендуется вызвать бригаду скорой медицинской помощи, затем измерить артериальное давление и, если его уровень не менее 120/80 мм. рт. ст. принять таблетку нитроглицерина. Если через 5 минут боли не исчезли, а бригада СМП еще не приехала, необходимо повторить прием данного препарата. Кроме этого, рекомендуется принять 500 мг ацетилсалициловой кислоты (аспирина).
Противопоказания к выполнению лизиса тромбов
- внутреннее кровотечение, произошедшее в последние две недели;
- высокое артериальное давление, превышающее 200/120 мм рт. столба;
- черепно-мозговая или другая травма, хирургическое вмешательство в последние две недели;
- пептическая язва желудка в активном состоянии;
- подозрение на перикардит (кровоизлияние в околосердечную область), угроза аневризмы аорты;
- аллергия к препарату, с помощью которого планируется проводить тромболизис.
- любая операция или черепно-мозговая травма, произошедшие более двух недель назад;
- геморрагический диатез (склонность к кровоточивости) как реакция на тромболизис;
- сахарный диабет;
- печеночная или почечная недостаточность;
- злокачественные опухоли;
- наличие активной инфекции;
- применение антикоагулянтов в последние шесть месяцев.
Что сделает медицинский работник?
В случае с фельдшером или врачом бригады скорой медицинской помощи, то данные сотрудники должны выполнить следующие действия перед началом проведения тромболизисной терапии:
- Уточнить у пациента время возникновения и характер болевого синдрома.
- Выполнить электрокардиогарфию для уточнения диагноза «инфаркт миокарда» и измерить уровень артериального давления.
- В случае постановки данного диагноза пациенту дают таблетку нитроглицерина, «Аспирина» (если он не принял ее ранее).
- В дальнейшем его в положении лежа переносят в машину скорой медицинской помощи.
- Уже во время транспортировки в стационар оценивается эффект от приема нитроглицерина (5 минут).
- Также пациенту вводится 5000 ЕД гепарина, дается не менее 40 мг статинов («Аторвастатин», «Розувастатин», «Ловастатин») и препараты из группы бета-адреноблокаторов («Метопролол», «Бисопролол», «Карведилол») и ингибиторов АПФ («Эналаприл», «Лизиноприл», «Периндоприл», «Рамиприл») в дозировке, которая не снизит уровень артериального давления менее 110/70 мм. рт. ст. и частоту сердечных сокращений менее 50 уд/мин.
- В дальнейшем медицинский работник уточняет наличие противопоказаний к проведению тромболизиса. Если они отсутствуют, то начинается проведение данной процедуры.
В случаях, когда стационарное учреждение здравоохранения располагается неподалеку от места вызова бригады скорой медицинской помощи, тромболизис чаще выполняется в условиях реанимационного отделения с целью снижения вероятности развития серьезных осложнений и наиболее быстрой стабилизации состояния пациента при их возникновении.
В больнице тромболизисная терапия проводится под постоянным контролем врача кардиолога/терапевта и врача реаниматолога.
После окончания процедуры врачи стабилизируют состояние пациента и переводят в специализированное учреждение здравоохранения с целью выполнения ангиопластики или стентирования. После выписки из стационара пациента направляют на амбулаторный этап лечения, где ему рекомендуется прием следующих медикаментов:
Эти лекарственные средства значительно снижают вероятность развития повторных инфарктов миокарда. В дальнейшем, при удовлетворительном состоянии пациента, а также наличии достаточного восстановительного потенциала (пациент не слишком возрастной, способен передвигаться, доступен продуктивному контакту) его направляют на реабилитацию, с целью восстановления нормальной жизнедеятельности. В случаях, когда речь идет о молодых людях, то их нередко направляют на восстановительный курс сразу после проведения стационарного этапа лечения.
Способы растворения тромба
Для восстановления кровообращения в закупоренном сосуде используется два метода – внутривенное введение традиционным способом или локальное – непосредственно в сосуд, в котором находится тромб. Есть исследования, доказывающие, что оба метода достаточно эффективны в первые 6 часов от момента приступа, но максимум положительных результатов тромболизиса отмечается до окончания третьего часа.
Легче всего растворить тромб в вене, поэтому при тромбоэмболии легочной артерии (несет венозную кровь) нужны меньшие дозы ферментов, чем при атеросклеротическом поражении (инфаркте миокарда или головного мозга). При этом нужно учитывать, что растворение кровяного сгустка в глубокой вене нижних конечностей опасно его продвижением к сосудам легких.
При системном тромболизисе (внутривенное поступление медикамента в капельнице) есть недостаток – угроза кровотечения. Это вызвано высокой дозой препарата, что также повышает риск нежелательных последствий.
Но у него есть и достоинство – тромбоз практически никогда не бывает изолированным, поэтому растворению подвергаются и сгустки других локализаций.
При локальном (селективном) введении ферментов требуется рентгенологический контроль за продвижением катетера к месту закупорки. Это позволяет точно доставить тромболитик в зону нарушения кровотока и применить меньшую дозу. Его проведение возможно только в специализированных учреждениях врачами, владеющими внутрисосудистыми методиками. Он может быть эффективен на более поздних сроках (6 — 12 часов), чем системный.
Прогноз
При соблюдении дозировок препаратов тромболизис при инфаркте миокарда в подавляющем большинстве случаев является успешным. Даже при использовании стрептокиназы количество серьезных осложнений не превышает 2%. Данные показатели эффективности актуальны в тех случаях, когда соблюдаются все рекомендации тромболизиса при инфаркте миокарда.
Несмотря на проведение данной процедуры, дальнейшее качество жизни пациента во многом будет зависеть от полноты и своевременности выполнения других лечебных и реабилитационных мероприятий. После тромболизиса пациентам рекомендуется пройти курс лечения в отделениях кардиологического профиля с возможным проведением ангиопластики или стентирования. Реабилитация включает в себя курсы лечебной физкультуры, составление графика необходимых физических нагрузок, а также регулярный прием медикаментозных препаратов.
Как оценивается эффективность терапии
Критерии оценки эффективности процедуры тромболизиса:
- Клиническая картина: уменьшается интенсивность болевого синдрома, развиваются реперфузионные аритмии.
- Данные электрокардиограммы: стремительное падение сегмента ST, появление отрицательного зубца T.
- Результаты лабораторных исследований: снижается активность КФК (креатинфосфокиназа) и ее форм, уменьшается уровень фибриногена, увеличивается тромбиновое время.
- Показатели ангиографии: исследование определяет проходимость сосудов сердца.
Эффективность тромболитической терапии зависит от множества различных факторов, таких как:
- Время старта лечения.
- Режим введения.
- Скорость восстановления проходимости артерий.
- Квалификация специалистов, проводящих лечение.
- Профилактические меры, предупреждающие развитие осложнений.
Особенности организации тромболизиса в стационаре
Наибольшую эффективность препараты, разрушающие тромбы, демонстрируют в течение первых 3 часов после приступа. Допустимо вводить их в течение 12 часов с момента проявления первых симптомов инфаркта. Но если сделать это позже, то процедура будет неэффективной. Поэтому первые инъекции препаратов пациенты получают в скорой. Но данные требования актуальны для больных с инфарктом миокарда.
Пациенты, поступившие с острым нарушением кровообращения мозга, могут подвергнуться данной терапии после установки ишемии. Для этого их необходимо обследовать с помощью ультразвука, рентгена или томографа. Больного нужно очень быстро доставить в госпиталь, т.к. каждая секунда важна. Решение об использовании искусственного тромболизиса для улучшения состояния больного принимает врач после того, как ознакомиться с результатами обследования. При инсульте данная методика позволяет:
- уменьшить время пребывания пациентов в стационаре на 3-4 дня;
- помогает избежать множество осложнений;
- позволяет сохранить полную трудоспособность 60% больным;
- позволяет ускорить реабилитацию пациентов.
Наибольшую эффективность процедура демонстрирует в состоянии перед приступом. Тогда можно избежать практически всех осложнений, связанных с инфарктами.
Показания к проведению тромболизиса
Показания к проведению тромболизиса
(пожилой возраст — не противопоказание): •
на ЭКГ
определяются подъем интервала ST более 1 мм в двух и более смежных отведениях (при подозрении на передний ИМ) или в 2 из 3 отведений от конечностей II, III, avF (при подозрении на нижний ИМ), или наличие БЛНПГ (вероятно, когда субтотальная окклюзия коронарной артерии прогрессирует в тотальную), или идиовентрикулярный ритм,
• первые 6 ч инфаркта миокарда
. Но при сохранении боли, подъеме сегмента ST и отсутствии зубца Q (когда миокард еще жив) «годятся» и первые 12 ч, если ИМ не завершился и имеется «мозаичность» клинической картины Решение о проведении тромболизиса в сроки после 12 ч принимается на основании клинической картины, анамнеза и ЭКГ
Проведение тромболизиса
при ОКС без стойкого подъема сегмента ST (или с инверсией зубца Т, или отсутствием изменений на ЭКГ) не показано