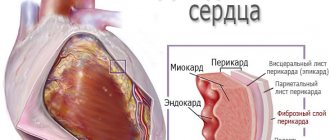
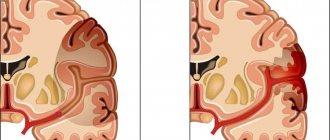
Портальная гипертензия наблюдается в ситуациях, когда при циркуляции крови в районе печени возникает какой-то барьер. Показатель давления в портальной системе составляет примерно 7 мм ртутного столба. Если показатель превышает 20 мм, кровь застаивается в венах. Поскольку стенки в этих сосудах не укрепляются мышцами, они расширяются. Может произойти разрыв. Когда развивается цирроз, почти в 90% примеров расширение происходит в области пищевода, других отделов ЖКТ. Иногда возникают кровотечения, есть высокая вероятность летального исхода.
Портальная гипертензия?
Проблемы с движением крови в венах могут возникать ниже печени, в самом органе или в области полой вены.
Расстройство классифицируются по признакам:
- Если в печеночных сосудах формируются тромбы, блокада возникает над органом. Воспаление перикарда провоцирует высокое давление в сосудах. Кровь из печени выходит медленно.
- Проблемы возникают внутри органа по причине цирроза, воспалительных процессов, новообразований, в спайках после повреждений и хирургического вмешательства.
- Токсины разрушают клетки печени, увеличивается сопротивление движению крови по сосудам. Гепатоциты отличаются высокой жизнеспособностью, могут регенерироваться.
- Даже при уничтожении фрагмента печени оставшаяся часть продолжает нормально работать, со временем функции органа восстанавливаются полностью.
- Проблемы могут возникнуть из-за регулярного воздействия токсинов, воспаления. Сформированные соединительные ткани не способны выполнять очистку организма.
Воспалительные процессы в брюшине могут вызывать блокировку кровотока до поступления в печень. Происходит сжатие нескольких ответвлений воротной вены. Сосуды суммируются аномально, возникают осложнения после неудачного хирургического вмешательства. У людей часто возникает изолированный тромбоз, причина этому может оказаться внутрибрюшная инфекция.
Классификация
По формам портальную гипертензию делят на:
- Предпеченочную портальную гипертензию – нарушение портального кровотока в воротной вене до ее вхождения в ворота печени;
- Внутрипеченочную портальную гипертензию – нарушение кровотока в портальной вене возникающее внутри печени;
- Постпеченочную портальную гипертензию – нарушение кровотока по печеночным венам или по нижней полой вене;
- Смешанную портальную гипертензию – наличие комбинации вышеперечисленных форм портальной гипертензии.
Внутрипеченочную форму портальной гипертензии подразделяют на несколько видов:
- пресинусоидальная внутрипеченочная портальная гипертензия – нарушение кровотока в воротной вене до вхождения ее в печеночную дольку;
- синусоидальная внутрипеченочная портальная гипертензия – нарушение кровотока в воротной вене на уровне печеночной дольки;
- постсинусоидальная внутрипеченочная портальная гипертензия – нарушение кровотока в печеночной вене, которая выходит из печеночной дольки.
По стадиям портальную гипертензию делят на:
- Доклиническая или начальная стадия, которая характеризуется отсутствием жалоб, подтверждается только при обследовании;
- Умеренная или компенсированная стадия – характеризуется появлением симптомов нарушения кровообращения печени, увеличением печени и селезенки;
- Выраженная или декомпенсированная стадия – резко выраженные все симптомы портальной гипертензии, незначительные кровотечения;
- Терминальная стадия – массивные, продолжительные кровотечения из вен желудочно-кишечного тракта.
Симптомы
Признаки портальной гипертензии, обусловленные патологией, вызывающие повышение давления в сосудах. По мере развития патологического процесса возникают клинические симптомы, свойственные для разных форм синдрома:
- Увеличивается размер селезенки, понижается концентрация тромбоцитов, эритроцитов, возникают проблемы со свертываемостью.
- Варикозное расширение в области желудка, прямой кишки.
- Усугубляется анемия, возникает венозное кровотечение.
- Асцит.
Клинические стадии:
- Доклиническая, при которой больной ощущает тяжесть справа в боку под ребрами, возникает недомогание, живот вздувается.
- Появляются выраженные признаки, боль, недомогание, вспучивается животик.
- Все признаки портальной гипертензии присутствуют, асцит, не наблюдается кровотечение.
- Возникают большие кровотечения.
При печеночной форме расстройство зачастую возникает в детском возрасте, развивается мягко, имеет позитивный прогноз. Портальная вена пережимается, учащаются осложнения, возникают кровотечения в сосудах в нижних отделах пищевода, сдавливается воротная вена, улучшается свертываемость.
Портальная гипертензия отличается признаками цирроза. Это основные симптомы заболевания. Динамика развития обуславливается интенсивностью возникновения гипертензии. Болезни сопровождаются кровотечениями, присутствует асцит. Кожные покровы желтеют, это указывает на то, что печень не выполняет нормально свои функции, переводящиеся в печеночную недостаточность. Изначально пожелтение возникает на ладонях и под языком. Патология Киари в основном является причиной надпеченочной формы ПГ. Летальный исход вызывает недостаточность органов и кровотечение.
Опасные последствия
Повышение давления в печеночной вене чревато жизнеугрожающими осложнениями. Нарушение функций селезенки ведет к массивному разрушению кровяных клеток, вследствие чего возникают:
- анемия;
- недостаточная свертываемость крови;
- иммунодефицитные состояния.
Запоздалое лечение печеночной гипертонии опасно расширением вен пищевода, эрозией его стенок, кровотечениями. На 3 и 4 стадиях возникают:
- брюшная водянка;
- недостаточность печени;
- бактериальный перитонит;
- вторичная дисфункция почек.
Синдром портальной гипертензии у детей в 7 из 10 случаев вызывается нарушением внутриутробного развития, тромбозом околопупочных вен. Несвоевременное выявление и терапия приводит к смертельному исходу.
Особенности развития болезни
Портальная гипертензия вызывает расстройство по всему организму. На первых этапах нарушение в периферических сосудах вызывает трудности с работой печени. Появляются проблемы с общим кровотоком, наблюдается воспаление в портальной вене. Начинаются разрушительные процессы в печени, регуляторная функция ухудшается. На поверхности органа возникает соединительная ткань.
Различают несколько видов развития болезни:
Циркуляция крови в печени у усугубляется по разным причинам:
- Повышает сопротивление портальным сосудам.
- Стачивается слишком много крови.
- Появляется асцит, по которому часто удается выявить заболевания.
- Создаются коллатерали.
- Проблемы с нервной деятельностью из-за расстройства печени.
- Размеры селезенки увеличиваются, создаются застойные явления.
Симптоматика и развитие проблемы
Первоначальные признаки портальной гипертензии тесно связаны с причиной, повлекшей за собой патологические изменения. С прогрессированием заболевания начинают проявляться сопутствующие симптоматические проявления:
- У больных значительно увеличивается селезенка в размере.
- Кровь плохо свертывается, что особо опасно при регулярных кровотечениях.
- Расширяются варикозные вены в области желудка и прямой кишки.
- Последствием частых кровотечений, выступает анемия.
- В животе начинает скапливаться жидкость, от этого он значительно увеличивается в размерах.
Диагностика
Для выявления портальной гипертензии нужно выполнить несколько обследований. Специалистам предстоит собрать детальный анамнез, определить возможные расстройства печени у родственников. Только после этого больного отправляют на диагностику. Сначала делают анализ крови, выявляют вирусные инфекции и иммуноглобулин. Потом пациента отправляют на рентген. Чтобы определить асцит, выполняется ультразвуковое обследование брюшины. С помощью допплерометрии проблемных органов удается определить качество кровообращения.
Стадии течения болезни
Субкомпенсированная
Портальная гипертензия включает три стадии течения:
- Компенсированная — это начальная стадия, которая характеризуется незначительным повышением давления в системе портальной вены, на этой стадии печень еще с помощью своих резервных возможностей справляется с этим повышением, наблюдается увеличение селезенки и печени (печень может и не увеличиваться).
- Субкомпенсированная — к проявлениям этой стадии относится следующее: высокое давление в портальной вене, увеличение селезенки, варикозное расширение вен пищевода, а также желудка, что клинически может сопровождаться кровотечением из этих сосудов, но его может и не быть, печени уже не хватает резервов для того, чтобы справиться с давлением.
- Декомпенсированная — это самая неблагоприятная в плане клиники и прогноза форма заболевания, проявляющаяся значительным увеличением селезенки, печени, варикозно расширенными венами пищевода, желудка, что клинически может сопровождаться кровотечением из этих сосудов, но его может и не быть, появляется асцит, к значительным, серьезным нарушениям кровообращения в системе портальной вены присоединяется нарушение центрального кровообращения (т.е. работы сердца).
Терапия
Шансы на успешное восстановление увеличиваются, если лечение портальной гипертензии выполняется вовремя. Только специалисту нужно доверять проведение терапии. Если заняться самолечением, можно серьезно навредить организму. Терапия портальной гипертензии подразумевает такие процедуры:
- Употребление Пропранолола 2 раза в сутки. При этом выполняется перевязка или склеротерапия сосудов, подверженных варикозу.
- Когда возникает кровотечение, нужно вколоть пациенту 1 мг Терлипрессина. Такую терапию выполняют каждые 4 часа на протяжении суток. Такая методика лечения отличается стабильностью, не провоцирует побочные действия.
Чтобы кровотечение не возникали так часто, нужно вкалывать соматостатин примерно по 250 мг, через несколько часов можно поставить капельницу с этим веществом. Уколы можно делать на протяжении 3-4 дней. Подобные методы лечения нарушают соотношение воды и соли в организме, поэтому нужно внимательно отслеживать, какие продукты употребляются в пищу в процессе лечения. Если развивается асцит, эта методика не используется.
Если портальная гипертензия слишком запущена, лекарствами ничего не удается изменить, приходится применять инвазивную терапию или делать операцию.
Перечислим самые эффективные процедуры:
- Эндоскопическая склеротерапия считается самым популярным способом воздействия, проводимым при портальной гипертензии. Смысл хирургического вмешательства заключается в выполнении тампонады, для этого применяется Соматостатин. Пациенту скалывается склерозант, способствующий склеиванию сосудов. Начинается закупорка, вскоре наблюдается отмирание. Процедура эффективна на 80%.
- Тампонада пищевода. Эта методика выполняется с применением зонда Блэкмора. В желудке размещаются специальные приспособления, через которые в орган поступает воздух. В результате часть пищевода пережимает вену желудка. Устройство нагнетает воздух в течение суток.
- Эндоскопическая перевязка выполняется на желудке и сосудах, подверженных варикозу. Процедура отличается сложностью, эффективностью. Получится сдержать кровотечение, предотвратить последующее развитие болезни.
- Плановые хирургические процедуры выполняются для предотвращения возможных кровотечений, при этом вырезают фрагменты печени или сосудов.
- Пересадка печени считается наиболее радикальным методом решения проблемы портальной гипертензии. Операция проводится в ситуации, когда патология осложняется постоянными кровотечениями или развивается цирроз.
Лечение
В качестве лечения, особо важно первоначально установить основную причину, которая и повлекла за собой такие патологические проявления.
Лечение портальной гипертензии заключается в следующем:
- Пропранолол 20-180 дважды в сутки в сопровождении перевязывания варикозных сосудов.
- При кровотечениях назначаются: терлипрессин 1 мг внутривенно, 1 мг каждые 4 часа в течение суток.
- «Золотым стандартом» при лечении ПГ является эндоскопическая склеротерапия. Проводится тампонада и вводится соматостатин. Это один из самых эффективных методов.
- Тампонада пищевода с использованием зонда Сенгстейкена-Блэйкмора. Зонд вводится в полость желудка, после чего в него напускается воздух, тем самым прижимает вены желудка к его стенкам. Баллон содержится в полости не более 24 часов.
- Эндоскопическая перевязка варикозного расширения изнутри специальными эластичными кольцами. Также один из самых эффективных методов лечения портальной гипертензии, но не во всех случаях возможен, в особенности при стремительной потере крови. Перевязка впоследствии предотвращает рецидивы с кровотечениями.
- Хирургические операции при портальной гипертензии. Предупреждает повторные кровотечения.
- Пациентам с циррозом печени и регулярным кровотечением показана госпитальная хирургия и трансплантация органа. При этом пациентам делается переливание крови. Данный метод лечения применяется за границей в Израиле и Германии.
Благоприятное лечение при портальной гипертензии, будет напрямую зависеть от главной причины, которая повлекла за собой такие последствия. ПГ является довольно серьезным заболеванием и при несвоевременном обращении за консультацией к врачу, несоблюдении всех его рекомендаций и регулярных кровотечениях, нередко приводит к летальному исходу. Ответить на вопрос с точностью, сколько живут люди с ПГ невозможно, так как каждый отдельный случай имеет свои характерные особенности и причины возникновения заболевания. Поэтому так важно вовремя определить заболевание, и своевременно вылечить болезнь.
Осложнения
Если долго не лечиться, могут возникнуть дополнительные проблемы со здоровьем. Чаще всего при этом забивается печень, другие внутренние органы. Перечислим возможные проблемы:
- кровотечение в разных отделах ЖКТ;
- асцит;
- гиперспленизм, по причине которого ухудшается работа иммунитета;
- печеночная недостаточность, при которой часть или весь орган не может выполнять свою работу;
- во время печеночной комы не выполняется очистка крови;
- из-за проблем с органом возникают проблемы с умственной деятельностью;
- язва желудка и проблемы с целостностью ткани;
- неспецифический колит;
- цистит;
- смертельный исход;
Распространенность и прогноз при портальной гипертензии
Портальная гипертензия, осложненная варикозным расширением вен пищевода, сопряжена с высоким риском гибели больного
Заболеваемость портальной гипертензией неизвестна. Ее основная причина – цирроз печени – находится на 10-12 месте среди других причин летального исхода.
Чем выше класс заболевания по Чайлд-Пью, тем хуже прогноз. Так, у детей с врожденной патологией класса А частота варикозного расширения вен пищевода составила 40%, а при классе С – уже 85%. При компенсированном циррозе эти цифры составляют 30%, при декомпенсированном – 70%.
Скорость варикозного расширения вен составляет около 8% в течение первых 2 лет после развития заболевания и к 6 году уже равна 30%. Риск кровотечения в первый год равен 30%.
Что касается распределения по полу, то 60% больных с портальной гипертензией – мужчины, и основная причина этого – алкогольная болезнь и вирусный гепатит. У женщин на первый план выступают венозно-окклюзионная болезнь и первичный билиарный цирроз. У детей основные причины патологии – тромбоз воротной вены и вторичный билиарный цирроз печени.
Варикозное кровотечение является наиболее распространенным осложнением, связанным с портальной гипертензией. Почти у 90% пациентов с циррозом развивается варикозное расширение вен, и примерно у 30% варикозные узлы кровоточат. Предполагаемая смертность при первом эпизоде варикозного кровотечения составляет 30-50%.
После первого эпизода кровотечения в течение года он повторяется у 60-80% пациентов. Примерно 30% из них смертельны.
Способствуют увеличению смертности и осложнения портальной гипертензии:
- печеночная энцефалопатия;
- аспирационная пневмония;
- почечная недостаточность;
- системные инфекции и сепсис;
- бактериальный перитонит;
- асцит (скопление жидкости в брюшной полости);
- гепаторенальный синдром;
- кардиомиопатия, гипотония, нарушения сердечного ритма.
Хирургическое лечение асцита
Развитие цирроза усложняет лечение асцита. Определенный момент патология не реагирует на действие медикаментов. Жидкость в области брюшины ограничивает способность диафрагмы двигаться, появляются проблемы с усвоением кислорода. Пациент слишком часто дышит, ему не хватает воздуха, появляются проблемы со сном, поскольку находиться в горизонтальном положении тяжело. Подобное состояние требует незамедлительного устранения накопившейся жидкости методом лапароцентеза. После такой процедуры из организма выводится примерно 80 л транссудата.
Проблемы с дыханием уходят, пациенту становится легче. Спустя две-три недели жидкость снова собирается в животе в таком же объеме. Делается повторная функция. Иногда в подобных ситуациях в животе делают дренаж, чтобы транссудат все время удалялся без необходимости многократного проведения хирургического вмешательства. Если удалять жидкость слишком часто, из организма будет выводиться белок, в результате будет усиливаться гипотермия, общее самочувствие ухудшается. Поэтому вторичное возникновение напряженного асцита предотвращается консервативными способами.
Проведение операции
Хирургическое лечение у пациентов с циррозом подразумевает сложности. Зачастую таких пациентов возникает много болезней, жизненно важные органы нормально не работают. При проведении операции возникают серьезные риски. Чтобы снизить вероятность летального исхода или осложнений, нужно проводить перитонеовенозное шунтирование. Поскольку асцитическая жидкость по своим характеристикам похожа на плазму, используются механизмы фильтрации и введение обратно в сосудистое русло. При этом застой лимфы удается устранить, жидкость больше не будет направляться в брюшную полость.
Признаки и клинические проявления
Чаще всего пациенты сталкиваются со следующими признаками патологии:
- спленомегалией (в некоторых случаях при ПГ первым симптомом считается именно увеличением размеров селезенки);
- варикозом венозных капилляров пищевода, желудка, живота (голова медузы) и ануса (узлы геморроя);
- асцитом – патологическим скоплением жидкости в брюшной полости, который может сочетаться с гидротораксом;
- болевым синдромом в области живота и правого подреберья;
- отсутствием аппетита, вздутием живота;
- диспепсией;
- симптомами интоксикации;
- общей слабостью;
- потерей веса;
- отеками лодыжек;
- эрозиями на слизистой системы пищеварения.
Если причиной портальной гипертензии стал застой крови на фоне закупорки печеночных протоков, у пациента желтеет кожа. Иногда диагностируется гиперспленизм – уменьшение количества эритроцитов, лейкоцитов, тромбоцитов крови вследствие повышения функции селезенки.
Особого внимания заслуживают признаки ПГ у детей. Они только внепеченочные, проявляются увеличением селезенки, варикозом венозных капилляров пищевода, геморрагиями. Кровотечения при этом возникают крайне редко.
Эндоскопическое лигирование сосудов, подверженных варикозу
Для разных видов кровотечения используют методику гемостаза. Нужно отдавать предпочтение адекватным способам, поскольку другой возможности сдержать кровотечение не представиться. Чтобы выявить места кровоизлияния, выполняется процедура ФЭГДС. С помощью этого метода диагностируется варикоз сосудов пищевода. Определяется область повреждения и характер кровотечения. В наиболее простых случаях можно быстро провести эндоскопическую процедуру. Лигирование считается самым результативным способом остановки кровотечения сосудов, подверженных варикозу. Эффективные технологии достигают 90%, а количество рецидивов минимальное.
Парабазальные склерозирование
В профилактических целях проводятся операции, направленные на уменьшение показателей давления в сосудах с несколькими протокавальными анастомозами. В смысле такой процедуры заключается в создание дополнительных путей оттока крови из места локализации воротной вены с помощью создания:
- Прямого анастомоза.
- Мезентерикоковального.
- Спленореального.
Формирование прямых анастомозов позволяет быстро уменьшить портальное давление из-за переноса крови в область нижней полой вены. При этом нужно предотвратить ухудшение работоспособности печени. Необходимо определить подходящий размер анастомоза. Последнее время популярностью пользуются портокавальные устройства с шириной 6, 8 и 10 мм. Анастомозы позволяют частично сбрасывать портальную кровь в область полой вены. Таким образом удается предотвратить осложнения.
Спленоренальный анастомоз требует устранения селезенки, что может подразумевать трудности в определенных условиях. Иногда во время проведения операции пациент теряет много крови.
Возможности ультразвуковых исследований при портальной гипертензии у детей
УЗИ сканер HS70
Точная и уверенная диагностика.
Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Портальная гипертензия — одна из основных причин тяжелых пищеводно-желудочных кровотечений у детей, нередко приводящая к летальности. Кроме того, исходом портальной гипертензии у детей с болезнями печени может быть печеночная или почечная недостаточность. В связи с этим крайне важно своевременное распознавание самого синдрома и установление причин его развития.
Впервые термин «портальная гипертензия» ввел в 1928 г. английский хирург A. McJandoe. В основе ее развития лежит препятствие току крови по системе воротной вены. Обычно предполагается блокада механического характера, но встречаются случаи функционального, спастического происхождения блокады какого-либо отдела портальной системы. Различаются следующие типы портальной гипертензии: внутрипеченочная (цирроз печени, врожденный фиброз печени, выраженная жировая инфильтрация, внутрипеченочные опухоли); внепеченочная (тромбоз воротной и селезеночной вен, изолированный тромбоз селезеночной вены, порок развития воротной вены, сдавление вен опухолью или лимфатическими узлами); надпеченочная (синдром Budd-Chiari, сдавление печеночных вен опухолью); смешанная (когда порок развития воротной вены осложняется хроническим вирусным гепатитом, а затем и циррозом печени или аномалия развития воротной вены сочетается с фиброзированием печени).
Патогенез портальной гипертензии при различных типах блокады портальной системы различен. Самой частой причиной печеночной формы гипертензии является цирроз печени, когда на фоне воспаления происходит склерозирование с последующим фиброзированием портальных трактов, развитие узлов регенерации, нарушение структуры печеночных долек, сдавливание сосудистых структур, в том числе внутрипеченочных разветвлений воротной вены. Нарушение же организации долек ведет к изменению внутридолькового кровообращения и является причиной развития некрозов в центре дольки, фиброза и выраженной клеточной инфильтрации с пролиферацией купферовских клеток. Последние могут вдаваться в просвет синусоидов, суживать их, приводя к повышению давления в портальной системе. Затруднение тока крови по системе воротной вены и повышение портального давления приводят к увеличению и гиперплазии селезенки. Далее портальная гипертензия вызывает развитие коллатералей как природных, так и новых портокавальных связей: через венечную вену желудка к венозному сплетению пищевода и далее через непарную и полунепарную вены с системой верхней полой вены. Расширяются вены пищевода. В развитии портокавальных анастомозов участвуют vv.epigastricae, образуя «голову медузы», чаще наблюдаемую у взрослых пациентов. Синдром Cruveillier-Baumgarten наиболее характерен для детского возраста при врожденном фиброзе печени. При развитии портокавальных коллатералей через v.mesentericae inferior увеличиваются геморроидальные вены. В возникновении развивающегося при портальной гипертензии асцита играют роль стаз в портальной и лимфатической системе органов брюшной полости и нарушение инактивации кортикостероидов, в частности, альдостерона.
В отличие от механизма внутрипеченочной портальной гипертензии внепеченочный, на первый взгляд, представляется более простым. Практическое отсутствие ствола и разветвлений воротной вены при врожденном генезе развития, облитерированный или суженный ее просвет в результате тромбоза или экстравазального сдавления приводит к повышению сопротивления кровотоку, ведущего к стабильному увеличению портального давления до 300-500 мм водяного столба (N до 120-180 мм водяного столба) и развитию гипердинамического типа гемоциркуляции в сосудах бассейна воротной вены, с выраженным артериовенозным шунтированием в органах, увеличивая нагрузку на сосуды, с последующими их морфологическими изменениями. Их выраженность зависит от продолжительности и тяжести течения заболевания.
Развитие портальной гипертензии при надпочечной блокаде кровообращения чаще всего обусловлено рестриктивным перикардитом, сужением печеночных вен или нижней полой вены выше ее слияния с печеночными венами (болезнь Chiari), сужением нижней полой и/или печеночной вен в результате врожденной перегородки, тромба, опухоли, гипертрофированной хвостатой доли печени, что в конечном счете ведет к расстройству крово- и лимфообращения в органах и тканях нижележащих отделов.
Основными методами исследования больных с подозрением на портальную гипертензию кроме общепринятых физикальных являются ангиографические, эндоскопические и ультразвуковые в сочетании с допплерографией (в цветном и обычном режимах). Все перечисленные методы взаимодополняют друг друга. Об относительной конкурентности может идти речь между ангиографией и допплерографией. Однако, учитывая безвредность ультразвукового метода и относительную простоту его применения, нужно признать, что он должен использоваться первым у каждого ребенка с увеличенной селезенкой и другими признаками, позволяющими подозревать портальную гипертензию. А затем, ориентируясь на полученные результаты, решать вопрос о проведении рентгеноконтрастных исследований.
Наиболее частой формой портальной гипертензии у детей по сравнению с другими является внепеченочная блокада портального кровообращения, частота которой в дифференциальной диагностике портальной гипертензии достигает 50-88%. При этом у взрослых этот показатель находится в пределах 10% [1, 2]. Такая разница объясняется тем, что основная причина развития гипертензии — это первичное поражение вен портальной системы, которое в ряде случаев сопровождается фиброзированием паренхимы печени.
Эхографическое исследование органов брюшной полости у детей с подозрением на внепеченочнув форму портальной гипертензии практически в 100% случаев позволяет правильно предположить диагноз. Печень, как правило, нормального или уменьшенного размера. Последнее обусловлено значительным снижением портального кровотока при развитии фиброзирования паренхимы, наблюдаемом у 60-70% детей. При врожденном фиброзе от паренхимы регистрируются множественные мелкие сильные эхосигналы, рассеянные по всей площади среза органа (рис. 1). Воротная вена изменена, при этом может наблюдаться отсутствие просвета ее ствола или основных ветвей (рис. 2), наличие множественных тонких извитых сосудов с гиперэхогенными стенками, собранных вместе — ангиоматозная трансформация (рис. 3), наличие тромба, сужающего или закрывающего просвет сосуда, или локальное сужение просвета, что приводит к развитию коллатералей, видимых как анэхогенные узкие, извитые тубулярные структуры, идущие рядом с основным стволом (рис. 4). Такие изменения воротной вены приводят к значительному замедлению кровотока. Цветное допплеровское картирование облегчает качественную оценку состояния воротной вены, позволяя определить направление кровотока (гепатопетальный — к печени или гепатофугальный — от печени).
Рис. 1.
Эхограмма печени при врожденном фиброзе.
Рис. 2.
Эхограмма воротной вены без просвета.
Рис. 3.
Эхограмма воротной вены при ангиоматозной трансформации.
Рис. 4.
Эхограмма правой ветви воротной вены с коллатералями, развившимися из-за тромбоза ствола.
Портальная гипертензия при ее внепеченочной форме постепенно приводит к ряду вторичных изменений. Селезенка увеличивается, наблюдается мелкоочаговое или диффузное мелкоочаговое уплотнение паренхимы, уплотнение стенок мелких сосудов, некоторые могут быть тромбированными (рис. 5). Селезеночная вена расширена, часто извита в области ворот. Скорость кровотока по ней, как правило, сохраняется, но значительно увеличивается показатель объемного кровотока. Селезеночная артерия несколько расширена, что приводит к увеличению индекса резистентности и свидетельствует об увеличении периферического сопротивления, косвенно подтверждая данные эхографии о состоянии паренхимы селезенки.
Рис. 5.
Эхограмма селезенки, тромбоз мелких ветвей селезеночной вены.
Малый сальник у детей обычно не визуализируется при эхографическом обследовании, однако при портальной гипертензии он часто утолщается и становится видимым как эхогенное тканевое образование с нечеткими краями, расположенное между передней поверхностью поджелудочной железы и задней поверхностью желудка, или, eсли желудок не виден, то задней поверхностью печени (рис. 6).
Рис. 6.
Эхограмма утолщенного малого сальника. Р — поджелудочная железа; ST — желудок.
В норме стенки желчного пузыря обычно не видны, но допускается их утолщение до 2 мм. При портальной гипертензии желчный пузырь, как правило, деформирован, с резко утолщенными стенками (рис. 7). В некоторых случаях в стенках могут быть видны варикозно расширенные сосуды, что особенно хорошо демонстрируется при использовании цветного допплеровского картирования в энергетическом режиме.
Рис. 7.
Эхограмма желчного пузыря с резко утолщенными стенками, содержащими варикозно расширенные сосуды, и уменьшенным просветом (режим ЦДК).
При тяжелой форме портальной гипертензии развиваются венозные коллатерали, некоторые из которых могут быть видны: это венечные, желудочно-пищеводные, определяемые между левой долей печени и головкой, телом поджелудочной железы как анэхогенные округлые или тубулярные структуры (рис. 8). Варикозно расширенные вены пищевода могут быть определены при продольном сканировании в области аорты. В связи с различной направленностью кровотока из-за извитости сосудов при ЦДК демонстрируется его смешанный характер. При исследовании печени при фиброзе отмечается проходимая пупочная вена, имеющая иногда неровные стенки и направленная от области бифуркации воротной вены к поверхности печени в цефально-латеральном направлении (рис. 9).
Рис. 8.
Эхограмма области головки поджелудочной железы с сосудистыми коллатералями (стрелка). L — печень; P — поджелудочная железа; VL — селезеночная вена; AO — аорта; IVC — нижняя полая вена.
Рис. 9.
Эхограмма расширенной пупочной вены. VU — пупочная вена; VP — воротная вена.
При печеночной форме портальной гипертензии, основной причиной развития которой у детей является цирроз печени, наблюдаются практически все те же вторичные изменения. Воротная же вена значительно расширена, достигая в диаметре 20 мм, стенки ее утолщены. Скорость кровотока по вене снижена, но за счет увеличения диаметра возрастает и величина объемного кровотока. Так же увеличение этого показателя имеет место и в селезеночной вене. Изменения, происходящие в портальной системе, ведут к перераспределению объема крови — его увеличению в сосудах портальной системы и снижению в других жизненно важных органах (мозг, почки) [3]. При более выраженных нарушениях кровообращения по воротной вене происходит накопление жидкости в брюшной полости, которая при ее малом количестве прежде всего локализуется в латеральных каналах и малом тазу, а затем в околопеченочном и околоселезеночном пространствах.
Наиболее эффективным способом лечения внепеченочной портальной гипертензии и основного ее осложнения — рецидивов острых кровотечений из варикозных вен пищевода и желудка — является создание портокавальных анастомозов, позволяющих создать условия для декомпрессии портальной системы. Выбор сосудов для создания шунта определяется индивидуально, с учетом гемодинамических параметров и возраста пациента. В последние годы предпочтение отдается спленоренальным, мезокавальным по типу «бок в бок». Все данные о кровотоке в потенциально используемых сосудах могут быть получены при допплеровском исследовании. Наблюдение же за характером кровотока после проведенной операции и сопоставление получаемых данных с первичными дает возможность говорить об эффективности проведенного оперативного лечения как сразу после него, так и в позднем катамнезе. Одним из осложений после проведенной операции шунтирования является образование гематомы (4-5% наблюдений), которая на эхограмме представляется округлым эхосвободным образованием с довольно четкими границами. Динамическое исследование позволяет контролировать состояние гематомы и регрессию ее размеров.
Одним из способов лечения внутрипеченочной портальной гипертензии является удаление селезенки. К основным возможным послеоперационным осложнениям, диагностируемым при УЗИ, следует отнести кровотечение с образованием гематомы, развитие абсцесса, реактивные изменения в соседних органах, чаще всего поджелудочной железе.
При синдроме Badd-Chiari на эхограммах определяется сужение или отсутствие просвета нижней полой вены или одной из печеночных вен, в частности, гипертрофированной хвостатой долей (рис. 10). При хронизации процесса образуются визуализируемые при УЗИ венозные коллатерали, сосуд выше облитерации или сужения расширен, кровоток значительно ослаблен.
Рис. 10.
Эхограмма нижней полой вены (продольный срез). Просвет вены сужен гипертрофированной хвостатой долей.
Таким образом, ультразвуковое исследование органов брюшной полости является методом выбора на раннем как амбулаторном, так и стационарном диагностическом этапах обследования детей с портальной гипертензией, включает обязательную допплеровскую оценку состояния кровотока, позволяет с высокой точностью подтвердить и определить причину портальной гипертензии, а сравнительный анализ данных, полученных в различные сроки терапевтического и хирургического лечения заболевания — оценить его эффективность.
Литература
- Пациора М.Д. Хирургия портальной гипертензии. М.: Медицина. 1974. С. 232.
- Van Vroonhen T., Molenaar J. Distal splenorenal shunt for decompression of portal hypertension in children with cystic fibrosis// Surg.Ginecol.Obst. 1979. V.149. P.559-566.
- Аббас Н.М. Состояние центральной и периферической гемодинамики у детей с хроническими заболеваниями печени: Дисс… канд. мед. наук. — М., 1996. С.160.
УЗИ сканер HS70
Точная и уверенная диагностика.
Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Принцип проведения трансплантации
Цирроз считается результатом разных воспалений. Патология может развиваться быстро или медленно. На этапе явных функциональных расстройств начинается портальная гипертензия. Для болезни свойственен асцитический синдром и кровотечение из сосудов пищевода. Пациенты получают инвалидность, нередко умирают по причине осложнений. Консервативные способы лечения на данном этапе не дают результата.
Сегодня используется большое количество хирургических методов воздействия. Большая часть из них отличается паллиативным характером. Возможность пересадки печени позволяет избавиться от серьезных нарушений, большого количества разных болезней и преобразования органов. Плюсы донорства тканей и органов люди научились решать на сегодняшний день.
Современные взгляды на лечение портальной гипертензии
Основные задачи лечения
- снижение давления в воротной вене. С этой целью используются нитраты (не рекомендуется монотерапия) — Изосорбида-5-мононитрат; бета-блокаторы неселективного характера — Пропранолол, Обзидан, Анаприлин, Тимолол, Надолол. Наиболее эффективно использование комбинации двух групп препаратов, но заметными минусами является негативное воздействие на почки;
- профилактика и остановка кровотечений. Первый пункт заключается в назначении бета-адреноблокаторов при наличии варикозных узлов небольшого диаметра и их эндоскопическом легировании (перевязке при помощи эластичных колец). Для остановки кровотечений используют тампонаду (сдавление изнутри) пищевода при помощи специального зонда Блэкмора; эндоскопическую склеротерапию — введение в полость пищевода специальных веществ, способствующих закупорке просвета вен — Соматостатина, Октреотида.
- нормализация системы свёртывания крови. Сводится к назначению препаратов, содержащих витамин К (Викасол и др.);
- коррекция печёночной недостаточности — осуществляется путём назначения гепатопротекторных средств (Гепасол, Тиотриазолин, Берлитион, Эссенциале), белковозамещающих препаратов и дезинтоксикационной терапии (Альбумин, Реополиглюкин, Трисоль);
- связывание токсических продуктов азотистого обмена. Для данной цели используется препарат, способствующий связыванию и выводу из организма аммиака — Гепа-мерц.
Оперативное лечение
При неэффективности консервативной терапии переходят к хирургическим вмешательствам. В настоящее время используют:
- портосистемное шунтирование — накладывание искусственных коллатералей с целью разгрузки печени;
- эмболизацию селезёночной артерии ретроэндоваскулярным способом — используется для устранения явлений гиперспленизма;
- спленэктомию — сводится к удалению селезёнки, если она увеличена до такой степени, что сдавливает органы брюшной полости;
- трансплантацию (пересадку) печени — позволяет уменьшить проявления портальной гипертензии, асцита, печёночной энцефалопатии, повторных кровотечений из варикозно расширенных вен.